
十年维拉帕米稳态下的隐匿风暴:一场多重用药诱发钙通道阻滞剂中毒的生死博弈 | 病例“心”编
一位服用维拉帕米 长达十年的高血压
长达十年的高血压 患者,因COVID-19阳性联用奈玛特韦/利托那韦
患者,因COVID-19阳性联用奈玛特韦/利托那韦 数日后,引发完全性心脏传导阻滞和休克
数日后,引发完全性心脏传导阻滞和休克 ,陷入危机。最终患者确诊为维拉帕米中毒
,陷入危机。最终患者确诊为维拉帕米中毒 ,通过液体复苏、升压治疗及钙剂拮抗,患者成功脱险,心律恢复正常。这一罕见病例揭示了多重用药中潜藏的药代动力学风暴,提示在COVID-19治疗中需高度警惕药物相互作用,尤其是对长期服用维拉帕米及合并肝肾疾病的患者,避免可预防的严重并发症。
,通过液体复苏、升压治疗及钙剂拮抗,患者成功脱险,心律恢复正常。这一罕见病例揭示了多重用药中潜藏的药代动力学风暴,提示在COVID-19治疗中需高度警惕药物相互作用,尤其是对长期服用维拉帕米及合并肝肾疾病的患者,避免可预防的严重并发症。
病例概述
01现病史
患者,女,58岁,因咳嗽 、气促伴恶心就诊。
、气促伴恶心就诊。
入院前近一周,患者于家中检测COVID-19结果呈阳性,并自行到急救诊所就医,接受奈玛特韦/利托那韦治疗。数日后,患者因服药期间症状加重至医院就诊。患者自述近3日下肢水肿 加重,遂自行将呋塞米
加重,遂自行将呋塞米 用量增加一倍。患者否认端坐呼吸、阵发性夜间呼吸困难
用量增加一倍。患者否认端坐呼吸、阵发性夜间呼吸困难 或体重增加。急诊科查体显示患者血流动力学不稳定,脉率
或体重增加。急诊科查体显示患者血流动力学不稳定,脉率 34次/分,血压75/ 39 mmHg,经4L鼻导管吸氧下的血氧饱和度为95%。体格检查发现患者嗜睡,心动过缓和双肺满布哮鸣音,未闻及心脏杂音
34次/分,血压75/ 39 mmHg,经4L鼻导管吸氧下的血氧饱和度为95%。体格检查发现患者嗜睡,心动过缓和双肺满布哮鸣音,未闻及心脏杂音 。
。
02既往史
患者既往有2型糖尿病、肥胖、高脂血症 、高血压、代谢功能障碍相关脂肪性肝肝炎
、高血压、代谢功能障碍相关脂肪性肝肝炎 继发肝硬化
继发肝硬化 、慢性肾脏病
、慢性肾脏病 以及既往已治疗的莱姆病
以及既往已治疗的莱姆病 病史。
病史。
患者每日用药包括螺内酯 (50 mg)、维拉帕米(180 mg,每天2次)、呋塞米(40 mg,每天1次)、乳果糖
(50 mg)、维拉帕米(180 mg,每天2次)、呋塞米(40 mg,每天1次)、乳果糖 (20 g/mL)、利福昔明
(20 g/mL)、利福昔明 (1100 mg)、二甲双胍
(1100 mg)、二甲双胍 (1000 mg)和重组人胰岛素注射液
(1000 mg)和重组人胰岛素注射液 U-500胰岛素(15 U,每天2次)。患者因预防性治疗偏头痛
U-500胰岛素(15 U,每天2次)。患者因预防性治疗偏头痛 和控制高血压,持续服用维拉帕米(180 mg,每天2次)已逾10年,剂量未作调整。
和控制高血压,持续服用维拉帕米(180 mg,每天2次)已逾10年,剂量未作调整。
03鉴别诊断
患者就诊时存在心脏传导阻滞,因此初步鉴别诊断包括与既往莱姆病感染史相关的莱姆心脏炎,或COVID-19感染后遗症(如心肌炎 )。然而,在综合考虑患者奈玛特韦/利托那韦的用药时间、急性肾损伤
)。然而,在综合考虑患者奈玛特韦/利托那韦的用药时间、急性肾损伤 以及符合维拉帕米中毒的临床表现后,高度怀疑患者为维拉帕米中毒。
以及符合维拉帕米中毒的临床表现后,高度怀疑患者为维拉帕米中毒。
04辅助检查
实验室检查异常结果包括:乳酸4.3 mmol/L;肌酐1.89 mg/dL(基线值1.1 mg/dL);血红蛋白 9.7 g/dL;高敏肌钙蛋白
9.7 g/dL;高敏肌钙蛋白 35 ng/L;钾5.2 mmol/L;镁2.2 mmol/L;促甲状腺激素为2.780 mIU/mL。COVID-19聚合酶链反应(PCR)检测结果为阳性。胸部X线检查未见明显异常。患者拒绝接受经胸超声心动图
35 ng/L;钾5.2 mmol/L;镁2.2 mmol/L;促甲状腺激素为2.780 mIU/mL。COVID-19聚合酶链反应(PCR)检测结果为阳性。胸部X线检查未见明显异常。患者拒绝接受经胸超声心动图 (TTE)检查。12导联心电图
(TTE)检查。12导联心电图 显示间歇性完全性心脏传导阻滞伴交界性逸搏心律,以及新发右束支传导阻滞(图1)。
显示间歇性完全性心脏传导阻滞伴交界性逸搏心律,以及新发右束支传导阻滞(图1)。
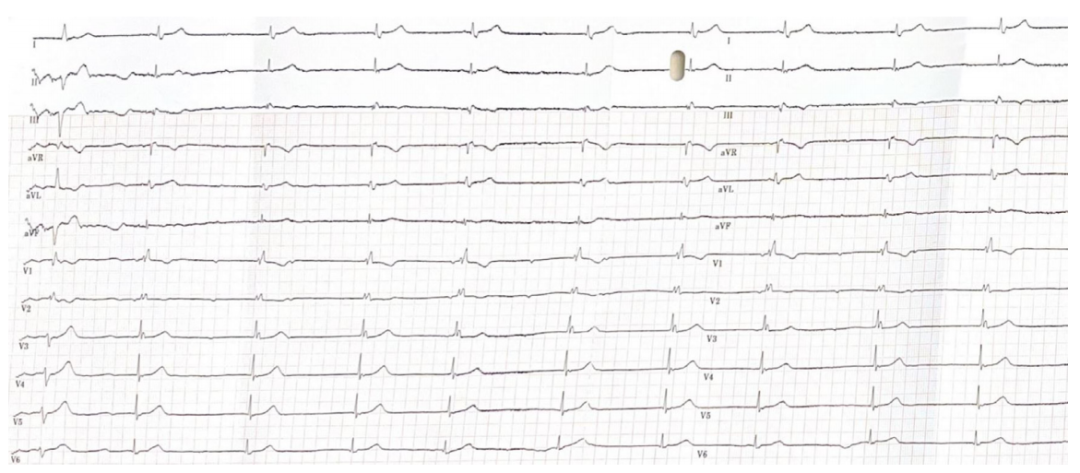
图1 入院心电图
05治疗经过
患者接受2L液体复苏后仍持续低血压,需短暂使用静脉输注去甲肾上腺素 维持血压。经多学科会诊后,予葡萄糖酸钙
维持血压。经多学科会诊后,予葡萄糖酸钙 2g静脉给药,并于胸骨前区及后背放置体外起搏电极片。在完成葡萄糖酸钙治疗约30分钟后,患者出现交界性心动过缓伴持续性右束支传导阻滞(图2)。次日上午,经支持治疗后患者心律转复为正常窦性心律,传导异常完全消失(图3)。住院期间未再出现其他异常情况,肾功能及低血压状况逐渐改善,未再发心律失常
2g静脉给药,并于胸骨前区及后背放置体外起搏电极片。在完成葡萄糖酸钙治疗约30分钟后,患者出现交界性心动过缓伴持续性右束支传导阻滞(图2)。次日上午,经支持治疗后患者心律转复为正常窦性心律,传导异常完全消失(图3)。住院期间未再出现其他异常情况,肾功能及低血压状况逐渐改善,未再发心律失常 。短期住院观察后,患者出院居家休养,后续安排初级保健医生及心脏专科医生随访。
。短期住院观察后,患者出院居家休养,后续安排初级保健医生及心脏专科医生随访。
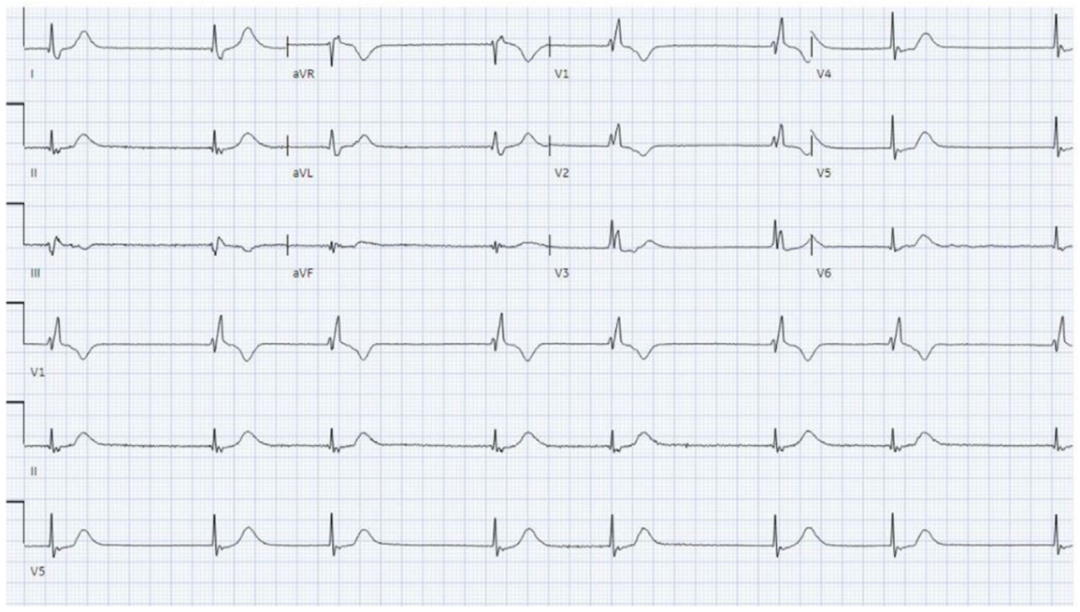
图2 接受葡萄糖酸钙治疗后的心电图
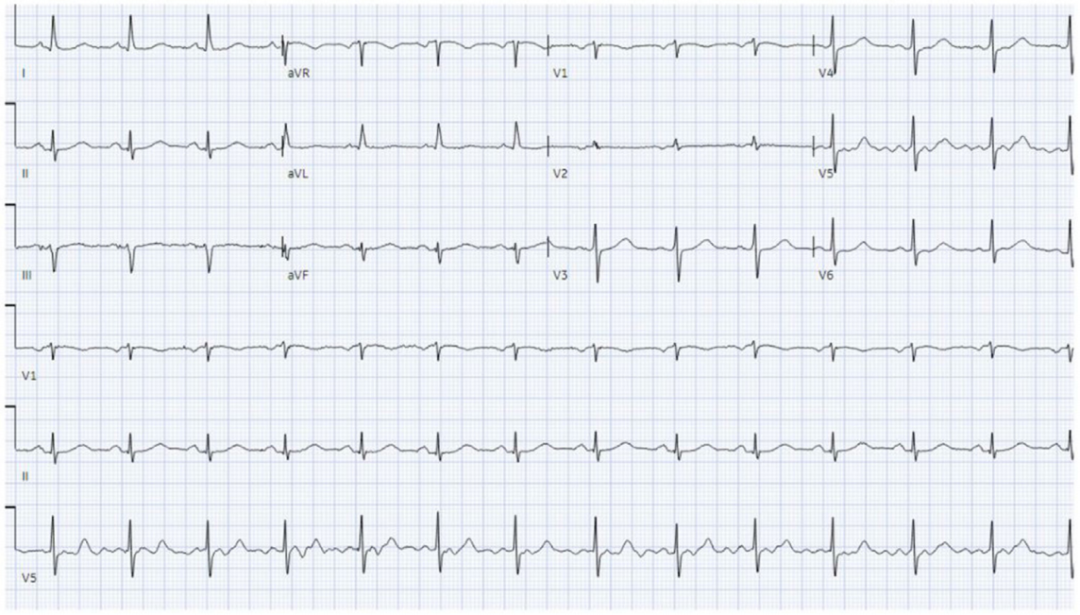
图3 出院时心电图
06结局及随访
患者住院3天后病情稳定出院,维拉帕米于出院后停用。出院3个月后,患者开始服用地尔硫䓬180mg每天2次,症状未再复发。鉴于此次心脏毒性具有自限性,预计无需进一步干预治疗。近期门诊记录显示患者恢复良好,但对其多重用药可能导致的药物相互作用仍感焦虑。
讨论
文献中关于维拉帕米药物相互作用导致中毒的报道较为罕见。本文病例提示临床医生,对正在服用维拉帕米(尤其是合并肾功能不全)的患者需要使用奈玛特韦/利托那韦时,需特别警惕其可能引发的严重并发症。
在分析本案例过程中,医生采用包含10个问题的诺氏评估量表(Naranjo Scale)评估药物不良反应的真实可能性,最终得分为6分,提示该反应属“可能”级别。尽管该量表存在某些不适用于本案例的局限性,但医生认为其有助于进一步明确药物相互作用特征。支持药物相互作用的诺氏评分证据包括:该药物反应存在文献记载的相互作用、反应时序符合逻辑、停药治疗后出现临床缓解,且不良事件经心电图等客观证据证实。量表问题5要求考虑其他潜在病因——COVID-19心肌炎亦可解释该患者的肌钙蛋白升高及完全性心脏传导阻滞。遗憾的是,患者拒绝接受TTE检查。由于缺乏TTE或心脏磁共振检查,无法完全排除COVID-19心肌炎病因,故在诺氏量表评分中作为减分项予以考量。
维拉帕米是一种非二氢吡啶类钙通道阻滞剂,可抑制L型电压门控钙通道。该抑制作用可导致心肌收缩力降低、心脏传导速度减慢及外周血管扩张,临床常用于高血压及心绞痛 治疗。其毒性反应主要表现为心血管系统并发症,包括心动过缓、低血压及传导异常(如窦性停搏、莫氏I型房室传导阻滞
治疗。其毒性反应主要表现为心血管系统并发症,包括心动过缓、低血压及传导异常(如窦性停搏、莫氏I型房室传导阻滞 或伴交界性心律[包括交界性心动过缓]的完全性心脏传导阻滞)。本病例中,患者出现的低血压与完全性心脏传导阻滞伴交界性逸搏心律,均为维拉帕米中毒的潜在征象。
或伴交界性心律[包括交界性心动过缓]的完全性心脏传导阻滞)。本病例中,患者出现的低血压与完全性心脏传导阻滞伴交界性逸搏心律,均为维拉帕米中毒的潜在征象。
维拉帕米经在肝脏中经历广泛代谢,主要通过细胞色素P450(CYP)酶系统代谢,其中最主要的代谢酶是CYP3A4、CYP3A5和CYP2C8,仅有不足5%以原型经尿液排泄。值得注意的是,维拉帕米本身是CYP3A4的强效抑制剂。而奈玛特韦/利托那韦中的利托那韦则是临床使用的强效CYP3A4酶抑制剂之一。在本病例中,维拉帕米代谢所需的CYP3A4同时受到维拉帕米自身和利托那韦的双重抑制,导致患者血清中维拉帕米有效浓度升高。另一个值得探讨的毒性加重因素是该患者的基础肝功能。患者早在十余年前即被诊断为代谢功能障碍相关脂肪性肝炎肝硬化,期间出现过肝性脑病 和腹水
和腹水 等并发症。患者自述规律服药并定期接受肝病专科随访,筛查和影像学检查也按时完成。其既有的肝功能异常可能加剧了维拉帕米与奈玛特韦/利托那韦之间的相互作用。此外,对于存在肾功能损害(如本例合并急性肾损伤)的患者,肾脏排泄在维拉帕米清除中的作用可能更加突出。这主要源于肾小球滤过率下降导致的药物排泄减少,以及可能伴随的药物分布改变。因此,肾功能不全患者即使接受标准剂量治疗,其血清维拉帕米浓度升高的风险显著增加,更易出现毒性反应。综上,本例患者因药物代谢和排泄途径同时受损,最终导致维拉帕米达到毒性浓度。虽然奈玛特韦/利托那韦说明书中已提及该相互作用,但由于降压药与抗病毒药物的作用机制看似无直接关联,临床实践中仍存在意外联用风险,且这种风险易被忽视和低估。
等并发症。患者自述规律服药并定期接受肝病专科随访,筛查和影像学检查也按时完成。其既有的肝功能异常可能加剧了维拉帕米与奈玛特韦/利托那韦之间的相互作用。此外,对于存在肾功能损害(如本例合并急性肾损伤)的患者,肾脏排泄在维拉帕米清除中的作用可能更加突出。这主要源于肾小球滤过率下降导致的药物排泄减少,以及可能伴随的药物分布改变。因此,肾功能不全患者即使接受标准剂量治疗,其血清维拉帕米浓度升高的风险显著增加,更易出现毒性反应。综上,本例患者因药物代谢和排泄途径同时受损,最终导致维拉帕米达到毒性浓度。虽然奈玛特韦/利托那韦说明书中已提及该相互作用,但由于降压药与抗病毒药物的作用机制看似无直接关联,临床实践中仍存在意外联用风险,且这种风险易被忽视和低估。
值得注意的是,对于维拉帕米中毒,目前尚未形成被广泛认可的治疗模式。如本病例所示,临床可通过给予葡萄糖酸钙拮抗钙通道阻滞效应,并应用血管升压药维持血流动力学稳定。对于症状性心动过缓可使用阿托品 ,利用大剂量胰岛素的正性肌力作用,以及采用亲脂性乳剂结合亲脂性维拉帕米。在重症病例中,可能需要实施心脏起搏、气管插管甚至体外膜肺氧合(ECMO)等高级生命支持手段。
,利用大剂量胰岛素的正性肌力作用,以及采用亲脂性乳剂结合亲脂性维拉帕米。在重症病例中,可能需要实施心脏起搏、气管插管甚至体外膜肺氧合(ECMO)等高级生命支持手段。
结语
临床医师应警惕COVID-19患者使用诸多新型药物及疗法可能产生的副作用与并发症。目前,关于奈玛特韦/利托那韦与维拉帕米相互作用的病例报告罕见。虽然维拉帕米中毒多由非意外过量导致,但本例展示了两种看似无关药物因药代动力学相互作用引发潜在致死风险的罕见案例。本病例为奈玛特韦/利托那韦与维拉帕米药物相互作用提供了实例,以期进一步降低可预防的发病与死亡。
信源:Evan Offord, Michelle Nabi, Michael Mankbadi, etal. Complete Heart Block Triggered by Nirmatrelvir-Ritonavir and Verapamil. JACC: Case Reports, Volume 30, Issue 8, 2025, 103238, ISSN 2666-0849. https://doi.org/10.1016/j.jaccas.2025.103238.
