
两例CHD2基因突变癫痫性脑病病例报道
作者:贺晶 ,张冰
,张冰 清,王海祥,史洁,周文静,清华大学玉泉医院癫痫
清,王海祥,史洁,周文静,清华大学玉泉医院癫痫 中心
中心
1997 年,Woodage 和他的同事详细描述了CHD2 基因。CHD2 基因(OMIM 602119)是位于15q26. 1。它包含39 个外显子。CHD2 基因编码的CHD2 蛋白是染色体 结构域解旋酶DNA 结合(chromodomain helicase DNA-binding,CHD)蛋白家族的一员。CHD2 参与了基因激活和抑制、DNA 重组和修复、细胞周期调控、发育和细胞分化等过程。因此,这些蛋白的失调与各种人类发育障碍有关,如孤独症谱系障碍
结构域解旋酶DNA 结合(chromodomain helicase DNA-binding,CHD)蛋白家族的一员。CHD2 参与了基因激活和抑制、DNA 重组和修复、细胞周期调控、发育和细胞分化等过程。因此,这些蛋白的失调与各种人类发育障碍有关,如孤独症谱系障碍 ,智力障碍和癫痫。CHD2 基因突变可导致发育性癫痫性脑病94 型(OMIM:615369)。国内外报道的例数不多。中国人癫痫确诊病例中分析CHD2 基因突变的患病率为2. 8% 。本文报告了清华大学玉泉医院收治的2 例CHD2 基因突变患者,分析其脑电图
,智力障碍和癫痫。CHD2 基因突变可导致发育性癫痫性脑病94 型(OMIM:615369)。国内外报道的例数不多。中国人癫痫确诊病例中分析CHD2 基因突变的患病率为2. 8% 。本文报告了清华大学玉泉医院收治的2 例CHD2 基因突变患者,分析其脑电图 、基因、影像及临床特点。
、基因、影像及临床特点。
1. 资料与方法
1. 1 一般资料
1.1. 1 患者1
患儿男性,就诊时3 岁11 个月。10 个月龄起病,表现为下肢无力,发软,跌倒发作,每天数次。给予德巴金 治疗,未见疗效。1 岁1 个月发作形式转变为发呆,每周数次。加服拉莫三嗪
治疗,未见疗效。1 岁1 个月发作形式转变为发呆,每周数次。加服拉莫三嗪 治疗,未见疗效。3 岁5 个月龄发作形式转变为身体节律性抖动几下,双眼睑眨动,伴随发呆,身体逐渐往下,每天发作20 余次。加服左乙拉西坦
治疗,未见疗效。3 岁5 个月龄发作形式转变为身体节律性抖动几下,双眼睑眨动,伴随发呆,身体逐渐往下,每天发作20 余次。加服左乙拉西坦 治疗未见明显疗效。发作与热敏感无关。患者发病前运动发育落后,不会坐。就诊时会跑跳,但跑不稳,不会单腿跳。对自己名字有反应,其余问题无法回答。家族中无类似患者。
治疗未见明显疗效。发作与热敏感无关。患者发病前运动发育落后,不会坐。就诊时会跑跳,但跑不稳,不会单腿跳。对自己名字有反应,其余问题无法回答。家族中无类似患者。
1.1. 2 患者2
患儿男性,就诊时4 岁8 个月。3 岁出现双眼上翻,数秒即过,100 多次/ 天,口服德巴金控制1 周,之后再次发作。加服托吡酯 2 周未发作。后再发作,表现为快速点头、双眼上翻,眨眼,数秒即过,少时2 ~ 3 次/ 周,多时2 ~3 次/ 天。3 岁半时开始生酮饮食治疗,治疗5 个月无效,转为普通饮食。
2 周未发作。后再发作,表现为快速点头、双眼上翻,眨眼,数秒即过,少时2 ~ 3 次/ 周,多时2 ~3 次/ 天。3 岁半时开始生酮饮食治疗,治疗5 个月无效,转为普通饮食。
4 岁在此基础上又出现了另外一种发作类型,表现为发呆,1 ~2 s 即过,有时继发双眼上翻,身体抖一下,持续10 多秒, 数百次/ 天。加服左乙拉西坦未见疗效。后多次调药拉莫三嗪、卫克泰、氯巴占 、唑尼沙胺
、唑尼沙胺 仍未见疗效。1 岁多出现1 次持续状态,当时体温38. 7 ℃出现意识丧失,双眼上翻,持续1 个多小时,使用安定后好转。发病前生长发育里程碑落后。目前会跑,能跳,能单脚站。可进行精细活动,喜欢用左手、左脚。语言表达可,能说10 个字句子,简单理解可。幼儿孤独症筛查为高风险。对自己名字有反应。家族中未见类似患者。
仍未见疗效。1 岁多出现1 次持续状态,当时体温38. 7 ℃出现意识丧失,双眼上翻,持续1 个多小时,使用安定后好转。发病前生长发育里程碑落后。目前会跑,能跳,能单脚站。可进行精细活动,喜欢用左手、左脚。语言表达可,能说10 个字句子,简单理解可。幼儿孤独症筛查为高风险。对自己名字有反应。家族中未见类似患者。
1. 2 基因检测方法
获取患儿及其父母外周血样2 ~4 mL。采用磁珠法血液基因组DNA 小量提取试剂盒(英芮诚生化科技)提取基因组DNA。对家系三人基因组DNA 进行高通量测序,根据dbNSFP、1 000 g、gnomAD 等数据库进行筛选,并通过有害性预测软件Polyphen2、LRT、SIFT 等进行分析,分析出疾病的候选致病突变。
对筛查发现的变异,采用PCR-Sanger 测序法进行验证。利用UCSC Genome Browser Home 软件(https:/ / www. genome. ucsc. edu)对各物种的CHD2 氨基酸 序列进行比对,分析突变氨基酸的保守性;采用UCSF chimera 软件( https:/ / www. cgl. ucsf. edu/chimera/ )分别对野生型和突变型蛋白进行3D 建模,比较他们之间的差异,分析CHD2 基因突变对蛋白空间结构影响程度。最后,根据美国医学遗传学与基因组学学会(American College of Medical Genetics,ACMG)制定的遗传变异标准与指南解读基因突变数据。
序列进行比对,分析突变氨基酸的保守性;采用UCSF chimera 软件( https:/ / www. cgl. ucsf. edu/chimera/ )分别对野生型和突变型蛋白进行3D 建模,比较他们之间的差异,分析CHD2 基因突变对蛋白空间结构影响程度。最后,根据美国医学遗传学与基因组学学会(American College of Medical Genetics,ACMG)制定的遗传变异标准与指南解读基因突变数据。
2. 结 果
2. 1 患者1
脑电图(10 - 20 国际系统,采样率500 Hz;Nihon Kohden,Tokyo,Japan)的情况见图1。两侧枕区均可见短程,低波幅7 ~8 Hz 活动,左右两侧基本对称。间期脑电图显示较多广泛性低-高波幅棘波,棘慢波放电和双侧前头部低-高波幅棘波,棘慢波放电。脑电图监测中发现9 次癫痫发作,患者表现为愣神伴身体快速有节律地抖动,并且身体逐渐往下,同时可见眼睑节律性眨动。发作期脑电图为广泛性3 Hz 中-高波幅棘慢波放电(图1)。
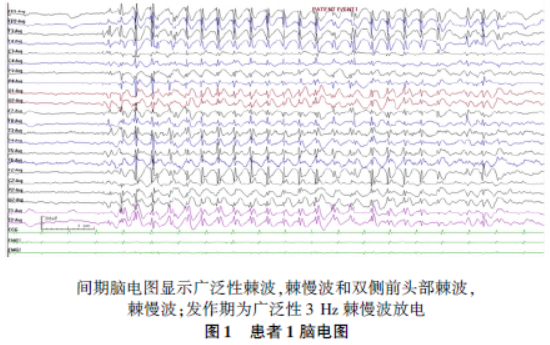
闪光刺激和过度换气诱发试验并未诱发癫痫发作。患儿脑部磁共振检查无异常改变。基因检测结果显示CHD2 基因(NM_001271. 3)c. 5068C> T(p. Arg1690Ter)杂合变异,该无义变异可以导致蛋白编码在第1 690 位精氨酸 翻译提前终止,从而产生长度为1 690个氨基酸的截短蛋白。该位点氨基酸在不同物种的比较,预测分析一致保守。在第1 690 位的精氨酸位置,翻译提前终止,从而产生长度为1 690 氨基酸的截短蛋白(图2)。
翻译提前终止,从而产生长度为1 690个氨基酸的截短蛋白。该位点氨基酸在不同物种的比较,预测分析一致保守。在第1 690 位的精氨酸位置,翻译提前终止,从而产生长度为1 690 氨基酸的截短蛋白(图2)。
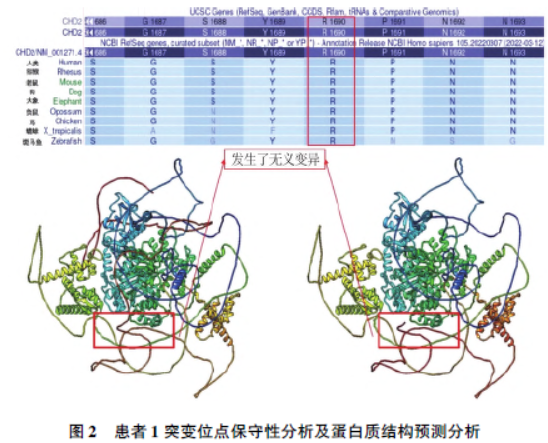
该变异位点为致病性变异(PVS1 + PS2 + PM2_Supporting)。超强致病证据(PVS1):该变异为无义变异,关联疾病为LOF 致病,其所在的转录本为有生物学意义的转录本,且不位于最后一个编码外显子或倒数第二个编码外显子最后50 bp,预测可能激活无义介导的mRNA 降解,从而影响该基因编码蛋白质的功能。强致病证据(PS2):经家系验证分析,该变异为新发变异,不排除父母生殖腺或体细胞存在嵌合可能。支持致病证据(PM2_Supporting):该变异在EXAC、gnomAD、千人基因组亚洲人群数据库的正常人群中为极低频变异或未见收录;人类基因突变数据库(The Human Gene Mutation Database,HGMD)未见该位点的相关性报道。
2. 2 患者2
脑电图结果为双侧枕区8 ~9 Hz ɑ 节律,间歇期为睡眠期广泛性低-高波幅多量棘波、多棘波、棘慢波/ 尖慢波、多棘慢波散发;左侧额区、中央区低-中波幅少量棘波、棘慢波/ 尖慢波散发。监测到数十次发作,患者表现为愣神伴少次身体抖动。发作期脑电图为广泛性2. 5 ~ 3 Hz 中-高波幅棘慢波放电(图3)。
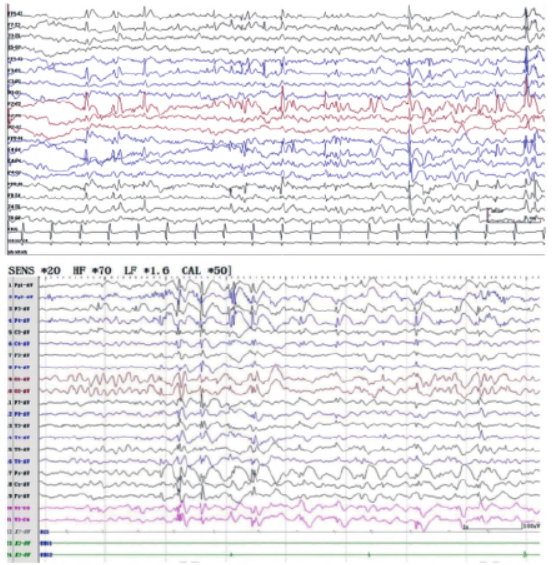
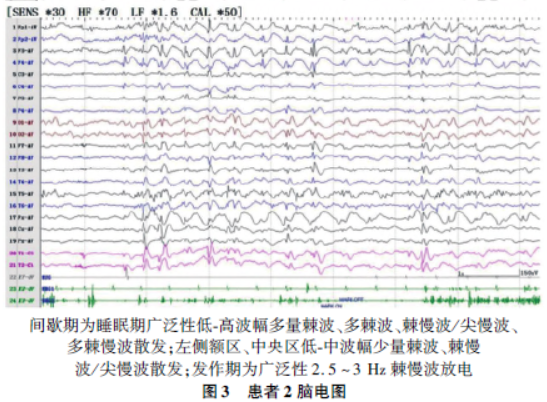
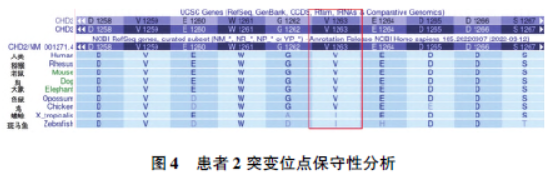
闪光刺激和过度换气诱发试验并未诱发癫痫发作。患者脑部磁共振检查无异常改变。基因结果为CHD2 基因c. 3787del G(p. Val1263Trpfs∗21)移码变异,该移码变异可以导致蛋白编码在第1 263 位由缬氨酸变为酪氨酸并发生移码,并在移码后的第21 个氨基酸处终止。该位点氨基酸在不同物种的比较,预测分析一致保守(图4)。
该位点为移码突变,结构图因终止翻译导致构象变化明显,因此蛋白构图就不具体呈现了。该变异位点为致病性变异(PVS1 + PS2 + PM2)。超强致病证据(PVS1):该变异为移码变异,此LOF 变异导致基因功能可能丧失,影响该基因编码蛋白质的功能。强致病证据(PS2):经家系验证分析,该变异为新发变异,不排除父母生殖腺或体细胞存在嵌合可能。中等致病证据( PM2): 该变异在EXAC、gnomAD、千人基因组亚洲人群数据库的正常人群中未见收录。
来源:贺晶,张冰清,王海祥,等.两例CHD2基因突变癫痫性脑病病例报道[J].临床神经外科杂志,2025,22(03):348-351.
