
青少年卵巢纤维瘤伴CA125升高和Meigs综合征一例
作者:王思瑶,胡晓红,令菲菲,刘畅 等,兰州大学第一临床医学院,兰州大学第一医院妇产科,甘肃省妇科肿瘤
等,兰州大学第一临床医学院,兰州大学第一医院妇产科,甘肃省妇科肿瘤 重点实验室
重点实验室
1病例报告
患者女,18岁,因腹胀伴下腹膨隆2个月余,于2023年8月22日就诊于兰州大学第一医院妇科。患者平素月经规律,12岁月经初潮,经期5 d,月经周期28~32 d,末次月经2023年7月28日,月经量中,色暗红,偶有痛经、血块史,无异常阴道出血史。患者2023年8月17日因腹胀就诊于当地医院,行盆腔增强磁共振成像 (magnetic resonance imaging,MRI)示:直肠子宫陷凹巨大占位性病变,腹盆腔大量积液,结合增强扫描,考虑直肠子宫陷凹子宫内膜样腺癌,直肠子宫陷凹见大小约11.3 cm×10.6 cm×7.9 cm的囊实性等长T1、等长T2信号灶,界限清楚,短反转时间反转恢复序列(short TIinversion recovery sequence,STIR序列)呈稍高信号,其内见多发斑片状长T1、长T2信号,STIR序列呈低信号,占位效应明显,子宫、直肠受压,动态增强扫描示肿块呈显著均匀增强,内囊性部分未见强化。CA125为1 168.00 U/mL(0~35 U/mL),血红蛋白
(magnetic resonance imaging,MRI)示:直肠子宫陷凹巨大占位性病变,腹盆腔大量积液,结合增强扫描,考虑直肠子宫陷凹子宫内膜样腺癌,直肠子宫陷凹见大小约11.3 cm×10.6 cm×7.9 cm的囊实性等长T1、等长T2信号灶,界限清楚,短反转时间反转恢复序列(short TIinversion recovery sequence,STIR序列)呈稍高信号,其内见多发斑片状长T1、长T2信号,STIR序列呈低信号,占位效应明显,子宫、直肠受压,动态增强扫描示肿块呈显著均匀增强,内囊性部分未见强化。CA125为1 168.00 U/mL(0~35 U/mL),血红蛋白 (hemoglobin,Hb)107 g/L(115~150 g/L),血小板(platelet,PLT)673×109/L(125×10 9/L~350×10 9/L)。为求进一步诊治患者就诊于我院,入院初步诊断:盆腔肿物性质待查;腹腔积液;盆腔积液;轻度贫血
(hemoglobin,Hb)107 g/L(115~150 g/L),血小板(platelet,PLT)673×109/L(125×10 9/L~350×10 9/L)。为求进一步诊治患者就诊于我院,入院初步诊断:盆腔肿物性质待查;腹腔积液;盆腔积液;轻度贫血 。患者自诉一般状况可,精神可,食欲欠佳,睡眠可,大小便正常,体质量无明显改变。
。患者自诉一般状况可,精神可,食欲欠佳,睡眠可,大小便正常,体质量无明显改变。
入院当日妇科检查 :外阴发育正常,肛诊可触及直肠前方肿物,黏膜光滑,质硬,界清,活动度欠佳,压迫直肠,子宫及双侧附件触诊不清。查体:体温36.9℃,脉搏
:外阴发育正常,肛诊可触及直肠前方肿物,黏膜光滑,质硬,界清,活动度欠佳,压迫直肠,子宫及双侧附件触诊不清。查体:体温36.9℃,脉搏 146次/min,呼吸20次/min,血压127/88 mmHg(1 mmHg=0.133 kPa)。身高170 cm,体质量40 kg。血常规
146次/min,呼吸20次/min,血压127/88 mmHg(1 mmHg=0.133 kPa)。身高170 cm,体质量40 kg。血常规 :Hb 101 g/L,PLT 698×109/L,CA125为1 075.00 U/mL,HE4为88.70 pmol/L(29.25~68.5pmol/L)。术前凝血功能检查示:凝血酶原时间14.1 s(9.4~12.5 s),凝血酶原活动度68%(75%~157%),血浆凝血酶原时间比值1.28(0.85~1.14),国际标准化比值1.29(0.86~1.13),纤维蛋白原9.02 g/L(2.39~4.98 g/L),活化部分凝血活酶时间
:Hb 101 g/L,PLT 698×109/L,CA125为1 075.00 U/mL,HE4为88.70 pmol/L(29.25~68.5pmol/L)。术前凝血功能检查示:凝血酶原时间14.1 s(9.4~12.5 s),凝血酶原活动度68%(75%~157%),血浆凝血酶原时间比值1.28(0.85~1.14),国际标准化比值1.29(0.86~1.13),纤维蛋白原9.02 g/L(2.39~4.98 g/L),活化部分凝血活酶时间 37 s(25.4~38.4 s),凝血酶时间12.1 s(10.3~16.6 s),D-二聚体
37 s(25.4~38.4 s),凝血酶时间12.1 s(10.3~16.6 s),D-二聚体 19.31μg/mL(0~0.50μg/mL),纤维蛋白降解产物
19.31μg/mL(0~0.50μg/mL),纤维蛋白降解产物 (57.34μg/mL(0~2.01μg/mL)。腹部超声示:腹水
(57.34μg/mL(0~2.01μg/mL)。腹部超声示:腹水 (大量)(最大深度位于下腹部,约109 mm);右侧附件区混合回声区大小约115mm×77 mm;右侧附件区囊肿(大小约20 mm×17 mm的无回声区);子宫及左侧附件未见明显异常。全腹增强CT示:①双侧附件多发异常强化结节并直肠子宫陷凹巨大囊实性占位(增强后实性部分轻度渐进性强化);②腹盆腔大量积液。盆腔MRI示:①直肠子宫陷凹巨大囊实性占位(106 mm×86mm),考虑肿瘤性病变,与附件关系密切;②盆腔大量积液;③肿块周围及双侧髂血管旁多发小淋巴结显示;④双侧附件区囊性灶,考虑卵泡。针对患者血液高凝状态行静脉血栓栓塞症风险评分Caprini评分:高危,给予低分子肝素
(大量)(最大深度位于下腹部,约109 mm);右侧附件区混合回声区大小约115mm×77 mm;右侧附件区囊肿(大小约20 mm×17 mm的无回声区);子宫及左侧附件未见明显异常。全腹增强CT示:①双侧附件多发异常强化结节并直肠子宫陷凹巨大囊实性占位(增强后实性部分轻度渐进性强化);②腹盆腔大量积液。盆腔MRI示:①直肠子宫陷凹巨大囊实性占位(106 mm×86mm),考虑肿瘤性病变,与附件关系密切;②盆腔大量积液;③肿块周围及双侧髂血管旁多发小淋巴结显示;④双侧附件区囊性灶,考虑卵泡。针对患者血液高凝状态行静脉血栓栓塞症风险评分Caprini评分:高危,给予低分子肝素 钙4 100IU皮下注射。综合患者病史体征和辅助检查初步考虑卵巢恶性肿瘤,遂完善电子胃肠镜示慢性非萎缩性胃炎
钙4 100IU皮下注射。综合患者病史体征和辅助检查初步考虑卵巢恶性肿瘤,遂完善电子胃肠镜示慢性非萎缩性胃炎 。2023年8月29日于气管插管全身麻醉下行经腹右侧卵巢输卵管切除术+盆腔肿物切除术+大网膜活检+右侧结肠旁沟腹膜活检+双侧阔韧带后叶病灶切除+直肠前壁病灶切除+膀胱前壁病灶切除+盆腔粘连松解+腹腔引流。术中见:大量腹水,可见一大小约10 cm×8 cm质硬实性肿物,异形血管爬行于表面,探查肿物来源于右侧卵巢,肿物前壁与膀胱前壁粘连,后壁与直肠前壁粘连,右侧壁与右侧阔韧带前后叶粘连,左侧壁与左侧阔韧带后叶粘连,子宫压迫于肿物下方,形态正常,左侧附件未见明显异常。大网膜、肠管、肝脏、脾脏、腹壁、双侧膈肌及胃未见异常。术中冰冻病理示:(右侧卵巢及肿物)形态学考虑卵泡膜纤维瘤。术中切除多处肿物,术后病理检查
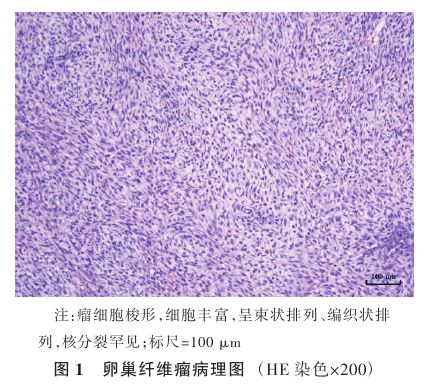
。2023年8月29日于气管插管全身麻醉下行经腹右侧卵巢输卵管切除术+盆腔肿物切除术+大网膜活检+右侧结肠旁沟腹膜活检+双侧阔韧带后叶病灶切除+直肠前壁病灶切除+膀胱前壁病灶切除+盆腔粘连松解+腹腔引流。术中见:大量腹水,可见一大小约10 cm×8 cm质硬实性肿物,异形血管爬行于表面,探查肿物来源于右侧卵巢,肿物前壁与膀胱前壁粘连,后壁与直肠前壁粘连,右侧壁与右侧阔韧带前后叶粘连,左侧壁与左侧阔韧带后叶粘连,子宫压迫于肿物下方,形态正常,左侧附件未见明显异常。大网膜、肠管、肝脏、脾脏、腹壁、双侧膈肌及胃未见异常。术中冰冻病理示:(右侧卵巢及肿物)形态学考虑卵泡膜纤维瘤。术中切除多处肿物,术后病理检查 示:镜下所见瘤细胞梭形,细胞丰富,呈束状排列、编织状排列,核分裂罕见,见图1。免疫组织化学检查示:s100(-),CD34(-),CD56(部分+),广谱细胞角蛋白(Cytokeratin Pan,CKpan)(-),钙视网膜蛋白(Calretinin,CR)(-),CK(灶+),结蛋白(Desmin)(部分+),上皮膜抗原(epithelial membrane antigen,EMA)(-),雌激素
示:镜下所见瘤细胞梭形,细胞丰富,呈束状排列、编织状排列,核分裂罕见,见图1。免疫组织化学检查示:s100(-),CD34(-),CD56(部分+),广谱细胞角蛋白(Cytokeratin Pan,CKpan)(-),钙视网膜蛋白(Calretinin,CR)(-),CK(灶+),结蛋白(Desmin)(部分+),上皮膜抗原(epithelial membrane antigen,EMA)(-),雌激素 受体(estrogen receptor,ER)(少量弱+),抑制素-α(Inhibin-α)(少量+),Ki-67增殖指数(5%),p53(-),孕激素
受体(estrogen receptor,ER)(少量弱+),抑制素-α(Inhibin-α)(少量+),Ki-67增殖指数(5%),p53(-),孕激素 受体(progesterone receptor,PR)(+),平滑肌肌动蛋白(smooth muscle actin,SMA)(部分+),波形蛋白(Vimentin)(+),肾母细胞瘤基因1(Wilms tumor gene 1,WT1)(弱+)。术后病理诊断:①(右侧卵巢)形态学及免疫组织化学结果支持卵巢纤维瘤,瘤组织巨大,请注意密切观察、随诊;②(右侧输卵管)输卵管上皮增生;③右侧子宫前壁肿物、左侧圆韧带肿物、阔韧带前叶组织、右侧阔韧带后叶结节、膀胱前壁组织和直肠前壁肿物可见瘤组织伴化脓性炎;④(大网膜)慢性炎伴化脓性炎,间皮增生;⑤右侧结肠旁沟腹膜活检见纤维脂肪组织,未见瘤组织;⑥直肠左侧系膜及阔韧带后叶可见瘤组织。
受体(progesterone receptor,PR)(+),平滑肌肌动蛋白(smooth muscle actin,SMA)(部分+),波形蛋白(Vimentin)(+),肾母细胞瘤基因1(Wilms tumor gene 1,WT1)(弱+)。术后病理诊断:①(右侧卵巢)形态学及免疫组织化学结果支持卵巢纤维瘤,瘤组织巨大,请注意密切观察、随诊;②(右侧输卵管)输卵管上皮增生;③右侧子宫前壁肿物、左侧圆韧带肿物、阔韧带前叶组织、右侧阔韧带后叶结节、膀胱前壁组织和直肠前壁肿物可见瘤组织伴化脓性炎;④(大网膜)慢性炎伴化脓性炎,间皮增生;⑤右侧结肠旁沟腹膜活检见纤维脂肪组织,未见瘤组织;⑥直肠左侧系膜及阔韧带后叶可见瘤组织。
术后第2天患者无明显诱因出现胸闷气短,2023年8月31日行胸部平扫CT示:①双肺多发磨玻璃斑片及条片,考虑感染,建议治疗后复查;②双侧胸腔积液 伴左肺下叶局限性膨胀不全;③腹腔积气。给予氧气吸入、抗感染等对症治疗,一般情况好转后于2023年9月4日出院。术后1个月随访,胸水及腹水消失,凝血功能逐渐好转。术后2年随访,患者无明显不适及异常。
伴左肺下叶局限性膨胀不全;③腹腔积气。给予氧气吸入、抗感染等对症治疗,一般情况好转后于2023年9月4日出院。术后1个月随访,胸水及腹水消失,凝血功能逐渐好转。术后2年随访,患者无明显不适及异常。
2讨论
2.1临床特征卵巢纤维瘤是一种常见的良性性索间质肿瘤,约占所有卵巢肿瘤的4%。该病多见于40~60岁女性,青少年较罕见,且多见于单侧卵巢,双侧少见,肿瘤的平均直径8 cm,约1/3的肿瘤直径小于3 cm[1] ,缺乏特异性的临床表现。1954年,Meigs正式建立了Meigs综合征的诊断标准:存在良性卵巢肿瘤,例如纤维瘤、甲状腺肿 、颗粒细胞瘤或Brenner瘤,伴有腹水、胸水,并且肿瘤切除后腹水和胸水消退[2] 。Meigs综合征仅发生在1%~2%的卵巢纤维瘤病例中。研究表明,Meigs综合征患者的血浆、胸水和腹水中有高浓度的血管内皮生长因子(vascular endothelial growth factor,VEGF)、白细胞介素-6(interleukin-6,IL-6)和成纤维细胞生长因子(fibroblast growth factor,FGF),可能是由于VEGF提高了毛细血管通透性,导致腹水和胸水。术后在切除盆腔肿块后,腹水和胸水消失,血浆中的VEGF、IL-6和FGF也有所下降[3] 。另有研究表明,胸水的产生可能是由于腹水通过网状淋巴管或网状裂孔进入胸腔而引起的;此外,盆腔肿瘤的生长可能导致淋巴管阻塞,从而阻碍腹腔和胸腔液体的正常回流,导致积液[4] 。在盆腔肿块切除后,肿瘤的压力消失,被压缩或堵塞的淋巴管恢复正常,从而清除腹水和胸水。本例患者患有卵巢纤维瘤,伴有大量腹水,并伴有CA125升高,术后出现胸水,术后1个月复查胸腹水明显消退,符合Meigs综合征的诊断。
、颗粒细胞瘤或Brenner瘤,伴有腹水、胸水,并且肿瘤切除后腹水和胸水消退[2] 。Meigs综合征仅发生在1%~2%的卵巢纤维瘤病例中。研究表明,Meigs综合征患者的血浆、胸水和腹水中有高浓度的血管内皮生长因子(vascular endothelial growth factor,VEGF)、白细胞介素-6(interleukin-6,IL-6)和成纤维细胞生长因子(fibroblast growth factor,FGF),可能是由于VEGF提高了毛细血管通透性,导致腹水和胸水。术后在切除盆腔肿块后,腹水和胸水消失,血浆中的VEGF、IL-6和FGF也有所下降[3] 。另有研究表明,胸水的产生可能是由于腹水通过网状淋巴管或网状裂孔进入胸腔而引起的;此外,盆腔肿瘤的生长可能导致淋巴管阻塞,从而阻碍腹腔和胸腔液体的正常回流,导致积液[4] 。在盆腔肿块切除后,肿瘤的压力消失,被压缩或堵塞的淋巴管恢复正常,从而清除腹水和胸水。本例患者患有卵巢纤维瘤,伴有大量腹水,并伴有CA125升高,术后出现胸水,术后1个月复查胸腹水明显消退,符合Meigs综合征的诊断。
2.2诊断及鉴别诊断
2.2.1病理学检查及影像学检查2020年世界卫生组织的组织学分类将卵巢的纤维性肿瘤分为卵泡膜纤维瘤、纤维瘤、交界性纤维瘤和纤维肉瘤 [5] 。其中卵巢纤维瘤的病理学特征表现为梭形纤维母细胞和胶原纤维束交织排列形成的界限清楚的良性肿瘤,细胞形态温和,每个高倍镜视野下核分裂象≤3个。本例的病理学检查界限清晰,无明显的核分裂象,符合卵巢纤维瘤。免疫组织化学检查对卵巢纤维瘤的诊断具有重要意义:Vimentin(+)证实其为间叶来源;EMA(-)、Inhibin-α(少量+)、Ki-67增殖指数(5%)和s100(-)支持卵巢纤维瘤诊断。卵巢纤维瘤患者初次就诊检查一般为超声,在超声成像中卵巢纤维瘤表现为边界明确的低回声肿块、后方回声衰减和极低的多普勒血流信号,但无特异性;CT主要表现为均匀的实性肿块并可见延迟强化,钙化少见,在肿瘤内部呈弥漫性分布[6] 。本例患者的CT有一定提示作用,但最终其病理学检查为诊断的金标准。
[5] 。其中卵巢纤维瘤的病理学特征表现为梭形纤维母细胞和胶原纤维束交织排列形成的界限清楚的良性肿瘤,细胞形态温和,每个高倍镜视野下核分裂象≤3个。本例的病理学检查界限清晰,无明显的核分裂象,符合卵巢纤维瘤。免疫组织化学检查对卵巢纤维瘤的诊断具有重要意义:Vimentin(+)证实其为间叶来源;EMA(-)、Inhibin-α(少量+)、Ki-67增殖指数(5%)和s100(-)支持卵巢纤维瘤诊断。卵巢纤维瘤患者初次就诊检查一般为超声,在超声成像中卵巢纤维瘤表现为边界明确的低回声肿块、后方回声衰减和极低的多普勒血流信号,但无特异性;CT主要表现为均匀的实性肿块并可见延迟强化,钙化少见,在肿瘤内部呈弥漫性分布[6] 。本例患者的CT有一定提示作用,但最终其病理学检查为诊断的金标准。
2.2.2肿瘤标志物 CA125是卵巢癌
CA125是卵巢癌 的首选肿瘤标志物,但其并非特异的诊断指标,在其他组织中也有表达,如输卵管上皮、子宫内膜和乳腺癌
的首选肿瘤标志物,但其并非特异的诊断指标,在其他组织中也有表达,如输卵管上皮、子宫内膜和乳腺癌 [7] ,临床上卵巢纤维瘤仅引起血清CA125升高相对少见,其合并Meigs综合征时多伴有CA125轻度升高,但水平超过1 000 U/mL的情况极其罕见[7-8] 。大多数学者认为Meigs综合征中CA125升高的原因为间皮细胞的表达[2] ,可能与肿瘤的物理刺激和炎症有关,而不是卵巢纤维瘤本身引起。本例CA125升高易被误诊为子宫内膜异位症
[7] ,临床上卵巢纤维瘤仅引起血清CA125升高相对少见,其合并Meigs综合征时多伴有CA125轻度升高,但水平超过1 000 U/mL的情况极其罕见[7-8] 。大多数学者认为Meigs综合征中CA125升高的原因为间皮细胞的表达[2] ,可能与肿瘤的物理刺激和炎症有关,而不是卵巢纤维瘤本身引起。本例CA125升高易被误诊为子宫内膜异位症 或卵巢恶性肿瘤[9] 。
或卵巢恶性肿瘤[9] 。
本例Meigs综合征患者同时伴有大量腹水、CA125增高和血小板增多 ,这三点间或许存在相关性。尚文雯等[10] 发现Meigs综合征患者血清CA125和HE4均升高,并与腹水量呈正相关。但有研究认为CA125水平与腹水间无相关性[7] 。在卵巢纤维瘤中出现血小板增多症鲜有报道,研究表明在卵巢恶性肿瘤中,腹水量与CA125水平及血小板增多均存在关联[11] ,此种血小板增多属于副肿瘤性血小板增多症(paraneoplastic thrombocytosis,PNT),其是一种继发性血小板增多症,其发生与多种细胞因子有关,其中包括血小板生成素(thrombopoietin,TPO)、IL-6、粒细胞集落刺激因子
,这三点间或许存在相关性。尚文雯等[10] 发现Meigs综合征患者血清CA125和HE4均升高,并与腹水量呈正相关。但有研究认为CA125水平与腹水间无相关性[7] 。在卵巢纤维瘤中出现血小板增多症鲜有报道,研究表明在卵巢恶性肿瘤中,腹水量与CA125水平及血小板增多均存在关联[11] ,此种血小板增多属于副肿瘤性血小板增多症(paraneoplastic thrombocytosis,PNT),其是一种继发性血小板增多症,其发生与多种细胞因子有关,其中包括血小板生成素(thrombopoietin,TPO)、IL-6、粒细胞集落刺激因子 (granulocyte colony stimulatingfactor,G-CSF)、粒细胞-巨噬细胞集落刺激因子(granulocyte macrophage colony stimulating factor, GM-CSF)和碱性成纤维细胞生长因子(basicfibroblast growth factor,bFGF)[ 12] ,PTN和肿瘤进展之间的潜在机制尚未完全阐明,但这提示肿瘤生长与血小板的产生和激活间可能存在相互作用。
(granulocyte colony stimulatingfactor,G-CSF)、粒细胞-巨噬细胞集落刺激因子(granulocyte macrophage colony stimulating factor, GM-CSF)和碱性成纤维细胞生长因子(basicfibroblast growth factor,bFGF)[ 12] ,PTN和肿瘤进展之间的潜在机制尚未完全阐明,但这提示肿瘤生长与血小板的产生和激活间可能存在相互作用。
HE4与CA125联合检测已成为早期检测卵巢恶性肿瘤的生物标志物,但是需注意在极少数Meigs综合征中也可见其同时升高[3,13] 。一项对9例Meigs综合征患者的回顾性研究发现,Meigs综合征患者的HE4水平高于卵巢纤维瘤组,但显著低于卵巢癌组[14] 。本例患者CA125和HE4水平均高于正常值,目前仅有3例病例报道HE4水平明显升高,同时CA125水平超过1 000 U/mL,这表明CA125水平与HE4水平之间可能存在相关性[3] ,并且HE4和CA125在肿物切除后快速下降,可提示卵巢纤维瘤区别于卵巢恶性肿瘤。
2.2.3鉴别诊断卵巢纤维瘤合并Meigs综合征主要与上皮性卵巢癌、卵巢纤维肉瘤及卵巢Brenner瘤相鉴别。①上皮性卵巢癌:其与Meigs综合征均可触及附件区实性肿块,晚期上皮性卵巢癌中常伴有胸腹水,血清CA125水平也可显著升高,但在其病理检查中,卵巢癌表现为高度异型的上皮样细胞形成复杂的恶性结构,并伴有浸润和破坏。②卵巢纤维肉瘤的细胞核异型明显,石蜡切片后每个高倍镜视野下细胞核分裂象≥4个,细胞恶性程度高,纤维瘤的Ki-67增殖指数通常很低,而纤维肉瘤显著增高,治疗后极易复发,病死率高。③卵巢Brenner瘤大多是一种卵巢良性实性肿瘤,极少数情况下,Brenner瘤也可伴有类似Meigs综合征的胸腹水,称为假性Meigs合征,其鉴别主要依赖病理诊断,Brenner瘤由巢状排列的上皮细胞和大量纤维间质构成,而纤维瘤由梭形的纤维细胞和胶原纤维束交织构成[15] 。
2.3治疗及预后
卵巢肿瘤切除术是治疗Meigs综合征的最佳治疗方案,肿瘤切除后胸水、腹水在数周内消失[16] 。年轻、有生育要求者,若为单侧肿瘤可行患侧卵巢肿瘤剥除术或行患侧附件切除术,若为双侧肿瘤应当积极行双侧卵巢肿瘤切除术或单侧附件切除术+对侧卵巢肿瘤剥除术[17] 或患侧附件切除术;对围绝经 期、已绝经或者怀疑有恶变倾向者,应行全子宫切除术+双侧附件切除术,术后无需化疗。本例患者有生育需求,行单侧附件切除+肿物切除术,术中送冰冻考虑纤维瘤,手术范围充足。
期、已绝经或者怀疑有恶变倾向者,应行全子宫切除术+双侧附件切除术,术后无需化疗。本例患者有生育需求,行单侧附件切除+肿物切除术,术中送冰冻考虑纤维瘤,手术范围充足。
卵巢纤维瘤患者多数预后良好。胸腔、腹腔积液多在肿瘤切除术后的数周自行消失,多数不会复发。有研究报道1例Meigs综合征患者术后10年随访期内未见复发[18] 。然而,在少数病例中,纤维瘤可以黏附到卵巢外周围组织,增加复发风险[19] 。本例患者术后病理提示多处瘤组织伴化脓性炎,经抗生素治疗后感染得到控制。鉴于其存在卵巢外粘连情况,故建议长期随访。
综上所述,卵巢纤维瘤CA125升高伴Meigs综合征罕见,患者就诊时一般无特异性的临床表现,多以腹部膨隆及腹痛就诊,治疗后总体预后好。对于不明原因胸水、腹水,甚至心包积液的盆腔肿物女性患者,可利用临床病史、病理组织学特征及免疫组织化学标志物行鉴别诊断。该病确诊需要依据病理活检,治疗以手术治疗为主,可根据患者情况选择不同的手术方式和范围。
参考文献略。
来源:王思瑶,胡晓红,令菲菲,等.青少年卵巢纤维瘤伴CA125升高和Meigs综合征一例[J].国际生殖健康/计划生育杂志,2025,44(06):471-474.
