
一例血友病A合并CYP21A2基因复合杂合变异患儿家系遗传学分析
作者:徐福蓉,陈元 康,康启超,唐联锐等,甘肃省妇幼保健院医学遗传中心,甘肃省出生缺陷与罕见病临床研究中心,胎儿医学中心
康,康启超,唐联锐等,甘肃省妇幼保健院医学遗传中心,甘肃省出生缺陷与罕见病临床研究中心,胎儿医学中心
血友病 A(hemophilia A,HA)是一种常见的X连锁隐性遗传性出血性疾病
A(hemophilia A,HA)是一种常见的X连锁隐性遗传性出血性疾病 ,在活产男胎中的发病率约为1/5 000[1] ,是由编码凝血因子Ⅷ(coagulationfactorⅧ,FⅧ)的基因变异引起血液中FⅧ活性降低而导致的凝血功能障碍性疾病,临床表现为皮肤黏膜、肌肉、关节、深部内脏组织的自发性出血或轻伤后出血[2-3] 。先天性肾上腺皮质增生症
,在活产男胎中的发病率约为1/5 000[1] ,是由编码凝血因子Ⅷ(coagulationfactorⅧ,FⅧ)的基因变异引起血液中FⅧ活性降低而导致的凝血功能障碍性疾病,临床表现为皮肤黏膜、肌肉、关节、深部内脏组织的自发性出血或轻伤后出血[2-3] 。先天性肾上腺皮质增生症 (congenital adrenalhyperplasia,CAH)主要是由肾上腺皮质激素合成过程中所需的不同酶类缺陷导致的一组常染色体
(congenital adrenalhyperplasia,CAH)主要是由肾上腺皮质激素合成过程中所需的不同酶类缺陷导致的一组常染色体 隐性遗传病,根据所缺乏的酶的种类不同可分为多种不同的亚型[4] ,其中最常见的类型是21-羟化酶缺乏症(21hydroxylase deficiency,21-OHD),约占所有CAH病例的95%以上[5] 。21-OHD发病率存在一定的种族和地区差异[6] 。现报告1例甘肃地区HA同时携带会导致21-OHD发生的CYP21A2基因复合杂合致病变异患儿的情况,通过对该患儿及其家系成员进行基因检测和遗传学分析,明确了患儿的致病原因,为该病的诊治提供参考。
隐性遗传病,根据所缺乏的酶的种类不同可分为多种不同的亚型[4] ,其中最常见的类型是21-羟化酶缺乏症(21hydroxylase deficiency,21-OHD),约占所有CAH病例的95%以上[5] 。21-OHD发病率存在一定的种族和地区差异[6] 。现报告1例甘肃地区HA同时携带会导致21-OHD发生的CYP21A2基因复合杂合致病变异患儿的情况,通过对该患儿及其家系成员进行基因检测和遗传学分析,明确了患儿的致病原因,为该病的诊治提供参考。
1病例报告
患儿男,4个月龄,因咳嗽 3周未好转以支气管肺炎
3周未好转以支气管肺炎 ,于2024年6月20日收入甘肃省妇幼保健院(我院)小儿呼吸科。患儿出生史及喂养史无特殊。患儿家属否认家族遗传病史,患儿父母否认近亲婚配,无疾病相关表型。患儿于入院前3周无明显诱因出现咳嗽,2~3声/次,白天咳嗽为主,少痰不易咳出;就诊于当地医院口服药物治疗未见好转,遂就诊于我院。入院当天常规凝血功能检查示:活化部分凝血活酶时间
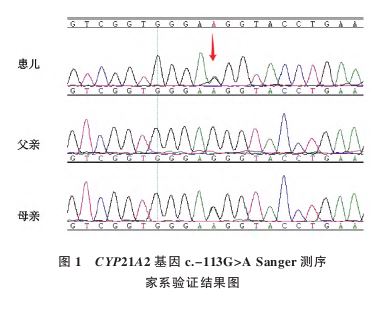
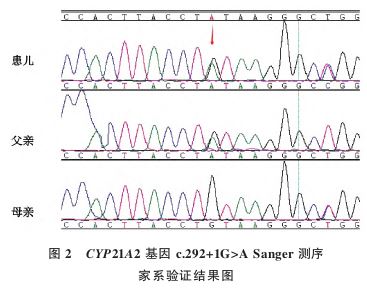
,于2024年6月20日收入甘肃省妇幼保健院(我院)小儿呼吸科。患儿出生史及喂养史无特殊。患儿家属否认家族遗传病史,患儿父母否认近亲婚配,无疾病相关表型。患儿于入院前3周无明显诱因出现咳嗽,2~3声/次,白天咳嗽为主,少痰不易咳出;就诊于当地医院口服药物治疗未见好转,遂就诊于我院。入院当天常规凝血功能检查示:活化部分凝血活酶时间 (activated partial thromboplastin time,APTT)138.2 s(升高,↑);凝血因子FⅡ71.1%(下降,↓);因凝血功能异常于2024年6月22日进一步行凝血因子活性检测,结果提示:凝血因子FⅦ43.1%(↓);凝血因子FⅧ<1%(↓);凝血因子FⅩ70.3%(↓);凝血因子FⅫ49.9%(↓)。浅表器官彩色多普勒超声检查示:左侧腕部皮下青紫处皮下及腕部掌侧深方低回声,考虑血肿。余无明显异常。于2024年6月24日采集患儿及其父母外周血2~3 mL,进行全外显子组测序(whole exome sequencing,WES),依据美国医学遗传学与基因组学学会(American College of Medical and Genomics,ACMG)指南[7]判读新变异的致病性,结果提示患儿在常染色体隐性遗传的CYP21A2基因有c.292+1G>A和c.-113G>A复合杂合变异,经Sanger测序家系验证结果提示患儿变异位点c.-113G>A来源于母亲(见图1),最终评级为可能致病性变异(PS3+PP4+PM3+PM2);变异位点c.292+1G>A来源于父亲,最终评级为致病性变异(PVS1_Moderate+PP1+PM3_Very Strong+PM2)(见图2)。
(activated partial thromboplastin time,APTT)138.2 s(升高,↑);凝血因子FⅡ71.1%(下降,↓);因凝血功能异常于2024年6月22日进一步行凝血因子活性检测,结果提示:凝血因子FⅦ43.1%(↓);凝血因子FⅧ<1%(↓);凝血因子FⅩ70.3%(↓);凝血因子FⅫ49.9%(↓)。浅表器官彩色多普勒超声检查示:左侧腕部皮下青紫处皮下及腕部掌侧深方低回声,考虑血肿。余无明显异常。于2024年6月24日采集患儿及其父母外周血2~3 mL,进行全外显子组测序(whole exome sequencing,WES),依据美国医学遗传学与基因组学学会(American College of Medical and Genomics,ACMG)指南[7]判读新变异的致病性,结果提示患儿在常染色体隐性遗传的CYP21A2基因有c.292+1G>A和c.-113G>A复合杂合变异,经Sanger测序家系验证结果提示患儿变异位点c.-113G>A来源于母亲(见图1),最终评级为可能致病性变异(PS3+PP4+PM3+PM2);变异位点c.292+1G>A来源于父亲,最终评级为致病性变异(PVS1_Moderate+PP1+PM3_Very Strong+PM2)(见图2)。
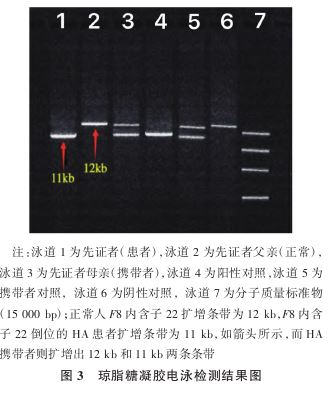
WES结果并不能解释患儿目前凝血功能异常的临床表型,结合患儿目前表型及相关辅助检查,高度可疑HA,利用长片段聚合酶链反应(long-range polymerase chain reaction,LR-PCR)对F8基因内含子22倒位情况进行检测(见图3),判读结果可知患儿为F8基因内含子22倒位患者,患儿母亲为携带者,患儿父亲正常。明确患儿基因诊断后,在治疗上予以人FⅧ替代治疗,头孢哌酮 钠舒巴坦
钠舒巴坦 钠抗感染、雾化等对症支持治疗后患儿病情好转,无发热
钠抗感染、雾化等对症支持治疗后患儿病情好转,无发热 ,咳嗽较前明显好转,左侧腕部皮下血肿较前明显消退,于2024年6月30日出院。门诊随诊至今,定期补充外源性FⅧ因子,病情尚稳定。
,咳嗽较前明显好转,左侧腕部皮下血肿较前明显消退,于2024年6月30日出院。门诊随诊至今,定期补充外源性FⅧ因子,病情尚稳定。
2讨论
2.1 HA的遗传机制及诊断经验HA是一种基因变异引起的FⅧ缺乏或功能低下导致的凝血障碍,是最常见的X连锁隐性遗传病之一。在血友病患者中,HA患者约占80%~85%。根据FⅧ活性不同可分为轻型(5%~40%)、中型(1%~5%)和重型(<1%)[8]。本例患儿FⅧ活性<1%,属重型,且临床已出现皮下血肿表现。F8基因是HA的致病基因,该基因位于染色体Xq28,全长约186 kb,共有26个外显子和25个内含子,编码2 351个氨基酸 。截至目前,人类基因突变数据库(The Human Gene Mutation Database,HGMD)中共报道致病性变异三千余种,主要以错义变异和无义变异为主。经LR-PCR检测发现本例患儿存在F8基因内含子22倒位,该变异主要是由于22号内含子内部存在一段9.5 kb的片段F8A,在F8基因上游400 kb及500 kb处还有两个9.5 kb大小的DNA片段,位于基因内的拷贝称为F8A1(int22h-1),两个基因外拷贝分别被命名为F8A2(int22h-2)和F8A3(int22h-3)。F8A3与F8A1转录方向相反,但F8A2与F8A1转录方向相同。在染色体复制过程中,由于两个同源拷贝F8A2或F8A3均可与F8A1发生同源重组而引起内含子22发生倒位,F8基因被分为两部分,导致转录提前终止,FⅧ无法正常产生引起重型HA,这是重型HA的常见分子机制。值得注意的是,WES未能检出该结构变异,凸显出该方法在大片段倒位检测中的局限性。通过本例情况可以看出,对临床高度疑似HA但WES未发现致病性点突变的患者,应积极联合LR-PCR等针对性技术进行结构变异检测,以避免漏诊。
。截至目前,人类基因突变数据库(The Human Gene Mutation Database,HGMD)中共报道致病性变异三千余种,主要以错义变异和无义变异为主。经LR-PCR检测发现本例患儿存在F8基因内含子22倒位,该变异主要是由于22号内含子内部存在一段9.5 kb的片段F8A,在F8基因上游400 kb及500 kb处还有两个9.5 kb大小的DNA片段,位于基因内的拷贝称为F8A1(int22h-1),两个基因外拷贝分别被命名为F8A2(int22h-2)和F8A3(int22h-3)。F8A3与F8A1转录方向相反,但F8A2与F8A1转录方向相同。在染色体复制过程中,由于两个同源拷贝F8A2或F8A3均可与F8A1发生同源重组而引起内含子22发生倒位,F8基因被分为两部分,导致转录提前终止,FⅧ无法正常产生引起重型HA,这是重型HA的常见分子机制。值得注意的是,WES未能检出该结构变异,凸显出该方法在大片段倒位检测中的局限性。通过本例情况可以看出,对临床高度疑似HA但WES未发现致病性点突变的患者,应积极联合LR-PCR等针对性技术进行结构变异检测,以避免漏诊。
2.2 CYP21A2基因复合杂合变异相关疾病及潜在表现本例患儿WES检出存在CYP21A2基因复合杂合变异:c.292+1G>A来源于父亲,为经典剪接位点致病性变异;c.-113G>A来源于母亲,位于启动子区,评级为可能致病,推测可能影响基因表达。虽然CYP21A2基因复合杂合变异与21-OHD型CAH的关联非绝对唯一,但具有极高的特异性和关联性。因为CYP21A2基因是编码21-羟化酶的关键基因,现有研究证实,CYP21A2基因的复合杂合变异是引发21-OHD的主要遗传学原因,且基因型与21-OHD的临床表型(典型/非典型)高度匹配,是21-OHD确诊的主要依据。21-羟化酶是肾上腺皮质激素合成的核心酶,该酶缺陷会导致皮质醇和盐皮质激素合成通路受阻,前体物质17-羟孕酮 (17-hydroxyprogesterone,17-OHP)不能转化为11-脱氧皮质醇(11deoxycortisol)而使得17-羟孕酮堆积,导致雄激素过度产生,表现出多毛、性早熟
(17-hydroxyprogesterone,17-OHP)不能转化为11-脱氧皮质醇(11deoxycortisol)而使得17-羟孕酮堆积,导致雄激素过度产生,表现出多毛、性早熟 以及骨龄提前等症状,女性出现阴蒂肥大、假两性畸形等临床症状[9-10] 。本例患儿目前虽然无典型CAH症状,可能与患儿目前年龄较小、属非经典型有关,但仍需长期随访监测17-OHP、电解质及生长发育指标,以便出现症状时
以及骨龄提前等症状,女性出现阴蒂肥大、假两性畸形等临床症状[9-10] 。本例患儿目前虽然无典型CAH症状,可能与患儿目前年龄较小、属非经典型有关,但仍需长期随访监测17-OHP、电解质及生长发育指标,以便出现症状时
及时干预[11] 。
2.3诊治策略及患者管理根据现有流行病学数据,HA在男性新生儿中发病率约为1/5 000,而CYP21A2基因变异相关联的疾病21-羟化酶缺乏症发病率约为1/15 000。两者均为罕见变异,共患概率理论上仅为1/75 000 000,目前尚未见文献报道。本研究揭示了这一罕见共存现象。对于重型HA临床上主要表现出的频繁的自发性出血和轻伤/手术/拔牙后的异常出血等症状,目前尚无法根治,只能外源性补充FⅧ进行替代治疗,并对症处理其他并发症。但外源性补充FⅧ可能会诱发机体产生FⅧ抑制物,导致替代治疗无效而更易出血[12] 。目前本例患儿针对CYP21A2基因变异相关联的21-OHD虽无临床症状,暂无需药物治疗,但需定期监测17-OHP和激素水平,防范肾上腺危象或高雄激素血症。需注意的是,若未来结合临床确诊为21-OHD,如使用糖皮质激素 治疗时需注意可能对HA产生的影响,可能增加出血风险[13] 。建议血液科与内分泌科共同制定治疗方案。本例患儿在门诊1年多的随访中未出现其他指标异常,定期补充外源性FⅧ病情平稳。遗传咨询方面,在明确了先证者的基因诊断后,未来可科学指导患儿母亲再生育;建议患者母亲再次妊娠
治疗时需注意可能对HA产生的影响,可能增加出血风险[13] 。建议血液科与内分泌科共同制定治疗方案。本例患儿在门诊1年多的随访中未出现其他指标异常,定期补充外源性FⅧ病情平稳。遗传咨询方面,在明确了先证者的基因诊断后,未来可科学指导患儿母亲再生育;建议患者母亲再次妊娠 时进行胚胎植入前遗传学检测(preimplantation genetictesting,PGT)助孕或有针对性地进行产前诊断,避免此类患儿再出生。
时进行胚胎植入前遗传学检测(preimplantation genetictesting,PGT)助孕或有针对性地进行产前诊断,避免此类患儿再出生。
综上,本文通过联合WES与LR-PCR技术,成功明确了1例HA患儿合并CYP21A2基因复合杂合致病性变异的罕见病例的基因诊断,为未来的遗传咨询和产前诊断提供了分子依据;同时强调了多项技术共用在复杂遗传病诊断中的重要性。提示在日常临床工作中,对不明原因多系统表型疾病应拓宽遗传检测策略,并注重多学科协作与长期随访,从而有利于患儿的预后。
参考文献略。
来源:徐福蓉,陈元康,康启超,等.一例血友病A合并CYP21A2基因复合杂合变异患儿家系遗传学分析[J].国际生殖健康/计划生育杂志,2025,44(06):468-470+480.
