
结肠镜发现的肠道子宫内膜异位症1例报告
作者:刘文静,莫文辉,徐选福等,上海理工大学附属市东医院消化内科
子宫内膜异位症 最早由Rokitansky于1860年描述,指子宫内膜组织在子宫腔外生长。该病在育龄妇女中的发病率约为10%~12%,其中5%~12%累及肠道[1-2] 。患者常表现为排便习惯改变(便秘
最早由Rokitansky于1860年描述,指子宫内膜组织在子宫腔外生长。该病在育龄妇女中的发病率约为10%~12%,其中5%~12%累及肠道[1-2] 。患者常表现为排便习惯改变(便秘 /腹泻
/腹泻 )、排便困难、腹痛、性交困难及不孕等症状[3],严重影响生活质量。由于临床表现和相关检查(包括内镜检查)缺乏特异性,结直肠子宫内膜异位症的诊断具有挑战性[2,4] 。本文报告1例结肠镜检查
)、排便困难、腹痛、性交困难及不孕等症状[3],严重影响生活质量。由于临床表现和相关检查(包括内镜检查)缺乏特异性,结直肠子宫内膜异位症的诊断具有挑战性[2,4] 。本文报告1例结肠镜检查 中发现的肠道子宫内膜异位症病例,并结合相关文献探讨其内镜表现及诊断策略。
中发现的肠道子宫内膜异位症病例,并结合相关文献探讨其内镜表现及诊断策略。
病例资料
患者为51岁女性,因间歇性下腹痛在外院行结肠镜检查,提示距肛门边缘约18 cm处见“息肉状”突起。患者计划接受内镜治疗,遂入住我院。患者月经初潮年龄为14岁,月经周期为4天,间隔30天,有痛经史,未系统诊治。患者曾怀孕1次,分娩 1次,6年前因子宫肌瘤
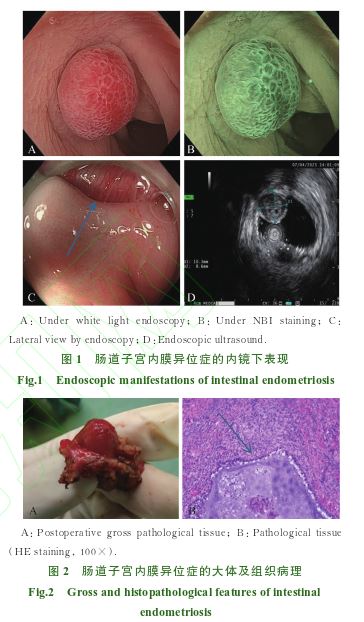
1次,6年前因子宫肌瘤 行全子宫切除术。入院后,患者腹部体格检查未见明显阳性体征。全腹CT扫描显示除子宫缺失外无明显异常。结肠镜检查显示(图1A,1B),直肠和乙状结肠交界处见一直径约1.5 cm的半球形隆起,表面结构呈规则脑回状,但侧面观显示病灶底部深深嵌入正常肠壁(图1C)。超声内镜检查
行全子宫切除术。入院后,患者腹部体格检查未见明显阳性体征。全腹CT扫描显示除子宫缺失外无明显异常。结肠镜检查显示(图1A,1B),直肠和乙状结肠交界处见一直径约1.5 cm的半球形隆起,表面结构呈规则脑回状,但侧面观显示病灶底部深深嵌入正常肠壁(图1C)。超声内镜检查 显示(图1D):第2、3层低回声带增厚,内部回声不均匀,向腔内突出,各层黏膜结构完整。黏膜下注射后,病灶抬举征阴性。结合上述表现,考虑结肠间质瘤或神经内分泌肿瘤可能性较大。经消化内科与外科医生讨论后,最终选择腹腔镜
显示(图1D):第2、3层低回声带增厚,内部回声不均匀,向腔内突出,各层黏膜结构完整。黏膜下注射后,病灶抬举征阴性。结合上述表现,考虑结肠间质瘤或神经内分泌肿瘤可能性较大。经消化内科与外科医生讨论后,最终选择腹腔镜 肠镜定位下的节段性肠切除术。术后病理(图2A,2B)显示:灰红色组织,大小为4.0 cm×2.8 cm×2 cm。免疫组化结果显示:ER(±)、PR(+)、CD10(+)、波形蛋白(+)、SMA(-)和CDX2(-),病理诊断为良性子宫内膜异位症病灶。患者术后5天出院,并在妇科医生建议下根据最新治疗观点[5]采用术后激素治疗方案:地诺孕素
肠镜定位下的节段性肠切除术。术后病理(图2A,2B)显示:灰红色组织,大小为4.0 cm×2.8 cm×2 cm。免疫组化结果显示:ER(±)、PR(+)、CD10(+)、波形蛋白(+)、SMA(-)和CDX2(-),病理诊断为良性子宫内膜异位症病灶。患者术后5天出院,并在妇科医生建议下根据最新治疗观点[5]采用术后激素治疗方案:地诺孕素 2 mg/d,持续6个月,抑制病灶复发。一项回顾性研究表明[6],与肠道子宫内膜以维持相关的并发症发生在早期(手术后第3个月)和晚期(手术后超过3个月)。我们在术后第2个月和第4个月进行随访,患者无腹痛等不适,结肠镜检查亦未见异常。
2 mg/d,持续6个月,抑制病灶复发。一项回顾性研究表明[6],与肠道子宫内膜以维持相关的并发症发生在早期(手术后第3个月)和晚期(手术后超过3个月)。我们在术后第2个月和第4个月进行随访,患者无腹痛等不适,结肠镜检查亦未见异常。
讨论
肠道子宫内膜异位症是一种罕见但具有挑战性的疾病,其诊断对内镜医生提出了较高的要求。随着内镜技术的不断发展,消化内镜在肠道子宫内膜异位症的早期诊断和治疗中发挥了越来越重要的作用。本病例通过结肠镜检查发现病灶,并结合超声内镜(endoscopic ultrasound,EUS)和黏膜下注射技术,最终明确了诊断。以下从消化内镜的角度,结合文献对肠道子宫内膜异位症的内镜表现、诊断策略及治疗选择进行深入分析。
肠道子宫内膜异位症的内镜表现多样,且缺乏特异性,这给内镜医生的诊断带来了挑战。既往文献报道中,病灶可表现为红酒色息肉[7]、偏心性肠壁增厚[8]或肠腔扭曲、狭窄等[9] 。Kim等[8]的研究指出,偏心性肠壁增厚是结直肠子宫内膜异位症最常见的内镜表现,而Milone等[7]则强调病灶表面颜色的变化可能是诊断的重要线索。国内学者[10] 提出了结肠子宫内膜异位症肠镜下表现的“长海分型”:肠壁僵硬、出血(瘀点/瘀斑/自发出血),黏膜起皱(轻微的、明显的或显著的),黏膜水肿 或增厚,黏膜颜色改变及糜烂,溃疡,狭窄这七大特征。本病例中,病灶在白光内镜下呈半球状,表面黏膜略发红,内镜窄带成像技术(narrow band imaging,NBI)染色及高清放大显示病灶表面血管呈规则网状,表面结构呈规则分支状,符合Pit pattern分型Ⅳ型及JNET分型2A型。这些表现与腺瘤性息肉相似,容易导致误诊。然而,本病例的一个关键发现是病灶侧面观显示其深深嵌入正常肠壁,且病灶侧黏膜有明显被牵拉的表现。这一特征提示病灶可能来源于黏膜深层,而非常见的结肠息肉
或增厚,黏膜颜色改变及糜烂,溃疡,狭窄这七大特征。本病例中,病灶在白光内镜下呈半球状,表面黏膜略发红,内镜窄带成像技术(narrow band imaging,NBI)染色及高清放大显示病灶表面血管呈规则网状,表面结构呈规则分支状,符合Pit pattern分型Ⅳ型及JNET分型2A型。这些表现与腺瘤性息肉相似,容易导致误诊。然而,本病例的一个关键发现是病灶侧面观显示其深深嵌入正常肠壁,且病灶侧黏膜有明显被牵拉的表现。这一特征提示病灶可能来源于黏膜深层,而非常见的结肠息肉 。此外,黏膜下注射后抬举征阴性,进一步证实了病灶的深层起源。这一发现提示,内镜医生在发现类似病灶时,应特别注意病灶的侧面观及黏膜下注射后的抬举征,以避免误诊。
。此外,黏膜下注射后抬举征阴性,进一步证实了病灶的深层起源。这一发现提示,内镜医生在发现类似病灶时,应特别注意病灶的侧面观及黏膜下注射后的抬举征,以避免误诊。
EUS对直肠乙状结肠子宫内膜异位症具有较高的阳性预测价值和高阴性预测价值,并具有良好的诊断准确性[11] 。既往有报道认为[9,12] ,结直肠的子宫内膜异位症症病变在超声内镜下大多是低回声和异质性病变,边缘不规则,涉及直肠壁的浆膜和固有肌层,呈纵向纺锤形,有时呈针状。James等[11] 将其描述为与固有肌层相邻的肿块的特征性低回声。本病例中,EUS显示病灶起源于第2、3层,内部回声不规则,以低回声为主,各层结构完整。
这一表现与既往报道相符 ,进一步支持了EUS在肠道子宫内膜异位症诊断中的价值。此外,EUS引导下细针穿刺活检(fine needle aspiration,FNA)可进一步提高诊断率[13] 。尽管本病例未进行FNA,但结合EUS表现及术后病理结果,进一步证实了EUS在该病诊断中的重要作用。随着内镜技术的进步,高清内镜、电子染色内镜[如NBI、蓝激光成像技术 (blue laser imaging,BLI)]及放大内镜等技术为肠道子宫内膜异位症的诊断提供了更多工具。本例中,通过NBI染色及高清弱放大,我们观察到病灶表面血管呈规则网状,表面结构呈规则分支状,这些表现与腺瘤性息肉相
似,但结合病灶的侧面观及EUS表现,最终排除了息肉的诊断。这一过程体现了多种内镜技术综合应用的重要性。此外,黏膜下注射技术在鉴别病灶起源中也发挥了关键作用。本例中,黏膜下注射后抬举征阴性,提示病灶来源于黏膜深层,这一发现为后续治疗方案的选择提供了重要依据。因此,内镜医生在遇到类似病灶时,应充分利用多种内镜技术,以提高诊断的准确性。肠道子宫内膜异位症的治疗原则是减少和消除病灶,改善患者生活质量。涉及肠道的子宫内膜异位症患者的主要治疗方法仍然是手术切除[14] 。本病例中,由于病灶深深嵌入肠壁,且EUS显示其累及第2、3层,最终选择了肠镜定位下的腹腔镜病灶切除术。尽管如此,内镜在治疗中的定位作用不可忽视。本病例中,肠镜精确定位病灶,为腹腔镜手术提供了重要参考,确保了病灶的完整切除。此外,对于部分表浅病灶,内镜下切除术可能是一种可行的选择。未来研究应进一步探讨内镜治疗在肠道子宫内膜异位症中的应用价值及安全性。尽管本病例为肠道子宫内膜异位症的诊断和治疗提供了有价值的参考,但仍有一些问题值得进一步探讨。例如,如何在内镜检查中更早地识别病灶的特征性表现?EUS引导下FNA在诊断中的具体应用价值如何?此外,对于不适合手术的患者,内镜下治疗的适应证和长期效果也需要更多研究支持。
本病例提示,对于周期性下腹痛的女性患者,应考虑肠道子宫内膜异位症的可能性,除了常规影像学检查外,肠镜检查尤为重要。通过综合应用高清内镜、电子染色内镜、超声内镜及黏膜下注射技术,内镜医生能够更准确地识别病灶的特征性表现,必要时可进行多学科讨论以避免误诊。未来研究应进一步优化内镜技术的应用,并探索内镜治疗在该病中的应用潜力。
作者贡献声明 刘文静,莫文辉 论文撰写和修订。徐选福 论文指导,构思和修订。
利益冲突声明 所有作者均声明不存在利益冲突。
参考文献略。
来源:刘文静,莫文辉,徐选福.结肠镜发现的肠道子宫内膜异位症1例报告[J/OL].复旦学报(医学版),1-4[2026-02-14].
