
胎儿多系统平滑肌功能障碍综合征的产前特征分析1例
作者:刘诗琪,杨 媚,唐 英,四川大学华西第二医院,医学遗传科产前诊断中心出生缺陷与相关妇儿疾病教育部重点实验室
1 病例报告
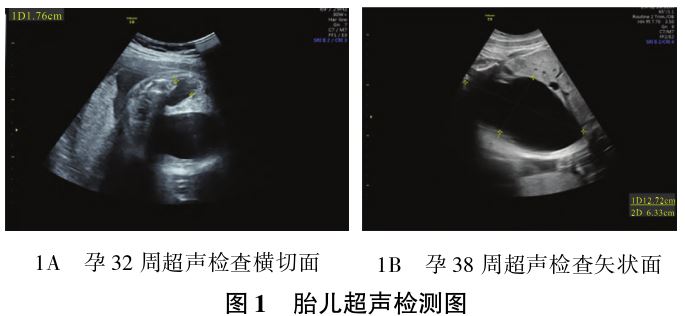
患者,28岁,G1P0,因孕38+1周,羊水进行性增加1+月,于2020年12月2日就诊于四川大学华西第二医院。孕早期于本院建卡产前检查,孕早期无阴道流血、流液,无毒物、射线接触史。孕早期唐氏筛查提示低风险,孕中期唐氏筛查:游离血β-人绒毛膜促性腺激素(β-hCG)轻度升高(2.65 U/L),遂行无创产前基因检测(NIPT)提示低风险,胎儿颈项透明层(NT)、胎儿系统产前超声、胎儿心脏超声检查未见明显异常。孕29周常规产前超声检查首次提示:胎儿双肾集合系统分离,胎儿膀胱大小约6.6 cm×3.7 cm×5.6 cm,反复动态观察未见明显缩小,羊水指数及羊水深度均在正常范围。孕32周复查胎儿泌尿系统针对性超声检查提示:胎儿膀胱大小8.9 cm×5.2 cm×5.4 cm,半小时后膀胱大小8.1 cm×4.3 cm×4.9cm,右肾集合系统分离0.70 cm,肾皮质最薄处厚约0.42 cm,左肾集合系统分离1.76 cm(见图1A),伴肾小盏扩张,肾皮质最薄处厚约0.16 cm。双侧输尿管未见明显扩张。羊水深度达8.8 cm,羊水指数达22.8 cm。于本院遗传科咨询建议行羊水穿刺,但患者因个人因素错过检测时机,患者及家属选择继续妊娠 并定期产检。孕晚期定期复查针对性彩超检查提示:胎儿膀胱呈进行性增大,患者羊水进行性增加。孕38周超声检查提示:膀胱大小达12.7 cm×6.3 cm×8.8 cm(见图1B)。患者无遗传病家族史,孕早期合并人乳头瘤病毒(HPV)11型感染,孕中期患外阴阴道假丝酵母菌病
并定期产检。孕晚期定期复查针对性彩超检查提示:胎儿膀胱呈进行性增大,患者羊水进行性增加。孕38周超声检查提示:膀胱大小达12.7 cm×6.3 cm×8.8 cm(见图1B)。患者无遗传病家族史,孕早期合并人乳头瘤病毒(HPV)11型感染,孕中期患外阴阴道假丝酵母菌病 ,孕期规范抗感染治疗。
,孕期规范抗感染治疗。
入院后经系统评估及术前准备,基于“羊水过多 、胎儿泌尿系统发育异常(膀胱进行性增大并伴双肾积水)”的医学指征,并结合患者及家属要求,于2020年12月3日实施剖宫产术娩出一女婴,体质量3530 g,身长47 cm,Apgar评分(1、5、10min)为9-10-10分。出生后2 h超声检查提示:双肾输尿管积水伴双侧输尿管上段扩张,膀胱过度充盈,上达剑突下1.0cm,两侧均达双侧锁骨中线外1.0 cm。患儿不能自主排出小便,安置尿管后可引流出小便。患儿于新生儿科出院诊断:泌尿道畸形、新生儿低血糖、新生儿肺炎
、胎儿泌尿系统发育异常(膀胱进行性增大并伴双肾积水)”的医学指征,并结合患者及家属要求,于2020年12月3日实施剖宫产术娩出一女婴,体质量3530 g,身长47 cm,Apgar评分(1、5、10min)为9-10-10分。出生后2 h超声检查提示:双肾输尿管积水伴双侧输尿管上段扩张,膀胱过度充盈,上达剑突下1.0cm,两侧均达双侧锁骨中线外1.0 cm。患儿不能自主排出小便,安置尿管后可引流出小便。患儿于新生儿科出院诊断:泌尿道畸形、新生儿低血糖、新生儿肺炎 、双眼多发大动脉瘤、新生儿病理性黄疸
、双眼多发大动脉瘤、新生儿病理性黄疸 、新生儿坏死性小肠结肠炎
、新生儿坏死性小肠结肠炎 、房间隔缺损、动脉导管未闭及卵圆孔未闭
、房间隔缺损、动脉导管未闭及卵圆孔未闭 。患儿出院后一直在本院进行儿保,随访发现,患儿在2021年1月于外院行临床全外显子组检测明确ACTA2c.536G>A(p.Arg179His)杂合变异,经美国医学遗传学与基因组学学会(ACMG)-分子病理学会(AMP)变异解释标准评估为致病性,未发现染色体
。患儿出院后一直在本院进行儿保,随访发现,患儿在2021年1月于外院行临床全外显子组检测明确ACTA2c.536G>A(p.Arg179His)杂合变异,经美国医学遗传学与基因组学学会(ACMG)-分子病理学会(AMP)变异解释标准评估为致病性,未发现染色体 数目异常以及致病性或可能致病性拷贝数变异。父母未行遗传学检查,且否认家族中有类似疾病或其他已知遗传病史。目前患儿已4岁,最新诊断包括复发性复杂型泌尿道感染、全面发育落后、右侧大脑前动脉A1段缺如、脑性瘫痪
数目异常以及致病性或可能致病性拷贝数变异。父母未行遗传学检查,且否认家族中有类似疾病或其他已知遗传病史。目前患儿已4岁,最新诊断包括复发性复杂型泌尿道感染、全面发育落后、右侧大脑前动脉A1段缺如、脑性瘫痪 等。
等。
2 讨 论
本病例结合产前持续存在的巨膀胱与上尿路扩张、出生后多系统受累表现,以及外院行临床全外显子检测发现的ACTA2c.536G>A(p.Arg179His)杂合致病性变异,可确认为ACTA2基因相关多系统平滑肌功能障碍综合征(MSMDS)。ACTA2基因编码的平滑肌-肌动蛋白(α-SMA)是血管及内脏平滑肌细胞收缩功能的核心结构蛋白,其变异可导致MSMDS,主要表现为心血管系统、神经系统等多器官平滑肌功能紊乱[1]。目前关于MSMDS的产后表型已逐步明确,但其产前特征仍缺乏系统性描述,且由于该综合征在胎儿期表现较为隐匿,传统超声检查易误诊为孤立性结构畸形导致遗传学检测延误[2]。本病例产前超声动态监测发现胎儿巨膀胱、进行性肾积水及羊水过多,通过分析ACTA2基因变异对胎儿平滑肌功能的早期影响,希望为产前诊断提供新视角。
2.1 产前特征分析 平滑肌功能障碍是MSMDS产前表型的核心机制。本例最早在孕29周发现膀胱扩张,病情随孕周呈进行性进展,至孕32周时,膀胱持续增大、上尿路扩张的同时,并发羊水过多。既往报道[2~8]的8例胎儿期病例中有7例提及胎儿期存在膀胱异常扩张的表现,最早可在孕13周[5]发现,多数发生于孕中晚期。这与本例观察一致,提示胎儿期巨膀胱可能是MSMDS的产前敏感线索。回顾既往文献既有羊水过多[6,9],也有羊水过少 [5]的报道,说明羊水异常在MSMDS中并不具有特异性,可能反映疾病在不同阶段的功能失代偿。值得注意的是,尽管47%的MSMDS患儿存在产后泌尿系统异常[10],但目前产前监测对泌尿系统的关注仍不足。基于本例胎儿产前巨膀胱的表现,需进行以下关键疾病的鉴别诊断:①后尿道瓣膜:动态观察未见膀胱壁增厚或“钥匙孔征”,下尿路超声检查亦不支持梗阻,可能性低;②染色体异常(如21-三体):NT正常且无其他结构畸形,且NIPT为低风险,可能性低;③神经源性膀胱
[5]的报道,说明羊水异常在MSMDS中并不具有特异性,可能反映疾病在不同阶段的功能失代偿。值得注意的是,尽管47%的MSMDS患儿存在产后泌尿系统异常[10],但目前产前监测对泌尿系统的关注仍不足。基于本例胎儿产前巨膀胱的表现,需进行以下关键疾病的鉴别诊断:①后尿道瓣膜:动态观察未见膀胱壁增厚或“钥匙孔征”,下尿路超声检查亦不支持梗阻,可能性低;②染色体异常(如21-三体):NT正常且无其他结构畸形,且NIPT为低风险,可能性低;③神经源性膀胱 :尚无脊柱裂或脊髓异常(如脊髓脊膜膨出)征象,可能性低;④Prune Belly综合征:尚无腹壁肌肉薄或缺如、双侧隐睾等特征,可能性低。
:尚无脊柱裂或脊髓异常(如脊髓脊膜膨出)征象,可能性低;④Prune Belly综合征:尚无腹壁肌肉薄或缺如、双侧隐睾等特征,可能性低。
从机制看,膀胱扩张主要源于ACTA2变异导致的平滑肌功能紊乱,而非单纯机械性梗阻[2]。本例孕晚期出现的羊水过多,除了可能与胎儿尿量 变化相关,还可能与吞咽障碍有关。一方面,极度膨大的膀胱可造成胃肠道受压,影响胎儿吞咽与肠蠕动;另一方面,MSMDS的全身性平滑肌功能障碍可累及食管与肠道,导致致病性吞咽障碍,从而减少羊水再吸收。上述推断与羊水生成主要取决于胎尿产生与吞咽的吸收平衡的生理规律相符[11],但仍需更多功能学证据加以验证。
变化相关,还可能与吞咽障碍有关。一方面,极度膨大的膀胱可造成胃肠道受压,影响胎儿吞咽与肠蠕动;另一方面,MSMDS的全身性平滑肌功能障碍可累及食管与肠道,导致致病性吞咽障碍,从而减少羊水再吸收。上述推断与羊水生成主要取决于胎尿产生与吞咽的吸收平衡的生理规律相符[11],但仍需更多功能学证据加以验证。
ACTA2基因变异是驱动表型的关键变异,其通过破坏α-SMA的核定位与染色质重塑功能,导致平滑肌分化缺陷以及表型异常,进而引发全身性平滑肌功能障碍,其中精氨酸 179位点的错义变异(如p.Arg179His)与最严重的表型相关[9]。本例患儿检出的ACTA2c.536G>A(p.Arg179His)变异,结合专家遗传学评估与ACMG指南[12],综合文献与数据库证据:人类基因组变异数据库(ClinVar数据库)收录为Pathogenic,2-star;人类基因突变数据库(HGMD数据库)注释为致病变异(DM),相关文献36篇;一般人群数据库(gnomAD数据库)未收录;致病性预测评分(REVEL=0.855),判定该变异为致病性。既往研究显示该位点变异可导致新生儿期动脉导管未闭、主动脉瘤
179位点的错义变异(如p.Arg179His)与最严重的表型相关[9]。本例患儿检出的ACTA2c.536G>A(p.Arg179His)变异,结合专家遗传学评估与ACMG指南[12],综合文献与数据库证据:人类基因组变异数据库(ClinVar数据库)收录为Pathogenic,2-star;人类基因突变数据库(HGMD数据库)注释为致病变异(DM),相关文献36篇;一般人群数据库(gnomAD数据库)未收录;致病性预测评分(REVEL=0.855),判定该变异为致病性。既往研究显示该位点变异可导致新生儿期动脉导管未闭、主动脉瘤 、肺动脉高压
、肺动脉高压 、泌尿系统障碍等问题。虽父母未验证,但ACMG评级及新生儿期表型一致性支持其致病性。并且该位点变异多报道为新发变异[13],符合本例无家族史的特征。目前与MSMDS有关的9例产前病例中(含本例),有5例患儿为p.Arg179His变异合并产前泌尿系统异常,且常伴多系统受累[2,5,6,8]。这一现象提示该位点可能与胎儿期泌尿表型相关。
、泌尿系统障碍等问题。虽父母未验证,但ACMG评级及新生儿期表型一致性支持其致病性。并且该位点变异多报道为新发变异[13],符合本例无家族史的特征。目前与MSMDS有关的9例产前病例中(含本例),有5例患儿为p.Arg179His变异合并产前泌尿系统异常,且常伴多系统受累[2,5,6,8]。这一现象提示该位点可能与胎儿期泌尿表型相关。
本研究为单中心单病例报道,并依赖文献回顾进行横向对照,存在样本量有限与发表偏倚。此外,本例缺乏胎儿期的客观功能学证据,对推断机制的支撑力度有限。上述因素可能低估或高估了特定产前征象的敏感性与特异性,结论需在前瞻性、多中心研究中进一步检验。
2.2 临床诊断与管理启示 基于上述产前特征与病理机制分析,本团队建议,若发现满足以下两类情况的胎儿,应尽早将ACTA2基因纳入检测范围,以警惕MSMDS的多系统受累:①巨膀胱:孕早期正中矢状切面上的膀胱上下径≥7 cm,或孕中晚期膀胱增大且持续时间>40~45 min[11]未观察到排空。可伴或不伴肾盂分离、输尿管扩张及羊水异常。②已排除梗阻性病变:经系统评估排除后尿道瓣膜等机械性梗阻后,仍存在进行性膀胱扩张。
当患者家属进行相关遗传咨询时,应强调MSMDS可能造成的多系统进行性损害,并客观评估其对患儿未来生存质量及家庭医疗负担的影响。在此基础上应结合家庭意愿及伦理原则,共同探讨继续妊娠、产时干预或终止妊娠的可行性。对于产前疑诊胎儿,本团队建议组建多学科团队以制定围产期及出生后的个体化管理计划,例如在新生儿出生后即刻开展对膀胱功能、心血管状态及神经发育情况的系统评估。
综上所述,结合本例患儿与文献回顾,提出了ACTA2基因变异相关MSMDS的主要产前超声线索与管理要点。建议对所有未提示梗阻性病因,但存在胎儿膀胱及肾盂扩张的病例进行有针对性的超声评估,同时结合基因检测等辅助诊断以排除其他病因。希望将MSMDS的诊断窗口从新生儿期前移至胎儿期,有望通过早期干预改善患儿生存质量、减轻家庭与社会负担。
参考文献略。
来源:刘诗琪,杨媚,唐英.胎儿多系统平滑肌功能障碍综合征的产前特征分析1例[J].实用妇产科杂志,2026,42(01):87-88.
