
胚胎移植合并门静脉海绵样变伴血栓形成1例
作者:刘唐影,孙厚坦,孙 阳,刘金英等,西北民族大学医学部,中国人民解放军联勤保障部队第九四〇医院超声诊断科,中国人民解放军联勤保障部队第九四〇医院生殖中心
门静脉海绵样变(cavernous transformation of the portal vein,CTPV)是由于肝门内或肝门血管通路受阻,引起门静脉高压 (portal hypertension,PHT)后导致门静脉周围侧支循环而形成[1]。CTPV根据病因可分为原发性和继发性,儿童多为原发性,成人多属继发性。继发性CTPV多因门静脉血栓
(portal hypertension,PHT)后导致门静脉周围侧支循环而形成[1]。CTPV根据病因可分为原发性和继发性,儿童多为原发性,成人多属继发性。继发性CTPV多因门静脉血栓 (portal vein thrombosis,PVT)引起,患者常表现为腹痛、脾大
(portal vein thrombosis,PVT)引起,患者常表现为腹痛、脾大 、脾功能亢进
、脾功能亢进 、腹水
、腹水 、门静脉高压性胃病等。胚胎移植术后口服雌激素
、门静脉高压性胃病等。胚胎移植术后口服雌激素 和孕激素
和孕激素 会引起体内凝血亢进,促使PVT形成,进而导致继发性CTPV[2]。CTPV属于门静脉代偿性改变,临床表现往往无特殊症状,但超声检查表现具有特异性,常表现为门静脉周围出现蜂窝状血流,门静脉主干管腔狭窄。经中国人民解放军联勤保障部队第九四〇医院(我院)医学伦理委员会批准,本文回顾1例接受胚胎移植术后出现CTPV患者的诊疗,旨在为临床诊治及预防该病提供参考。
会引起体内凝血亢进,促使PVT形成,进而导致继发性CTPV[2]。CTPV属于门静脉代偿性改变,临床表现往往无特殊症状,但超声检查表现具有特异性,常表现为门静脉周围出现蜂窝状血流,门静脉主干管腔狭窄。经中国人民解放军联勤保障部队第九四〇医院(我院)医学伦理委员会批准,本文回顾1例接受胚胎移植术后出现CTPV患者的诊疗,旨在为临床诊治及预防该病提供参考。
1 病例资料
患者,女,37岁,身高170 cm,体重61 kg,体重指数 21.1 kg/m2,因“冷冻胚胎移植术后3周,上腹疼痛半个月,加重3 d”于2024年2月25日就诊于我院。2023年12月15日凝血功能:凝血酶原时间9.7 s、凝血酶时间17.9 s、活化部分凝血活酶时间
21.1 kg/m2,因“冷冻胚胎移植术后3周,上腹疼痛半个月,加重3 d”于2024年2月25日就诊于我院。2023年12月15日凝血功能:凝血酶原时间9.7 s、凝血酶时间17.9 s、活化部分凝血活酶时间 23.6 s、纤维蛋白原2.53 g/L。2024年2月3日,患者在我院采用拮抗剂促排卵方案,获卵数12颗,获胚数7颗,准备内膜方案采用激素替代周期,行冻融胚胎移植术后双胎妊娠
23.6 s、纤维蛋白原2.53 g/L。2024年2月3日,患者在我院采用拮抗剂促排卵方案,获卵数12颗,获胚数7颗,准备内膜方案采用激素替代周期,行冻融胚胎移植术后双胎妊娠 ,术后给予地屈孕酮片(30 mg/次,3次/d)、雌二醇
,术后给予地屈孕酮片(30 mg/次,3次/d)、雌二醇 片/雌二醇地屈孕酮片(40 mg/次,2次/d)、戊酸雌二醇片(2片/次,2次/d)及阿司匹林
片/雌二醇地屈孕酮片(40 mg/次,2次/d)、戊酸雌二醇片(2片/次,2次/d)及阿司匹林 肠溶片(75 mg/次,1次/d)对症治疗。患者入院前2周无明显诱因出现上腹部疼痛,以剑突下为甚,呈间断性,可忍受。入院前3 d剑突下疼痛加重,呈持续性,不可忍受,自服抑酸、保护胃黏膜药物,效果不佳。入院前2 h,患者剑突下持续性疼痛加重,伴恶心、纳差、乏力。既往有甲状腺功能减退
肠溶片(75 mg/次,1次/d)对症治疗。患者入院前2周无明显诱因出现上腹部疼痛,以剑突下为甚,呈间断性,可忍受。入院前3 d剑突下疼痛加重,呈持续性,不可忍受,自服抑酸、保护胃黏膜药物,效果不佳。入院前2 h,患者剑突下持续性疼痛加重,伴恶心、纳差、乏力。既往有甲状腺功能减退 症病史,G1P0,无吸烟饮酒史,无高血压
症病史,G1P0,无吸烟饮酒史,无高血压 、糖尿病
、糖尿病 、心脏病
、心脏病 史,否认肝炎
史,否认肝炎 、结核病史,无外科手术史,个人史、家族史无特殊。患者入院时阿司匹林已停药。入院查体:体温36.2℃,脉搏
、结核病史,无外科手术史,个人史、家族史无特殊。患者入院时阿司匹林已停药。入院查体:体温36.2℃,脉搏 70次/min,呼吸频率18次/min,血压110/78 mmHg(1 mmHg=0.133 kPa);神志清楚,精神差,急性病面容,皮肤巩膜无黄染,浅表淋巴结未触及肿大;心肺查体无特殊;腹微隆,腹壁静脉不明显,剑突下压痛,腹壁划痕征阳性,余无特殊。血常规
70次/min,呼吸频率18次/min,血压110/78 mmHg(1 mmHg=0.133 kPa);神志清楚,精神差,急性病面容,皮肤巩膜无黄染,浅表淋巴结未触及肿大;心肺查体无特殊;腹微隆,腹壁静脉不明显,剑突下压痛,腹壁划痕征阳性,余无特殊。血常规 :白细胞计数10.59×109/L,中性粒细胞百分比72.9%。血凝六项:纤维蛋白原降解产物45.20 μg/ml,D-二聚体
:白细胞计数10.59×109/L,中性粒细胞百分比72.9%。血凝六项:纤维蛋白原降解产物45.20 μg/ml,D-二聚体 13.04 mg/L。血生化:总胆汁酸24.3 μmol/L、白蛋白
13.04 mg/L。血生化:总胆汁酸24.3 μmol/L、白蛋白 37.3 g/L、丙氨酸
37.3 g/L、丙氨酸 氨基转移酶60 IU/L、天冬氨酸转氨酶23 IU/L、血清脂肪酶31 U/L、淀粉酶
氨基转移酶60 IU/L、天冬氨酸转氨酶23 IU/L、血清脂肪酶31 U/L、淀粉酶 59 IU/L;白介素-6(电化学发光法)11.2 pg/ml、降钙素
59 IU/L;白介素-6(电化学发光法)11.2 pg/ml、降钙素 原(电化学发光法)0.066 ng/ml。肿瘤标志物
原(电化学发光法)0.066 ng/ml。肿瘤标志物 :糖类抗原-125 440.6 U/ml、糖类抗原-199 54.3 U/ml。C反应蛋白、甲功、尿常规
:糖类抗原-125 440.6 U/ml、糖类抗原-199 54.3 U/ml。C反应蛋白、甲功、尿常规 、肌红蛋白
、肌红蛋白 、肌钙蛋白
、肌钙蛋白 、血尿
、血尿 淀粉酶、抗心磷脂抗体
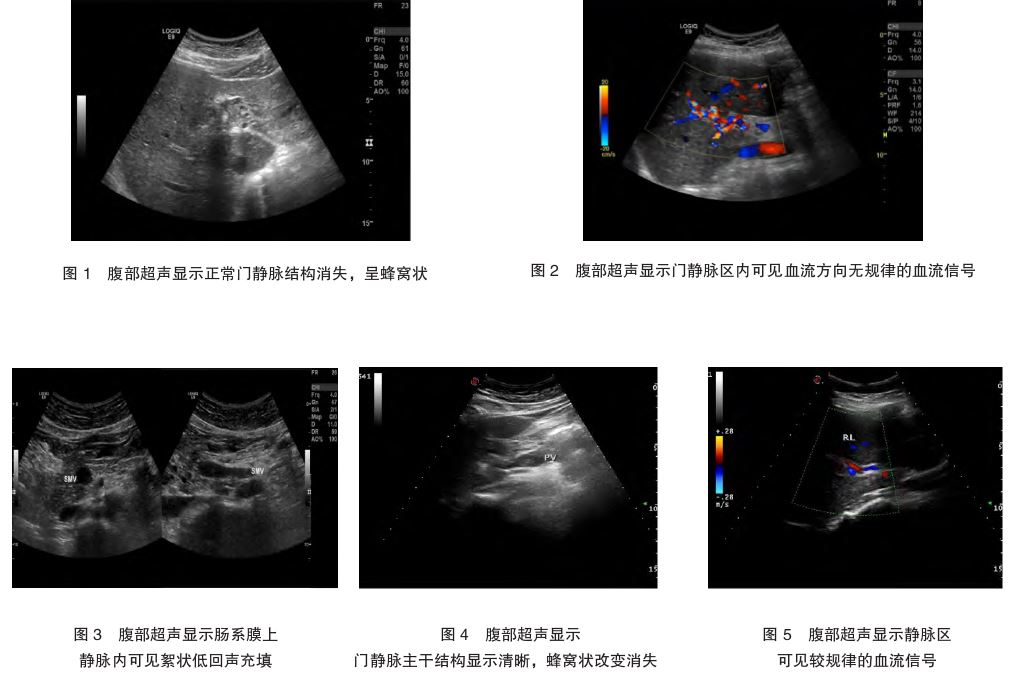
淀粉酶、抗心磷脂抗体 、抗核抗体、自身抗体谱、类风湿疾病等化验均阴性。腹部超声检查:CTPV(主干及右支),PVT形成(图1、2);胆囊结石
、抗核抗体、自身抗体谱、类风湿疾病等化验均阴性。腹部超声检查:CTPV(主干及右支),PVT形成(图1、2);胆囊结石 ,胆汁淤积
,胆汁淤积 ,肝外胆管显示不清;胰腺回声不均匀,考虑胰腺炎
,肝外胆管显示不清;胰腺回声不均匀,考虑胰腺炎 ,主胰管扩张;腹腔淋巴结肿大。
,主胰管扩张;腹腔淋巴结肿大。
入院后予以间苯三酚 解痉、补液、维持电解平衡等对症治疗后,患者剑突下疼痛症状缓解不明显;后采用氯化钠
解痉、补液、维持电解平衡等对症治疗后,患者剑突下疼痛症状缓解不明显;后采用氯化钠 100 ml+地塞米松
100 ml+地塞米松 5 mg静脉滴注,剑突下疼痛症状明显缓解。2024年2月28日复查腹部超声提示肠系膜上静脉栓子形成(图3),同时伴有中量腹腔积液。经多学科讨论后予以头孢曲松
5 mg静脉滴注,剑突下疼痛症状明显缓解。2024年2月28日复查腹部超声提示肠系膜上静脉栓子形成(图3),同时伴有中量腹腔积液。经多学科讨论后予以头孢曲松 钠抗感染、适量激素抗炎、抗凝治疗(低分子肝素
钠抗感染、适量激素抗炎、抗凝治疗(低分子肝素 )、黄体支持等对症治疗。2024年3月1日,患者D-二聚体进行性下降,抗凝治疗有效。因患者为早孕状态,低分子肝素皮下注射每12小时1次改为1次/d。2024年3月3日复查腹部超声提示门静脉工字部、肠系膜上静脉内径较前缩小。2024年3月4日患者出现剑突下疼痛间断发作,发作时疼痛评分1~4分,请心血管外科会诊,结合患者病史特点,患者目前处于高凝状态,建议低分子肝素注射改为每12小时1次,禁食水。2024年3月6日腹部超声提示门静脉主干、右支及矢状部内壁增厚,管腔内栓子形成,肠系膜上静脉血栓(近端)延伸至门静脉。开展病例讨论,建议先减胎(1个),考虑患者处于孕早期,继续抗凝治疗,必要时行刮宫术。2024年3月7日与患者及家属讲明病情后,患者及家属决定终止妊娠,接受人工流产
)、黄体支持等对症治疗。2024年3月1日,患者D-二聚体进行性下降,抗凝治疗有效。因患者为早孕状态,低分子肝素皮下注射每12小时1次改为1次/d。2024年3月3日复查腹部超声提示门静脉工字部、肠系膜上静脉内径较前缩小。2024年3月4日患者出现剑突下疼痛间断发作,发作时疼痛评分1~4分,请心血管外科会诊,结合患者病史特点,患者目前处于高凝状态,建议低分子肝素注射改为每12小时1次,禁食水。2024年3月6日腹部超声提示门静脉主干、右支及矢状部内壁增厚,管腔内栓子形成,肠系膜上静脉血栓(近端)延伸至门静脉。开展病例讨论,建议先减胎(1个),考虑患者处于孕早期,继续抗凝治疗,必要时行刮宫术。2024年3月7日与患者及家属讲明病情后,患者及家属决定终止妊娠,接受人工流产 抽吸刮宫术,手术顺利。2024年3月8日腹部增强CT提示门静脉主干及其分支、肠系膜上静脉及其属支、脾静脉内血栓广泛形成;CTPV。2024年3月10日,患者下腹痛,考虑术后反应但不排除PVT引起,予以缩宫素
抽吸刮宫术,手术顺利。2024年3月8日腹部增强CT提示门静脉主干及其分支、肠系膜上静脉及其属支、脾静脉内血栓广泛形成;CTPV。2024年3月10日,患者下腹痛,考虑术后反应但不排除PVT引起,予以缩宫素 、鲜益母草、头孢曲松+奥硝唑
、鲜益母草、头孢曲松+奥硝唑 抗感染、帕瑞昔布
抗感染、帕瑞昔布 注射液对症治疗。2024年3月15日,患者无腹痛等不适,停禁食水,予以利伐沙班片(15 mg/次,2次/d)抗凝治疗,同时加用贝前列素钠片(40 μg/次,3次/d)。2024年3月19日,患者自觉无特殊不适,准予出院,嘱定期复查。2024年4月9日复查腹部超声,PVT情况较前好转(图4、5),继续抗凝治疗。2025年1月22日,利伐沙班片减量至10 mg/次,1次/d。2025年2月24日改用低分子肝素注射液(5000 U/次,1次/d)桥接治疗。2025年5月26日,患者再次妊娠,低分子肝素注射液改量(3000 U/次,2次/d) 治疗至2025年9月1日。
注射液对症治疗。2024年3月15日,患者无腹痛等不适,停禁食水,予以利伐沙班片(15 mg/次,2次/d)抗凝治疗,同时加用贝前列素钠片(40 μg/次,3次/d)。2024年3月19日,患者自觉无特殊不适,准予出院,嘱定期复查。2024年4月9日复查腹部超声,PVT情况较前好转(图4、5),继续抗凝治疗。2025年1月22日,利伐沙班片减量至10 mg/次,1次/d。2025年2月24日改用低分子肝素注射液(5000 U/次,1次/d)桥接治疗。2025年5月26日,患者再次妊娠,低分子肝素注射液改量(3000 U/次,2次/d) 治疗至2025年9月1日。
2 讨论
CTPV是门静脉主干和/或其分支阻塞后形成侧支循环,主要由肝外门静脉阻塞引起[3]。肝外门静脉阻塞的常见原因是PVT,而妊娠状态属于PVT的重要发病因素,因此,本例患者胚胎移植术后检查发现CTPV伴PVT,可能与妊娠状态有关。有研究表明[4], 雌激素、孕激素在血管疾病的发生发展中有重要作用,体内雌激素水平升高可引起凝血途径中的部分凝血因子及纤维蛋白原数量增加,从而导致凝血功能亢进。孕激素可通过糖皮质激素 受体下调内皮一氧化氮
受体下调内皮一氧化氮 合酶来增加血小板聚集[5],此外,孕激素还可增强肝素酶促凝血活性[6]。因此,妊娠期机体血液的高凝状态容易导致PVT,进而增加CTPV的发生风险。
合酶来增加血小板聚集[5],此外,孕激素还可增强肝素酶促凝血活性[6]。因此,妊娠期机体血液的高凝状态容易导致PVT,进而增加CTPV的发生风险。
CTPV患者肝功能多正常,较少出现腹水、黄疸 症状,当门静脉压迫胆管时可出现黄疸。CTPV在二维超声中可表现为门静脉周围蜂窝状血管结构,门静脉管壁增厚、管腔变细或阻塞,管腔内出现中低回声。彩色多普勒观察门静脉及周围可见血流信号丰富、稀疏甚至无血流信号区域[7]。目前,门静脉血管造影是诊断CTPV的金标准,但其属于侵入性、有创性检查,不作为临床诊断首选。CT和磁共振分辨率较好,能更加清晰地显示CTPV的血管结构及有无血栓形成,三维动态增强磁共振血管造影
症状,当门静脉压迫胆管时可出现黄疸。CTPV在二维超声中可表现为门静脉周围蜂窝状血管结构,门静脉管壁增厚、管腔变细或阻塞,管腔内出现中低回声。彩色多普勒观察门静脉及周围可见血流信号丰富、稀疏甚至无血流信号区域[7]。目前,门静脉血管造影是诊断CTPV的金标准,但其属于侵入性、有创性检查,不作为临床诊断首选。CT和磁共振分辨率较好,能更加清晰地显示CTPV的血管结构及有无血栓形成,三维动态增强磁共振血管造影 对门脉系统的显示更加直观,对临床诊断CTPV及PHT的严重程度和治疗效果评估具有重要价值[8]。但CT对于妊娠期患者不适用,磁共振费用较高。本例患者因腹痛入院,首选超声检查,发现CTPV伴PVT,及时明确病因有助于为下一步临床治疗提供依据。
对门脉系统的显示更加直观,对临床诊断CTPV及PHT的严重程度和治疗效果评估具有重要价值[8]。但CT对于妊娠期患者不适用,磁共振费用较高。本例患者因腹痛入院,首选超声检查,发现CTPV伴PVT,及时明确病因有助于为下一步临床治疗提供依据。
临床治疗CTPV的原则是控制或预防静脉曲张导致的破裂出血,治疗方法可参考肝硬化 所致PHT。治疗方法分为药物治疗、内镜治疗、介入治疗和外科手术治疗。药物抗凝溶栓治疗常作为首选方法,采用抗凝药物低分子肝素联合华法林
所致PHT。治疗方法分为药物治疗、内镜治疗、介入治疗和外科手术治疗。药物抗凝溶栓治疗常作为首选方法,采用抗凝药物低分子肝素联合华法林 治疗急性PVT效果确切。防治肝硬化PHT食管胃静脉曲张出血的相关共识提出[9],药物治疗无效的患者应早期实施内镜或血管介入治疗。针对严重的CTPV患者、保守治疗及内镜介入治疗无效的患者,可选择外科手术治疗,包括断流术、分流术和肝移植
治疗急性PVT效果确切。防治肝硬化PHT食管胃静脉曲张出血的相关共识提出[9],药物治疗无效的患者应早期实施内镜或血管介入治疗。针对严重的CTPV患者、保守治疗及内镜介入治疗无效的患者,可选择外科手术治疗,包括断流术、分流术和肝移植 术[10]。本例患者处于妊娠期,母体对有创手术反应较大,故优先采用药物保守治疗。早期妊娠合并CTPV相对少见,国内外鲜有报道,容易漏诊,但该病可造成肝硬化甚至肝萎缩,肠系膜静脉血栓可引起肠梗阻
术[10]。本例患者处于妊娠期,母体对有创手术反应较大,故优先采用药物保守治疗。早期妊娠合并CTPV相对少见,国内外鲜有报道,容易漏诊,但该病可造成肝硬化甚至肝萎缩,肠系膜静脉血栓可引起肠梗阻 、肠坏死,甚至导致患者死亡[11]。妊娠期机体的变化会对肝脏产生影响[12],甚至会加重原有的肝病,临床应重视肝功能检查
、肠坏死,甚至导致患者死亡[11]。妊娠期机体的变化会对肝脏产生影响[12],甚至会加重原有的肝病,临床应重视肝功能检查 ,同时要预防胃底食管静脉曲张
,同时要预防胃底食管静脉曲张 及产后出血
及产后出血 等不良后果,及时纠正孕产妇贫血
等不良后果,及时纠正孕产妇贫血 ,排除抗磷脂综合征
,排除抗磷脂综合征 、系统性红斑狼疮
、系统性红斑狼疮 等特殊疾病[13],同时避免发生其他危及生命的症状[14-15],诊断明确后对症治疗,结合患者自身情况,必要时可行内镜介入或外科手术治疗,合理运用多学科资源,从而降低母体与胎儿的风险。
等特殊疾病[13],同时避免发生其他危及生命的症状[14-15],诊断明确后对症治疗,结合患者自身情况,必要时可行内镜介入或外科手术治疗,合理运用多学科资源,从而降低母体与胎儿的风险。
3 小结
胚胎移植术后并发CTPV较为少见,临床表现无特异性,虽然该病目前不属于妊娠禁忌证,但死亡率较高,仍需引起重视。CTPV在超声检查中具有特异性表现,有助于早期诊断,以及时采取抗凝治疗,降低死亡率。此外,临床针对此类孕妇还应监测凝血功能,定期复查腹部超声,必要时采取多学科会诊,结合孕妇具体情况调整治疗方案。
参考文献略。
来源:刘唐影,孙厚坦,孙阳,等.胚胎移植合并门静脉海绵样变伴血栓形成1例[J].妇儿健康导刊,2026,5(01):64-67.
