
宫颈中肾管腺癌伴股骨转移1例并文献复习
作者:王长英,曹平,湖北医药学院附属襄阳市第一人民医院、襄阳市第一人民医院肿瘤科
中肾管腺癌(MNA)是起源于胚胎时期残存的中肾管组织、好发于宫颈的一类罕见、高度恶性的肿瘤[1]。宫颈MNA临床表现多为阴道不规则出血,多呈息肉状外生性或内生浸润性生长。本病镜下结构多样,在活检标本有限时,如宫颈诊刮标本时易漏诊或误诊为宫颈腺癌、透明细胞癌等,多数病人通常在子宫颈锥切标本或子宫切除术标本中确诊。因该病临床罕见且易漏诊误诊,目前尚无规范化诊疗方案。本研究通过报告1例伴股骨转移的宫颈中肾腺癌的病例并复习文献,以丰富临床诊断和治疗该病的经验。本研究符合世界医学会《赫尔辛基宣言》相关要求,病人已签署知情同意书。
1 病例资料
女,63岁,因绝经 10年,阴道不规则少量出血1月余于2022年8月就诊湖北医药学院附属襄阳市第一人民医院,妇科检查
10年,阴道不规则少量出血1月余于2022年8月就诊湖北医药学院附属襄阳市第一人民医院,妇科检查 :阴道通畅;宫颈光滑;子宫萎缩变小,质硬,无压痛;附件未见明显异常。2022年8月14日经阴道超声
:阴道通畅;宫颈光滑;子宫萎缩变小,质硬,无压痛;附件未见明显异常。2022年8月14日经阴道超声 :宫腔内见一新生物,大小1.8 cm×1.2 cm×1.5 cm等回声、内可见血流信号,子宫内膜厚约0.1 cm。宫颈液基细胞学检查(TCT)及人乳头瘤病毒(HPV)检测未见明显异常。2022年8月30日全腹CT:宫腔内见斑片状异常信号影。既往史:2010年行左侧卵巢良性肿物切除术。
:宫腔内见一新生物,大小1.8 cm×1.2 cm×1.5 cm等回声、内可见血流信号,子宫内膜厚约0.1 cm。宫颈液基细胞学检查(TCT)及人乳头瘤病毒(HPV)检测未见明显异常。2022年8月30日全腹CT:宫腔内见斑片状异常信号影。既往史:2010年行左侧卵巢良性肿物切除术。
完善相关检查,排除手术禁忌后行腹腔镜 经腹全子宫+右侧附件+盆腔淋巴结切除术。2022年9月5日术后常规病理报告:子宫颈体交界处MNA,癌灶长径约0.6 cm,位于浅肌层(<1/2层);双侧宫旁及右附件均未见癌累及;未见明确脉管内癌栓及神经侵犯;双侧盆腔及髂总淋巴结共约30枚,未见癌累及。免疫组织化学染色:癌细胞配对框(Pax)8+、Pax2+、GATA结合蛋白3(GATA3)+、雄激素受体(AR)−、雌激素
经腹全子宫+右侧附件+盆腔淋巴结切除术。2022年9月5日术后常规病理报告:子宫颈体交界处MNA,癌灶长径约0.6 cm,位于浅肌层(<1/2层);双侧宫旁及右附件均未见癌累及;未见明确脉管内癌栓及神经侵犯;双侧盆腔及髂总淋巴结共约30枚,未见癌累及。免疫组织化学染色:癌细胞配对框(Pax)8+、Pax2+、GATA结合蛋白3(GATA3)+、雄激素受体(AR)−、雌激素 受体(ER)−、孕激素
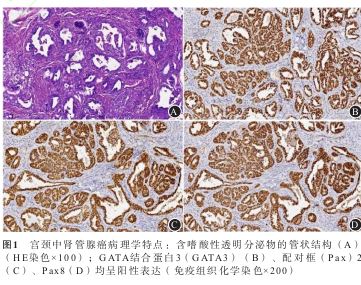
受体(ER)−、孕激素 受体(PR)−、波形蛋白(VIM)灶+、钙结合蛋白(CR)−、Wilms肿瘤基因(WT-1)−、P53+、P16−、Ki-67阳性率约40%(见图1A、B、C、D)。2022年10月19日右大腿磁共振成像
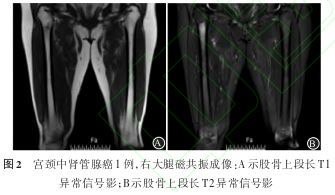
受体(PR)−、波形蛋白(VIM)灶+、钙结合蛋白(CR)−、Wilms肿瘤基因(WT-1)−、P53+、P16−、Ki-67阳性率约40%(见图1A、B、C、D)。2022年10月19日右大腿磁共振成像 (MRI):右侧股骨中上段异常信号,考虑为转移病灶(见图2A、B)。于2022年10月19日开始行紫杉醇
(MRI):右侧股骨中上段异常信号,考虑为转移病灶(见图2A、B)。于2022年10月19日开始行紫杉醇 联合卡铂
联合卡铂 (紫杉醇240 mg,第1天;卡铂350 mg,第1天)化疗1周期,病人因个人原因拒行后续术后辅助
(紫杉醇240 mg,第1天;卡铂350 mg,第1天)化疗1周期,病人因个人原因拒行后续术后辅助
放化疗,在本院定期复查随访。
2 结果
截至术后16个月,病人一般情况良好,病情稳定,未见局部复发和远处新发转移。
3 讨论
MNA是中肾残余组织发生恶性转化所致,常见发病部位为宫颈,也可发生于阴道和膀胱[2]。宫颈MNA来源于宫颈侧壁残留的中肾管,与HPV感染无关,是宫颈上皮性肿瘤的一种独特亚型,临床罕见,约占宫颈恶性肿瘤的1%。中位发病年龄为53.5岁,常见临床症状为阴道不规则出血,也有病人表现为月经过多、下腹痛。
宫颈MNA临床表现多样,病灶在CT或MRI上也无特异性表现,很难与宫颈鳞癌或腺癌相鉴别,诊断依赖病理组织形态、免疫组织化学和分子检测。(1)病理组织形态方面,镜下MNA结构多样,包括管样、腺管样、乳头状、网状及实体结构等。最常见的为腺管样结构,腺腔内可见均匀的嗜酸性物质[3]。(2)免疫组织化学方面,GATA3在MNA细胞中的阳性率高达92.3%,且多表现为弥漫强阳性或阳性。CD10的阳性率高达74.1%,主要定位于腔缘。Pax8呈弥漫强阳性。Pax2表现为弥漫性核染色。P16阴性可协助诊断该病,用于鉴别MNA与其他子宫颈腺癌。ER、PR阴性是MNA诊断中不可缺少的诊断依据。(3)分子检测方面:最常见的分子改变为Kirsten大鼠肉瘤 病毒癌基因同源物(KRAS)和Neuroblastoma大鼠肉瘤病毒癌基因同源物(NRAS)突变,可作为诊断依据,还有较少见的成纤维细胞生长因子受体2(FGFR2)、视网膜母细胞瘤
病毒癌基因同源物(KRAS)和Neuroblastoma大鼠肉瘤病毒癌基因同源物(NRAS)突变,可作为诊断依据,还有较少见的成纤维细胞生长因子受体2(FGFR2)、视网膜母细胞瘤 基因(RB1)、β-连环蛋白(CTNNB1)基因突变的报道[4-5],而在子宫内膜癌
基因(RB1)、β-连环蛋白(CTNNB1)基因突变的报道[4-5],而在子宫内膜癌 和其他类型的宫颈腺癌中常见的遗传突变——第10号染色体
和其他类型的宫颈腺癌中常见的遗传突变——第10号染色体 上缺失与张力
上缺失与张力 蛋白同源的磷酸酶(PTEN)、磷脂酰肌醇
蛋白同源的磷酸酶(PTEN)、磷脂酰肌醇 4,5-二磷酸3-激酶催化亚基α(PIK3CA)、TP53突变,在MNA病人中并不常见,因此,KRAS或NRAS突变结合PIK3CA、PTEN和TP53突变的缺失可用于支持中肾腺癌的诊断[6]。
4,5-二磷酸3-激酶催化亚基α(PIK3CA)、TP53突变,在MNA病人中并不常见,因此,KRAS或NRAS突变结合PIK3CA、PTEN和TP53突变的缺失可用于支持中肾腺癌的诊断[6]。
临床上还有一类疾病与MNA有相同的组织学特征,即中肾样腺癌(MLA),两者的区别是发生部位不同,MLA主要发生于子宫体和卵巢等,其周围无中肾管残余或增生组织[7]。目前尚无针对MNA特定的治疗方案,现多参照宫颈腺癌的指导方针进行管理。MNA的治疗方式取决于疾病的国际妇产科联盟(FIGO)分期。早期病人主要采用手术治疗。对于ⅠB3、ⅡA2期病人目前首选同步放化疗,也可选择新辅助化疗后再手术,新辅助化疗可缩小肿瘤体积,减轻周围浸润,提高局部手术切除率[8]。对于ⅡB~ⅣA期,首选同步放化疗,以单药顺铂 同步化疗。对于ⅣB期病人以系统性化疗为主,常用的化疗方案为紫衫类联合铂类。
同步化疗。对于ⅣB期病人以系统性化疗为主,常用的化疗方案为紫衫类联合铂类。
临床上也有抗血管生成靶向药物联合免疫药物在微卫星位点高度不稳定(MSI-H)的复发病人中治疗有效的报道。Devarashetty等[4]在2022年报道了1例老年宫颈中肾腺癌的病人二次进展后,行肺部转移灶组织二代测序(NGS)检测发现FGFR2p.S252W突变和MSI-H,给予仑伐替尼 联合帕博丽珠单抗治疗效果良好,从首次复发至2022年4月已随访66个月,目前疾病处于有效控制中且治疗耐受性好。本病发生KRAS突变的频率较高,包括KRAS G12C、G12V、G12D等位点。sotorasib为KRAS G12C抑制剂,其在伴KRAS G12C突变局部晚期或转移性非小细胞肺癌
联合帕博丽珠单抗治疗效果良好,从首次复发至2022年4月已随访66个月,目前疾病处于有效控制中且治疗耐受性好。本病发生KRAS突变的频率较高,包括KRAS G12C、G12V、G12D等位点。sotorasib为KRAS G12C抑制剂,其在伴KRAS G12C突变局部晚期或转移性非小细胞肺癌 中取得了显著疗效,中位缓解期为11.1个月,且安全性良好,那这些靶向药物在伴KRAS G12C突变的MNA中是否可取得相同的疗效,可以在以后的工作中做相关的临床研究。
中取得了显著疗效,中位缓解期为11.1个月,且安全性良好,那这些靶向药物在伴KRAS G12C突变的MNA中是否可取得相同的疗效,可以在以后的工作中做相关的临床研究。
MNA的预后尚可,5年总生存率达74%[9]。但MNA常呈侵袭性发展,易出现复发转移,FIGOⅠ期的MNA复发率为32%,明显高于宫颈腺癌的16%[10]。常见转移部位为肺和骨盆,股骨转移尚未有文献报道。
综上所述,MNA的治疗方案参考宫颈腺癌,治疗方式取决于疾病的分期,主要通过手术治疗,也包括化疗和放疗,关于抗血管靶向药物、免疫治疗的方式也有个案报道,且取得了一定的临床疗效。KRAS靶向药物在有突变的晚期病人中也可尝试,但仍需进一步的临床研究证实。
参考文献略 。
来源:王长英,曹平.宫颈中肾管腺癌伴股骨转移1例并文献复习[J].安徽医药,2026,30(3):618-620。
