
以髓外侵犯首发急性早幼粒细胞白血病误诊Ewings肉瘤1例报道
作者:熊博钰,王萌 萌,马镜云,戴卓文等,南京医科大学无锡医学中心 无锡市人民医院 南京医科大学附属无锡人民医院检验科
萌,马镜云,戴卓文等,南京医科大学无锡医学中心 无锡市人民医院 南京医科大学附属无锡人民医院检验科
急性早幼粒细胞白血病 (a c u t e promyelocytic leukemia,APL)是急性髓系白血病
(a c u t e promyelocytic leukemia,APL)是急性髓系白血病 (acute myeloid leukemia,AML)的一种特殊类型,多数患者存在特异性染色体
(acute myeloid leukemia,AML)的一种特殊类型,多数患者存在特异性染色体 易位 t(15;17)(q22;q12),形成PML-RARA融合基因,其蛋白产物导致细胞分化迟缓、凋亡不足,是APL主要的分子机制[1] 。APL患者具有侵袭性临床表现,易发生出血和栓塞,早期死亡率为9%~30%[2] 。有研究发现,全反式维甲酸(all-transretinoic acid,ATRA)可通过促进分化,从而大大提高APL患者的完全缓解率[3] 。具体来说,ATRA和三氧化二砷
易位 t(15;17)(q22;q12),形成PML-RARA融合基因,其蛋白产物导致细胞分化迟缓、凋亡不足,是APL主要的分子机制[1] 。APL患者具有侵袭性临床表现,易发生出血和栓塞,早期死亡率为9%~30%[2] 。有研究发现,全反式维甲酸(all-transretinoic acid,ATRA)可通过促进分化,从而大大提高APL患者的完全缓解率[3] 。具体来说,ATRA和三氧化二砷 (arsenic trioxide,ATO)联合治疗可将APL患者5年无病生存率提高至90%以上,接近治愈标准[4] 。ATO在提高缓解率和治愈率的同时,可降低化疗相关毒性[5] , 已被纳入APL的治疗方案。目前,APL已成为一种无需造血干细胞移植
(arsenic trioxide,ATO)联合治疗可将APL患者5年无病生存率提高至90%以上,接近治愈标准[4] 。ATO在提高缓解率和治愈率的同时,可降低化疗相关毒性[5] , 已被纳入APL的治疗方案。目前,APL已成为一种无需造血干细胞移植 即可基本治愈的白血病,早期诊断和治疗对疾病的预后具有积极意义。APL的初步诊断主要依靠流式细胞术和细胞形态学检查。对于形态多变的APL,如微颗粒型,其诊断主要依据免疫表型,尤其是髓过氧化物酶(myeloperoxidase,MPO)强阳性[6] 。本文报道1例罕见的MPO阴性APL病例,以提高临床对此类疾病细胞形态学特征的认识,减少误诊和漏诊。
即可基本治愈的白血病,早期诊断和治疗对疾病的预后具有积极意义。APL的初步诊断主要依靠流式细胞术和细胞形态学检查。对于形态多变的APL,如微颗粒型,其诊断主要依据免疫表型,尤其是髓过氧化物酶(myeloperoxidase,MPO)强阳性[6] 。本文报道1例罕见的MPO阴性APL病例,以提高临床对此类疾病细胞形态学特征的认识,减少误诊和漏诊。
1 病例资料
患者,女,43岁。2022年10月中旬于外院行胸椎肿物占位切除手术。术后病理示圆细胞恶性肿瘤(椎管肿瘤)。免疫组化示BCL-2(+)、BCL-6(+)、CD10(-)、CD20 (-)、CD23(-)、CD3(-)、CD30(-)、 CD5(-)、CD57(-)、CD99(+)、CKpan (-)、EMA(-)、Ki-67(约50%+)、LCA(-)、MPO(-)、NSE(-)、PLAP(-)、 Syn(-)、S100(-)、Vimentin(+)、WT (-)、MUM1(-)、CyclinD1(-)、Pax-5 (-)、CD79a(-)、SALL4(-)、C-myc (局灶+)。支持高级圆细胞恶性肿瘤,考虑Ewing肉瘤 ,建议行荧光原位杂交检测。术后予安罗替尼
,建议行荧光原位杂交检测。术后予安罗替尼 靶向治疗。2022年11月12日查血常规
靶向治疗。2022年11月12日查血常规 示白细胞计数3.2×109L-1、血红蛋白
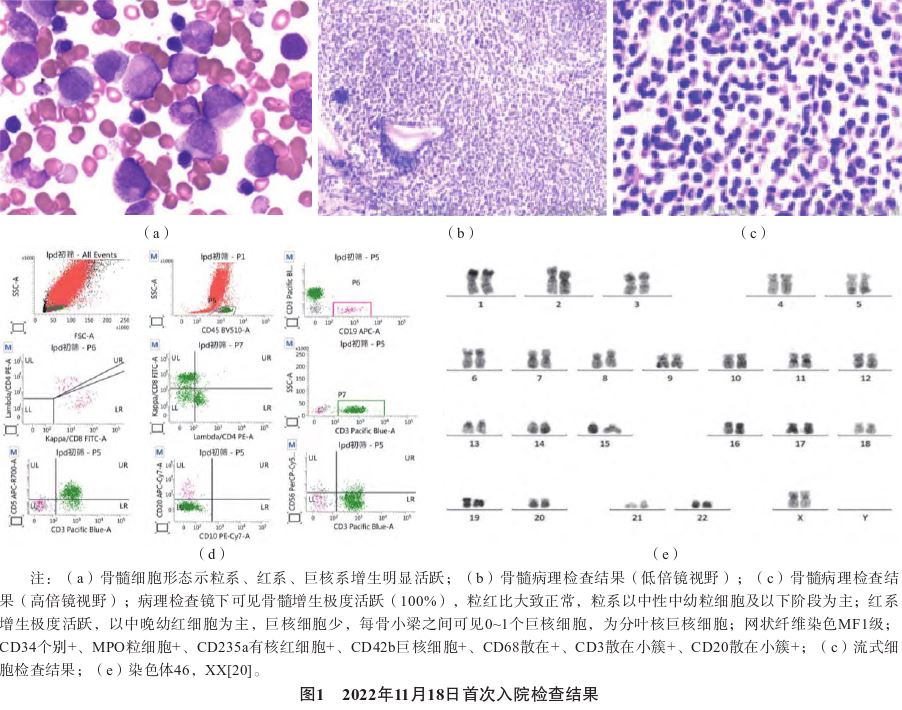
示白细胞计数3.2×109L-1、血红蛋白 77 g·L-1、血小板计数9.0×109L-1,生化未见明显异常,二次骨髓穿刺均干抽。遂至无锡市人民医院门诊就诊,2022年11月18日骨髓细胞形态示粒系、红系、巨核系增生明显活跃[图1(a)]。骨髓病理示MF1级,免疫组化示CD34(个别+),MPO(粒细胞+),CD235a(有核红+),CD42b(巨核细胞),CD68(散在+),CD3(散在小簇+),CD20(散在+);提示骨髓增生异常综合征
77 g·L-1、血小板计数9.0×109L-1,生化未见明显异常,二次骨髓穿刺均干抽。遂至无锡市人民医院门诊就诊,2022年11月18日骨髓细胞形态示粒系、红系、巨核系增生明显活跃[图1(a)]。骨髓病理示MF1级,免疫组化示CD34(个别+),MPO(粒细胞+),CD235a(有核红+),CD42b(巨核细胞),CD68(散在+),CD3(散在小簇+),CD20(散在+);提示骨髓增生异常综合征 待定[图1(b)、(c)]。流式细胞检测示淋巴细胞占6.3%,表达CD3(88.7%)、CD3+CD4 + (23.0%)、CD3+CD8 + (50.1%)、 CD3-CD56+(3.8%)、CD10(-)、CD19 +(4.0%),CD19+细胞表达Kappa 57.3%、Lambda 38.5%,提示淋巴细胞占6.3%,CD4/CD8比例倒置。细胞碎片+有核红细胞
待定[图1(b)、(c)]。流式细胞检测示淋巴细胞占6.3%,表达CD3(88.7%)、CD3+CD4 + (23.0%)、CD3+CD8 + (50.1%)、 CD3-CD56+(3.8%)、CD10(-)、CD19 +(4.0%),CD19+细胞表达Kappa 57.3%、Lambda 38.5%,提示淋巴细胞占6.3%,CD4/CD8比例倒置。细胞碎片+有核红细胞 占2.4%、粒细胞94.3%、CD13/CD11b分化模式异常,单核细胞0.9%、淋巴细胞1.5%,未见明显异常原始细胞[图1(d)]。染色体:46,XX[20][图1(e)]。后定期监测血常规示接近正常范围。
占2.4%、粒细胞94.3%、CD13/CD11b分化模式异常,单核细胞0.9%、淋巴细胞1.5%,未见明显异常原始细胞[图1(d)]。染色体:46,XX[20][图1(e)]。后定期监测血常规示接近正常范围。
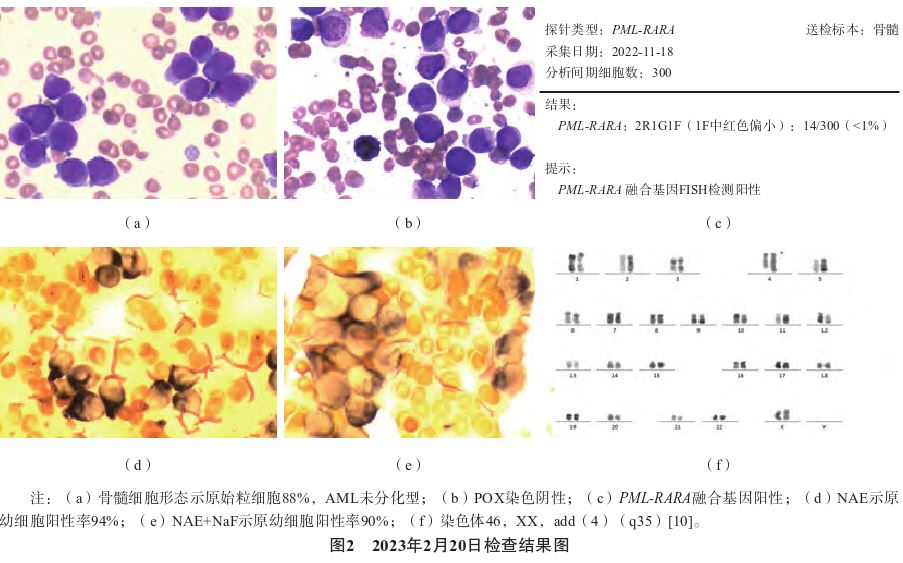
2023年2月初患者再次出现腰骶部疼痛,伴发热 (体温最高38.8 ℃),乏力,盗汗,牙龈出血,双上肢皮肤多发皮下瘀斑,遂至当地医院住院治疗,停用安罗替尼,予对症支持治疗后复查血常规(外院):白细胞计数24.35×109L-1,中性粒细胞16.97×109L-1,血红蛋白79 g·L-1,血小板计数18.00×109L-1,建议至上级医院就诊。2023年2月16日于无锡市人民医院查血常规:白细胞计数37.92×109L-1,中性粒细胞18.62×109L-1, 血红蛋白82 g·L-1,血小板计数20.00×109L-1。外周血细胞形态:白细胞总数增高,原始细胞占68%。2023年2月20日于无锡市人民医院检查骨髓细胞形态:原始粒细胞88%,AML未分化型。细胞化学组化:过氧化物酶(peroxidase,POX)染色示原始细胞阴性;醋酸萘酚酯酶染色(naphthol acetate esterase,NAE)示原幼细胞阳性率94%;NAE+氟化钠
(体温最高38.8 ℃),乏力,盗汗,牙龈出血,双上肢皮肤多发皮下瘀斑,遂至当地医院住院治疗,停用安罗替尼,予对症支持治疗后复查血常规(外院):白细胞计数24.35×109L-1,中性粒细胞16.97×109L-1,血红蛋白79 g·L-1,血小板计数18.00×109L-1,建议至上级医院就诊。2023年2月16日于无锡市人民医院查血常规:白细胞计数37.92×109L-1,中性粒细胞18.62×109L-1, 血红蛋白82 g·L-1,血小板计数20.00×109L-1。外周血细胞形态:白细胞总数增高,原始细胞占68%。2023年2月20日于无锡市人民医院检查骨髓细胞形态:原始粒细胞88%,AML未分化型。细胞化学组化:过氧化物酶(peroxidase,POX)染色示原始细胞阴性;醋酸萘酚酯酶染色(naphthol acetate esterase,NAE)示原幼细胞阳性率94%;NAE+氟化钠 抑制试验(Sodium Fluoride Inhibition Test,NAF)示原幼细胞阳性率90%。骨髓病理:增生极度活跃(>90%),提示AML。流式细胞检测示原始幼稚细胞占77.6%,白血病相关免疫表型(leukemia associated immunophenotype,LAIP)(CMPO+、CD117 + 、CD33+、CD13 + 、 CD81+、CD38 + 、CD58+、CD11c(dim)、CD123 +(部分)、CD9+,提示CD34- AML。PML-RARA荧光原位杂交检测示2R1G1F(1F中R信号偏小)、213/300(<1%),提示PML-RARA融合基因阳性。染色体46,XX,add(4)(q35)[10]。mRNA转录组测序检出PML:RARA(S型)融合基因,基因突变检测示可能具有临床意义的变异类型:NRAS基因突变,WT1基因突变。外院取椎管肿物,于无锡市人民医院病理科会诊:椎体后占位,免疫组化标记示CD20(-)、Pax-5(-)、CD3(-)、CD43(+)、LM02(+)、 L E F-1(-)、C D 1 9(-)、C D 4(灶+)、 CD8(-)、Lysozyme(+)、MPO(-)、 CD34(-)、TdT(散在+)CD68(弱+)、 CD163(-)、CD117(+),结合苏木精-伊红染色切片和外周血、骨髓实验室检查结果,明确诊断为APL(高危)。2月23日起予亚砷酸
抑制试验(Sodium Fluoride Inhibition Test,NAF)示原幼细胞阳性率90%。骨髓病理:增生极度活跃(>90%),提示AML。流式细胞检测示原始幼稚细胞占77.6%,白血病相关免疫表型(leukemia associated immunophenotype,LAIP)(CMPO+、CD117 + 、CD33+、CD13 + 、 CD81+、CD38 + 、CD58+、CD11c(dim)、CD123 +(部分)、CD9+,提示CD34- AML。PML-RARA荧光原位杂交检测示2R1G1F(1F中R信号偏小)、213/300(<1%),提示PML-RARA融合基因阳性。染色体46,XX,add(4)(q35)[10]。mRNA转录组测序检出PML:RARA(S型)融合基因,基因突变检测示可能具有临床意义的变异类型:NRAS基因突变,WT1基因突变。外院取椎管肿物,于无锡市人民医院病理科会诊:椎体后占位,免疫组化标记示CD20(-)、Pax-5(-)、CD3(-)、CD43(+)、LM02(+)、 L E F-1(-)、C D 1 9(-)、C D 4(灶+)、 CD8(-)、Lysozyme(+)、MPO(-)、 CD34(-)、TdT(散在+)CD68(弱+)、 CD163(-)、CD117(+),结合苏木精-伊红染色切片和外周血、骨髓实验室检查结果,明确诊断为APL(高危)。2月23日起予亚砷酸 10 mg qd+ATRA20 mg bid双诱导治疗。3月14日复查骨髓细胞形态:增生尚活跃,未见原始细胞;染色体正常核型;PML-RARA原始百分比(raw percentage,RAW%)1.3%。2023年3月17日复查头颅+胸椎MR3T(平扫+增强):两侧额颞骨及枕骨局部散在小片状强化灶,斜坡后缘小片状强化过,白血病所致骨改变?斜坡后缘强化灶较前 2月20日稍缩小。T7、T8术后改变,背部和腰部皮下软组织水肿
10 mg qd+ATRA20 mg bid双诱导治疗。3月14日复查骨髓细胞形态:增生尚活跃,未见原始细胞;染色体正常核型;PML-RARA原始百分比(raw percentage,RAW%)1.3%。2023年3月17日复查头颅+胸椎MR3T(平扫+增强):两侧额颞骨及枕骨局部散在小片状强化灶,斜坡后缘小片状强化过,白血病所致骨改变?斜坡后缘强化灶较前 2月20日稍缩小。T7、T8术后改变,背部和腰部皮下软组织水肿 伴强化。双侧胸腔积液
伴强化。双侧胸腔积液 。见图2。积极治疗后,2023年4月复诊,复查骨髓细胞形态:骨髓增生尚活跃,粒系增生活跃,各阶段细胞比例形态大致正常,白细胞计数正常,淋巴细胞比例正常,形态正常[图3(a)]。染色体:46,XX[20][图3(b)]。分子检测示PML-RARA融合基因检测阴性[图3(c)]。脱落细胞检查
。见图2。积极治疗后,2023年4月复诊,复查骨髓细胞形态:骨髓增生尚活跃,粒系增生活跃,各阶段细胞比例形态大致正常,白细胞计数正常,淋巴细胞比例正常,形态正常[图3(a)]。染色体:46,XX[20][图3(b)]。分子检测示PML-RARA融合基因检测阴性[图3(c)]。脱落细胞检查 示脑脊液未见有核细胞。患者症状明显改善,治疗时间轴见图4。
示脑脊液未见有核细胞。患者症状明显改善,治疗时间轴见图4。
2 讨论
本例患者曾在当地医院行椎管占位切除术,诊断为Ewing肉瘤,后因血象异常至无锡市人民医院就诊,第1次骨髓细胞形态检查发现原始粒细胞和异常早幼粒细胞,第2次骨髓细胞形态诊断M3,但异常早幼粒细胞POX阴性,患者是2种肿瘤还是1种肿瘤存疑,外院椎管切除病理标本送无锡市人民医院病理科会诊后诊断为髓系肉瘤,证明是M3椎管浸润。根据颗粒的大小,法国-美国-英国(FrenchAmerican-British,FAB)分型将APL分为M3a(粗颗粒型)、M3b(细颗粒型)、M3v(微颗粒型),其中M3v较少见,易与其他类型AML混淆,如急性单核细胞白血病(M5),急性单核细胞白血病POX染色通常为弱阳性或阴性。APL的典型特征是POX强阳性、非特异性酯酶强阳性且不被氟化钠抑制、碱性磷酸酶和糖原染色 阴性或弱阳性[2] 。然而,本例患者POX呈阴性。MO等[7] 发现了1例矩形晶体POX呈阴性的9岁APL女性患儿,其左肩和腹部疼痛10 d,且有浅表性淋巴结病变,没有任何明显的原因;骨髓免疫分型示89.6%的细胞异常,细胞遗传学分析示46,XX,t(15;17),荧光原位杂交技术(fluorescence in situ hybridization,FISH)检测示PML-RARA融合基因阳性。有研究发现,AML患者严重感染时中性粒细胞会出现POX缺乏[8] ,本例患者无明显感染,可排除严重感染导致POX阴性的可能。HEIBLIG等[9] 报道了1例53岁的患者因出血就诊,血涂片
阴性或弱阳性[2] 。然而,本例患者POX呈阴性。MO等[7] 发现了1例矩形晶体POX呈阴性的9岁APL女性患儿,其左肩和腹部疼痛10 d,且有浅表性淋巴结病变,没有任何明显的原因;骨髓免疫分型示89.6%的细胞异常,细胞遗传学分析示46,XX,t(15;17),荧光原位杂交技术(fluorescence in situ hybridization,FISH)检测示PML-RARA融合基因阳性。有研究发现,AML患者严重感染时中性粒细胞会出现POX缺乏[8] ,本例患者无明显感染,可排除严重感染导致POX阴性的可能。HEIBLIG等[9] 报道了1例53岁的患者因出血就诊,血涂片 姬姆萨法染色示中等大小的原始细胞,没有颗粒或Auer小体,原始细胞MPO阴性,FISH示原始细胞中t(15;17)易位的双重融合信号,单核苷酸多态性分析示17号染色体长臂的单亲二倍体,该患者原始细胞是纯合的MPO功能缺失突变。
姬姆萨法染色示中等大小的原始细胞,没有颗粒或Auer小体,原始细胞MPO阴性,FISH示原始细胞中t(15;17)易位的双重融合信号,单核苷酸多态性分析示17号染色体长臂的单亲二倍体,该患者原始细胞是纯合的MPO功能缺失突变。
ROMANI等[10] 报道了1例伴髓外广泛受累致死性压倒性小颗粒变异(M3v)病例,该病例为38岁男性,因呼吸困难 、肝脾肿大和发热入院,细胞化学显示与MPO反应强烈,而非特异性酯酶染色为阴性,标准细胞遗传学分析显示t(15;17),在第3天,临床迅速恶化,伴有发热、腹痛和严重的呼吸困难;电子计算机断层扫描显示患者存在巨大肝脾肿大、腹腔和胸腔积液以及胸部腺体肿大;白细胞计数增至93×109L-1,弥散性血管内凝血
、肝脾肿大和发热入院,细胞化学显示与MPO反应强烈,而非特异性酯酶染色为阴性,标准细胞遗传学分析显示t(15;17),在第3天,临床迅速恶化,伴有发热、腹痛和严重的呼吸困难;电子计算机断层扫描显示患者存在巨大肝脾肿大、腹腔和胸腔积液以及胸部腺体肿大;白细胞计数增至93×109L-1,弥散性血管内凝血 加重,肝肾功能衰竭(乳酸脱氢酶 9 650 U·L-1,转氨酶1 452 U·L-1和1 388 U·L-1,肌酐203.3 μmol·L-1);患者第4天死于多器官功能衰竭,尸检显示白血病累及肺、心、肾、肠道、骨髓、脾、肝和脑,证实为bcr3转录阳性。
加重,肝肾功能衰竭(乳酸脱氢酶 9 650 U·L-1,转氨酶1 452 U·L-1和1 388 U·L-1,肌酐203.3 μmol·L-1);患者第4天死于多器官功能衰竭,尸检显示白血病累及肺、心、肾、肠道、骨髓、脾、肝和脑,证实为bcr3转录阳性。
本例患者接受亚砷酸+ATRA双诱导治疗。目前报道的十余种变异型APL大部分对ATRA或亚砷酸不敏感,而对于不敏感的患者,往往采取类似AML治疗的联合化疗,经典型APL通常携带15号、17号染色体的相互平衡易位形成的PML-RARA融合基因,PML-RARA融合基因抑制维甲酸信号通路的转录活化,并导致PML核体的正常结构被破坏,使造血祖细胞分化受阻于早幼粒细胞阶段,且凋亡不足,这是M3发病的主要分子机制[11] 。ATO和ATRA都通过促进PMLRARA降解而起作用。当联合治疗时,这些药物可使APL持久缓解[12] 。ATO通过结合、抑制和降解Pin1来预防癌症,而 ATRA 也能结合和破坏Pin1,这2种药物联合使用可增加细胞对ATO的吸收,从而显著增强抗癌效果[13] 。PML核体位于核内染色质之间,直径为0.1~2.0 µm[14] 。早幼粒细胞白血病核小体是应激调节结构域,直接参与APL的根除,在多种细胞功能中起重要调节作用,包括肿瘤抑制、调节DNA损伤和应激反应、转录调节、诱导细胞凋亡和衰老。在APL中,早幼粒细胞白血病核小体的正常结构被破坏,而治疗APL的特异性药物ATO可以促使PML核体重新形成和聚集,癌蛋白PML-RARA抑制早幼粒细胞白血病核小体组装,并可导致成熟的白血病发生[15-18] 。
大多数情况下,APL的细胞学诊断较简单。血液疾病的诊疗应以细胞形态学为基础,再结合免疫学分析、细胞遗传学、骨髓活检等联合检测,可以提高诊断准确率,改善疗 效[19] 。虽然APL的免疫表型可能会出现多种变化,但MPO阳性是不变的,当1例急性白血病 患者MPO阴性时,APL的可能性较低[20] 。因此,POX阴性不一定可以排除APL,需要重视细胞形态学检查,如果有相关提示,应行PML-RARA融合基因检测,APL的及时诊断和治疗对患者预后有着重要的意义。当儿童疑诊APL时,无须等待确诊,可立即开始使用ATRA,砷剂可待确诊后使用。加强细胞生理、亚细胞器理论知识的掌握和理解,可以更好地掌握细胞形态,也能更好地判断和治疗APL。
患者MPO阴性时,APL的可能性较低[20] 。因此,POX阴性不一定可以排除APL,需要重视细胞形态学检查,如果有相关提示,应行PML-RARA融合基因检测,APL的及时诊断和治疗对患者预后有着重要的意义。当儿童疑诊APL时,无须等待确诊,可立即开始使用ATRA,砷剂可待确诊后使用。加强细胞生理、亚细胞器理论知识的掌握和理解,可以更好地掌握细胞形态,也能更好地判断和治疗APL。
参考文献略。
来源:熊博钰,王萌萌,马镜云,等. 以髓外侵犯首发急性早幼粒细胞白血病误诊Ewings肉瘤1例报道[J]. 检验医学,2025,40(10):1025-1029.
