
宫腔镜诊断早期输卵管癌1例分析
作者:李楠 楠,王瑞,张伟
楠,王瑞,张伟 ,杨贵霞等,德州市妇幼保健院妇科德州市妇产疾病临床医学研究中心
,杨贵霞等,德州市妇幼保健院妇科德州市妇产疾病临床医学研究中心
原发性输卵管癌(fallopian tube carcinoma,PFTC)起源于输卵管上皮,在女性生殖系统恶性肿瘤中仅占1%~2%[1]。早期输卵管癌病灶体积小、位置深隐,临床症状不典型,多表现为轻度下腹不适、异常阴道出血或白带增多等,常被误诊为功能性子宫出血 或盆腔炎性疾病
或盆腔炎性疾病 ,临床诊断困难。现有检查方法如阴道超声、CT及MRI对微小病灶识别能力有限,血清CA125等肿瘤标志物
,临床诊断困难。现有检查方法如阴道超声、CT及MRI对微小病灶识别能力有限,血清CA125等肿瘤标志物 亦在病情进展后才显著升高,难以用于早期筛查[2-3]。宫腔镜
亦在病情进展后才显著升高,难以用于早期筛查[2-3]。宫腔镜 具有直视性强、取样精准、创伤小等优势,目前已广泛用于不明原因子宫出血、宫腔占位及子宫内膜病变的诊断[4-5]。该技术可直观显示双侧输卵管间质部及开口区域,有助于在早期尚未形成明显结构破坏时,发现异常突起、病理渗出等微小改变,为早期输卵管癌的诊断提供了新途径。本文通过回顾分析1例经宫腔镜初步发现异常、后续行腹腔镜
具有直视性强、取样精准、创伤小等优势,目前已广泛用于不明原因子宫出血、宫腔占位及子宫内膜病变的诊断[4-5]。该技术可直观显示双侧输卵管间质部及开口区域,有助于在早期尚未形成明显结构破坏时,发现异常突起、病理渗出等微小改变,为早期输卵管癌的诊断提供了新途径。本文通过回顾分析1例经宫腔镜初步发现异常、后续行腹腔镜 手术确诊为早期输卵管癌的病例,系统回顾其诊疗过程,结合文献探讨宫腔镜在此类罕见疾病中的临床价值与实践意义,以提升对输卵管早期病变的识别能力。
手术确诊为早期输卵管癌的病例,系统回顾其诊疗过程,结合文献探讨宫腔镜在此类罕见疾病中的临床价值与实践意义,以提升对输卵管早期病变的识别能力。
1病例简介
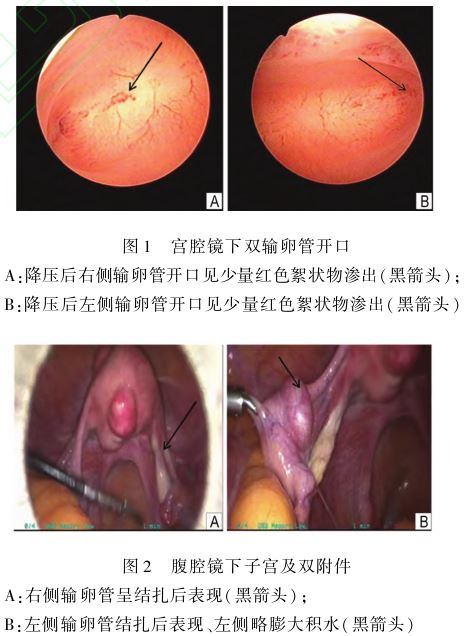
患者,女,57岁,因“绝经 8+年,近8月内间断阴道少量流血2次冶于2022年5月23日入院。患者8+年前自然绝经,否认绝经后服用激素类药物及保健品。8+月前曾因“绝经后出血冶于我院行宫腔镜检查,提示宫颈内口粘连封闭,子宫内膜薄,宫腔内未见占位。在超声引导下分离粘连,给予抗炎对症治疗,出血停止。1月前再次无诱因出现阴道少量流血,色暗红,淋漓不尽,伴间断下腹坠痛,无其他不适。11天前复查宫腔镜检查,术中见双侧输卵管开口处少量红色絮状物渗出(图1)。诊刮病理:个别腺体细胞呈鞋钉样改变。患者既往有“经腹双侧输卵管结扎术冶史。入院查体:T36.2益,P 86次/min,R 18次/min,Bp 163/115mmHg。妇科检查
8+年,近8月内间断阴道少量流血2次冶于2022年5月23日入院。患者8+年前自然绝经,否认绝经后服用激素类药物及保健品。8+月前曾因“绝经后出血冶于我院行宫腔镜检查,提示宫颈内口粘连封闭,子宫内膜薄,宫腔内未见占位。在超声引导下分离粘连,给予抗炎对症治疗,出血停止。1月前再次无诱因出现阴道少量流血,色暗红,淋漓不尽,伴间断下腹坠痛,无其他不适。11天前复查宫腔镜检查,术中见双侧输卵管开口处少量红色絮状物渗出(图1)。诊刮病理:个别腺体细胞呈鞋钉样改变。患者既往有“经腹双侧输卵管结扎术冶史。入院查体:T36.2益,P 86次/min,R 18次/min,Bp 163/115mmHg。妇科检查 :外阴发育正常,阴道内见少量暗红色血液,宫颈萎缩,子宫前位、萎缩、质中、无压痛,双附件未触及明显异常。女性肿瘤标志物(CA125、CA19鄄9、CA15鄄3、CEA、AFP)均正常。彩超提示:子宫多发性低回声结节,左附件区管状无回声(考虑输卵管积水可能),宫腔分离约2.3mm,内膜厚3mm。排除禁忌后,于2022年5月24日在全麻下行腹腔镜下全子宫+双附件切除术。术中见双侧输卵管结扎后改变(图2A),左侧输卵管略膨大积水(图2B)。术中快速病理:输卵管水肿
:外阴发育正常,阴道内见少量暗红色血液,宫颈萎缩,子宫前位、萎缩、质中、无压痛,双附件未触及明显异常。女性肿瘤标志物(CA125、CA19鄄9、CA15鄄3、CEA、AFP)均正常。彩超提示:子宫多发性低回声结节,左附件区管状无回声(考虑输卵管积水可能),宫腔分离约2.3mm,内膜厚3mm。排除禁忌后,于2022年5月24日在全麻下行腹腔镜下全子宫+双附件切除术。术中见双侧输卵管结扎后改变(图2A),左侧输卵管略膨大积水(图2B)。术中快速病理:输卵管水肿 伴少量急慢性炎细胞浸润;腹腔冲洗液见少量间皮细胞及淋巴细胞。术后病理:输卵管中分化浆液性癌,浸润浅肌层,免疫组化:ER(1+,20%),PR(-),PAX鄄8(+),p53(3+,70%,突变型),WT鄄1(-),p16(-),NHF1鄄beta(-),Ki67阳性率约15%。2022年6月15日于外院行腹腔镜下大网膜切除术+盆腔淋巴结清扫+腹主动脉旁淋巴结切除+肠粘连松解术。术后病理:各区域淋巴结均未见癌转移[左、右盆腔(0/1、0/5),腹主动脉旁(0/4)],大网膜结节为脂肪坏死,右侧骨盆漏斗韧带及大网膜未见癌。术后诊断:输卵管低级别浆液性癌IA期,术后未行辅助治疗。术后规律随访3+年,未出现肿瘤复发征象,患者一般情况良好。
伴少量急慢性炎细胞浸润;腹腔冲洗液见少量间皮细胞及淋巴细胞。术后病理:输卵管中分化浆液性癌,浸润浅肌层,免疫组化:ER(1+,20%),PR(-),PAX鄄8(+),p53(3+,70%,突变型),WT鄄1(-),p16(-),NHF1鄄beta(-),Ki67阳性率约15%。2022年6月15日于外院行腹腔镜下大网膜切除术+盆腔淋巴结清扫+腹主动脉旁淋巴结切除+肠粘连松解术。术后病理:各区域淋巴结均未见癌转移[左、右盆腔(0/1、0/5),腹主动脉旁(0/4)],大网膜结节为脂肪坏死,右侧骨盆漏斗韧带及大网膜未见癌。术后诊断:输卵管低级别浆液性癌IA期,术后未行辅助治疗。术后规律随访3+年,未出现肿瘤复发征象,患者一般情况良好。
2讨论
输卵管癌临床罕见且恶性程度较高,术前确诊率仅为2%~6%[6]。患者初诊时常被误诊为卵巢癌 、子宫内膜癌
、子宫内膜癌 或附件炎症。其典型“三联征冶(阴道不规则流血、下腹部疼痛和阴道水样分泌物)出现比例较低,临床提示意义有限[7]。部分患者仅表现为绝经后少量阴道出血或月经紊乱,易被归为功能失调性子宫出血范畴[8]。超声和常规盆腔影像检查对早期输卵管癌的敏感性较低,尤其在输卵管未显著扩张或未合并积液的条件下,病灶极易遗漏,从而延误治疗。
或附件炎症。其典型“三联征冶(阴道不规则流血、下腹部疼痛和阴道水样分泌物)出现比例较低,临床提示意义有限[7]。部分患者仅表现为绝经后少量阴道出血或月经紊乱,易被归为功能失调性子宫出血范畴[8]。超声和常规盆腔影像检查对早期输卵管癌的敏感性较低,尤其在输卵管未显著扩张或未合并积液的条件下,病灶极易遗漏,从而延误治疗。
宫腔镜作为一种直视性检查方式,传统上主要用于诊断子宫腔内病变。近年来发现,其在识别早期输卵管病变方面也具有重要作用。当输卵管病灶脱落至宫腔或输卵管开口结构异常时,宫腔镜可提供直接视野,有望突破以往诊断依赖影像和肿瘤标志物的诊断局限。输卵管癌多起源于输卵管远端腺上皮,尤以伞端区域最为常见。浆液性输卵管上皮内癌(serous tubal intraepithelial carcinoma,STIC)被视为高级别乳头状腺癌的前驱病变。STIC病灶体积微小,早期无邻近组织侵犯,临床极易被遗漏[9-10]。宫腔镜可直接观察宫颈管、宫腔形态、子宫内膜及双侧输卵管开口[11]。正常输卵管开口多呈对称的星点状或裂隙状,表面光滑。若出现不对称、突出、毛糙或渗血等异常,应高度警惕是否存在潜在病变。早期输卵管癌可能向宫腔方向生长,宫腔镜能够发现开口区的微小突变、乳头样赘生物或渗血等改变,而这些细节常被传统检查忽略。相较于盲视的分段诊刮术[12],宫腔镜可对可疑区域进行靶向取材,显著提高诊断的灵敏度与特异性[13]。
超声在识别输卵管早期病灶方面存在局限。无积液时输卵管难以辨识,诊断依赖于操作者经验和设备分辨率。CT与MRI虽能提供更清晰的软组织结构图像,但对于<1cm的病灶敏感性亦有限,且成本高昂、操作时间长。相比之下,宫腔镜操作简便、可重复,能在微创条件下获得组织标本,是目前少数能在“常规无异常冶时主动发现潜在病变的工具[14-15],尤其适用于绝经后不明原因出血、子宫内膜无病变但症状持续的患者。本研究患者因绝经后出血就诊,常规检查未见明确异常,宫腔镜下可见血液自输卵管口溢出,且足量、足疗程抗炎治疗后症状仍持续,因此高度可疑输卵管肿瘤。因此,提示在临床实践中,宫腔镜检查应常规评估输卵管开口区,不能只关注子宫内膜或宫腔形态。对可疑异常,既使超声及肿瘤指标均为阴性,也需充分活检。
宫腔镜在早期诊断输卵管癌方面仍存在局限:(1)视野受限:仅能观察输卵管间质部至近端区域,远端(尤其伞端)病变若未向宫腔突出,可能被遗漏[15];(2)操作者依赖性强:输卵管开口结构细微,识别细微异常对操作者技术及经验要求高,且受膨宫压、术中出血、视角等因素影响,目前尚无统一的形态学分类标准,诊断存在主观差异;(3)取样技术待改进:输卵管区域位置较深,现有器械进行精准活检仍有一定难度,取样不充分可能导致假阴性。未来研究方向包括:建立宫腔镜下输卵管开口区域的形态学评估标准与分级系统,提高判读一致性;推动数字宫腔镜系统、光学增强成像、AI图像分析技术的发展[16],提升识别效率;联合分子标志物检测、液基细胞学检查,构建多维度早期筛查模型。对于BRCA基因突变携带者、有家族史等高危人群,可考虑将宫腔镜纳入定期随访方案,制定标准化、个体化监测路径。
综上所述,宫腔镜检查在早期输卵管癌诊断中具有独特优势,尤其在常规影像学及临床表现不典型时,提供了直视发现病灶并进行定点活检的可能性。本病例表明,宫腔镜不仅能评估不明原因子宫出血,也可作为高危人群早期妇科恶性肿瘤筛查 的重要工具。未来结合人工智能、分子病理等新技术,有望进一步提升其早期诊断的准确性与临床价值,为输卵管癌的早诊早治提供更可靠的支持。
的重要工具。未来结合人工智能、分子病理等新技术,有望进一步提升其早期诊断的准确性与临床价值,为输卵管癌的早诊早治提供更可靠的支持。
参考文献略。
来源:李楠楠,王瑞,张伟,等.宫腔镜诊断早期输卵管癌1例分析[J/OL].现代妇产科进展,1-2[2026-03-13].https://doi.org/10.13283/j.cnki.xdfckjz.2026.04.033.
