
低级别浆液性卵巢癌1例并文献复习
作者:王小伟,宋玉琴 ,陆建荣,王国庆等,陕西省肿瘤医院妇瘤科;庆阳市人民医院妇科
,陆建荣,王国庆等,陕西省肿瘤医院妇瘤科;庆阳市人民医院妇科
卵巢癌 是常见的且最为致命的妇科癌症之一,死亡率居妇科恶性肿瘤之首。据WHO最新数据统计,2022年全球卵巢癌新发病例32.5万例,死亡病例20.7万例,而中国卵巢癌新发和死亡病例分别为6.1万例和3.3万例[1]。上皮性卵巢癌(epithelialovariancancer,EOC)约占卵巢恶性肿瘤的80%~90%,其中浆液性卵巢癌(serousovariancancer,SOC)占EOC的75%~80%。根据形态学和分子遗传学的研究,Shih等[2]最早于2004年提出二元模型论,将EOC分为两型:I型和II型,基于此模型,SOC又被分为高级别浆液性卵巢癌(high⁃gradeserousovariancancer,HGSOC)和低级别浆液性卵巢癌(low⁃gradeserousovariancancer,LGSOC)两种类型。LGSOC是EOC中较为少见的一种病理类型,约占卵巢癌的1.02%~3.64%,占SOC的4%~10%[3]。随着对LGSOC的不断研究,有研究发现LGSOC与HGSOC相比,具有不同的生物学行为、临床特征及分子信号通路[4⁃5]。在临床特征方面,HGSOC中位发病年龄56~63岁,病情发展迅速,侵袭性强,对紫杉醇
是常见的且最为致命的妇科癌症之一,死亡率居妇科恶性肿瘤之首。据WHO最新数据统计,2022年全球卵巢癌新发病例32.5万例,死亡病例20.7万例,而中国卵巢癌新发和死亡病例分别为6.1万例和3.3万例[1]。上皮性卵巢癌(epithelialovariancancer,EOC)约占卵巢恶性肿瘤的80%~90%,其中浆液性卵巢癌(serousovariancancer,SOC)占EOC的75%~80%。根据形态学和分子遗传学的研究,Shih等[2]最早于2004年提出二元模型论,将EOC分为两型:I型和II型,基于此模型,SOC又被分为高级别浆液性卵巢癌(high⁃gradeserousovariancancer,HGSOC)和低级别浆液性卵巢癌(low⁃gradeserousovariancancer,LGSOC)两种类型。LGSOC是EOC中较为少见的一种病理类型,约占卵巢癌的1.02%~3.64%,占SOC的4%~10%[3]。随着对LGSOC的不断研究,有研究发现LGSOC与HGSOC相比,具有不同的生物学行为、临床特征及分子信号通路[4⁃5]。在临床特征方面,HGSOC中位发病年龄56~63岁,病情发展迅速,侵袭性强,对紫杉醇 和铂类为基础的化疗敏感,但治疗后易复发,5年生存率较低,约40%。LGSOC中位发病年龄43~55岁,病情进展缓慢,表现为惰性生物学行为,对标准化疗敏感性较低,但5年生存率较高约75%[6⁃8]。在分子生物学特征方面,HGSOC具有较高TP53突变率,BRCA基因突变及其他基因突变导致的同源重组修复缺陷,同时常有包括CCNE1、NOTCH3、AKT2、RSF1、PIK3CA等在内的DNA拷贝数量异常。LGSOC中罕见TP53突变,常表现为TP53野生型,而KRAS、BRAF、NRAS、ERBB2突变较常见,进而诱导其下游MAPK信号通路的激活参与肿瘤的发生发展,LGSOC也存在PI3K⁃AKT⁃mTOR通路相关的IK3CA、FFAR1、USP9X和EIF1A的驱动突变[9⁃12]。此外,LGSOC组织中有较高的雌孕激素
和铂类为基础的化疗敏感,但治疗后易复发,5年生存率较低,约40%。LGSOC中位发病年龄43~55岁,病情进展缓慢,表现为惰性生物学行为,对标准化疗敏感性较低,但5年生存率较高约75%[6⁃8]。在分子生物学特征方面,HGSOC具有较高TP53突变率,BRCA基因突变及其他基因突变导致的同源重组修复缺陷,同时常有包括CCNE1、NOTCH3、AKT2、RSF1、PIK3CA等在内的DNA拷贝数量异常。LGSOC中罕见TP53突变,常表现为TP53野生型,而KRAS、BRAF、NRAS、ERBB2突变较常见,进而诱导其下游MAPK信号通路的激活参与肿瘤的发生发展,LGSOC也存在PI3K⁃AKT⁃mTOR通路相关的IK3CA、FFAR1、USP9X和EIF1A的驱动突变[9⁃12]。此外,LGSOC组织中有较高的雌孕激素 受体表达,为激素治疗提供了指导价值[13⁃14]。本文报道1例因“卵巢囊肿”行“囊肿剥除术”时意外发现的年仅28岁的LGSOC患者,在经过初始肿瘤细胞减灭术⁃疾病复发⁃二次肿瘤细胞减灭术⁃疾病复发⁃激素维持治疗的模式后总生存期长达10余年之久,现报道如下。
受体表达,为激素治疗提供了指导价值[13⁃14]。本文报道1例因“卵巢囊肿”行“囊肿剥除术”时意外发现的年仅28岁的LGSOC患者,在经过初始肿瘤细胞减灭术⁃疾病复发⁃二次肿瘤细胞减灭术⁃疾病复发⁃激素维持治疗的模式后总生存期长达10余年之久,现报道如下。
1 病例报告
患者,女,28岁,以“卵巢癌术后3月,3程化疗后1月,腹胀1周”之主诉于2011年9月19日首次就诊于陕西省肿瘤医院。2011年6月患者因“卵巢囊肿(双侧);原发性不孕”在当地医院行“腹腔镜 下双侧卵巢囊肿剥除+双侧输卵管通液术”,术后病理结果回报示:双侧卵巢交界性肿瘤并局部癌变(浆液性腺癌),术后行多西他赛
下双侧卵巢囊肿剥除+双侧输卵管通液术”,术后病理结果回报示:双侧卵巢交界性肿瘤并局部癌变(浆液性腺癌),术后行多西他赛 +奥沙利铂
+奥沙利铂 化疗3程,为进一步诊治,患者转至陕西省肿瘤医院就诊。入院后查体:生命体征平稳,心肺腹查体未见明显异常。妇科检查
化疗3程,为进一步诊治,患者转至陕西省肿瘤医院就诊。入院后查体:生命体征平稳,心肺腹查体未见明显异常。妇科检查 :外阴已婚式,阴毛呈女性分布;阴道通畅,黏膜光滑,分泌物不多;宫颈光滑常大;宫体前位,稍大,质中,活动稍差,无压痛;左右附件区分别可触及约6cm、5cm大小包块,质软,固定,压痛阴性;三合诊
:外阴已婚式,阴毛呈女性分布;阴道通畅,黏膜光滑,分泌物不多;宫颈光滑常大;宫体前位,稍大,质中,活动稍差,无压痛;左右附件区分别可触及约6cm、5cm大小包块,质软,固定,压痛阴性;三合诊 双侧骶主韧带无增厚。患者既往因“阑尾炎
双侧骶主韧带无增厚。患者既往因“阑尾炎 ”切除阑尾,余无特殊。入院后完善相关检查,会诊外院病理切片结果示:“双侧”卵巢交界性浆液性乳头状囊腺瘤,局灶浆液性腺癌I级形成。腹部及盆腔CT提示:双侧附件区包块,右侧约4.4cm×6.2cm,左侧约5.0cm×5.0cm大小,内可见分割,余无异常。肿瘤标志物
”切除阑尾,余无特殊。入院后完善相关检查,会诊外院病理切片结果示:“双侧”卵巢交界性浆液性乳头状囊腺瘤,局灶浆液性腺癌I级形成。腹部及盆腔CT提示:双侧附件区包块,右侧约4.4cm×6.2cm,左侧约5.0cm×5.0cm大小,内可见分割,余无异常。肿瘤标志物 :CA⁃12546.7U/mL,HE4:102.9pmol/L。结合患者病史及辅助检查考虑LGSOC不全术后未控,与患者及家属充分沟通病情后于2011年9月23日行全子宫+双附件切除+大网膜切除术,术中探查见腹腔内约400mL草绿色清亮腹水
:CA⁃12546.7U/mL,HE4:102.9pmol/L。结合患者病史及辅助检查考虑LGSOC不全术后未控,与患者及家属充分沟通病情后于2011年9月23日行全子宫+双附件切除+大网膜切除术,术中探查见腹腔内约400mL草绿色清亮腹水 ,大网膜表面散在粟粒至米粒大小结节,肠管间扭曲,呈广泛膜状粘连,未见梗阻表现,阑尾缺如,双侧卵巢均囊实性多房性增大,与周围组织广泛粘连,双侧输卵管外观毛糙,呈慢性炎症改变,腹主动脉旁及盆腔各组淋巴结均未触及肿大,手术后评估达R0。术后病理结果回报提示:“双侧”卵巢交界性浆液性乳头状囊腺瘤,局灶浆液性腺癌I级形成,大网膜见癌种植,“右侧”输卵管见癌浸润,“左侧”输卵管组织,子宫内膜单纯性增生,慢性宫颈炎
,大网膜表面散在粟粒至米粒大小结节,肠管间扭曲,呈广泛膜状粘连,未见梗阻表现,阑尾缺如,双侧卵巢均囊实性多房性增大,与周围组织广泛粘连,双侧输卵管外观毛糙,呈慢性炎症改变,腹主动脉旁及盆腔各组淋巴结均未触及肿大,手术后评估达R0。术后病理结果回报提示:“双侧”卵巢交界性浆液性乳头状囊腺瘤,局灶浆液性腺癌I级形成,大网膜见癌种植,“右侧”输卵管见癌浸润,“左侧”输卵管组织,子宫内膜单纯性增生,慢性宫颈炎 。术后诊断:卵巢低级别浆液性腺癌IIIB期。术后给予紫杉醇+卡铂
。术后诊断:卵巢低级别浆液性腺癌IIIB期。术后给予紫杉醇+卡铂 全身静脉化疗6程(末次化疗时间:2012.03.02)后评估疾病达CR,按时于门诊随访。
全身静脉化疗6程(末次化疗时间:2012.03.02)后评估疾病达CR,按时于门诊随访。
2018年8月,患者常规复查时发现CA12558.8U/mL,HE4189.8pmol/L,PET⁃CT:子宫及双附件术后缺如,脾脏混杂密度病变,葡萄糖 代谢不均匀增高,提示恶性病变,转移性肿瘤可能,肝左叶内侧段血管瘤
代谢不均匀增高,提示恶性病变,转移性肿瘤可能,肝左叶内侧段血管瘤 ,副脾。遂以“卵巢低级别浆液性腺癌IIIB期术后化疗后;恶性肿瘤复发”收住院,入院后行影像学评估提示肿瘤病灶孤立于脾脏,考虑患者系铂敏感复发、无腹水、肿瘤孤立可切除,于2018⁃08⁃31在全麻下行脾脏+肿瘤切除+副脾切除术,术后病理提示:脾脏见腺癌浸润,结合免疫组化结果考虑低级别浆液性癌,以卵巢来源可能性大,肿瘤大小6.5cm×6cm×6cm,癌组织侵犯但未浸透被膜,脾脏断端未见癌,另见副脾一枚。免疫组化显示肿瘤细胞p16(局灶+),PR(⁃),ER(+40%),ki67(15%),WT⁃1(⁃),p53(⁃),术后行基因检测提示BRCA(⁃)。给予紫杉醇脂质体+卡铂全身静脉化疗6程达完全缓解(末次化疗时间:2019.01),后门诊按时随访。
,副脾。遂以“卵巢低级别浆液性腺癌IIIB期术后化疗后;恶性肿瘤复发”收住院,入院后行影像学评估提示肿瘤病灶孤立于脾脏,考虑患者系铂敏感复发、无腹水、肿瘤孤立可切除,于2018⁃08⁃31在全麻下行脾脏+肿瘤切除+副脾切除术,术后病理提示:脾脏见腺癌浸润,结合免疫组化结果考虑低级别浆液性癌,以卵巢来源可能性大,肿瘤大小6.5cm×6cm×6cm,癌组织侵犯但未浸透被膜,脾脏断端未见癌,另见副脾一枚。免疫组化显示肿瘤细胞p16(局灶+),PR(⁃),ER(+40%),ki67(15%),WT⁃1(⁃),p53(⁃),术后行基因检测提示BRCA(⁃)。给予紫杉醇脂质体+卡铂全身静脉化疗6程达完全缓解(末次化疗时间:2019.01),后门诊按时随访。
2019年5月患者以“CA125升高”再次入院(CA12546.67U/mL),入院后妇科检查见阴道残端增厚,可触及直径约1cm大小结节。盆腔MRI提示:系卵巢癌术后,阴道残端较前明显增厚。阴道残端穿刺活检病理提示:“阴道残端”符合浆液性腺癌。考虑患者此次系铂耐药复发,完善相关检查后行多柔比星 脂质体+贝伐珠单抗
脂质体+贝伐珠单抗 全身静脉化疗4程(末次化疗时间2019.07),经评估疾病达CR后与患者及家属充分沟通,给予来曲唑
全身静脉化疗4程(末次化疗时间2019.07),经评估疾病达CR后与患者及家属充分沟通,给予来曲唑 口服维持治疗(2.5mg/次,QD),现患者仍门诊如期随访,处于无瘤生存状态,从初始治疗至今总生存期约10年余。
口服维持治疗(2.5mg/次,QD),现患者仍门诊如期随访,处于无瘤生存状态,从初始治疗至今总生存期约10年余。
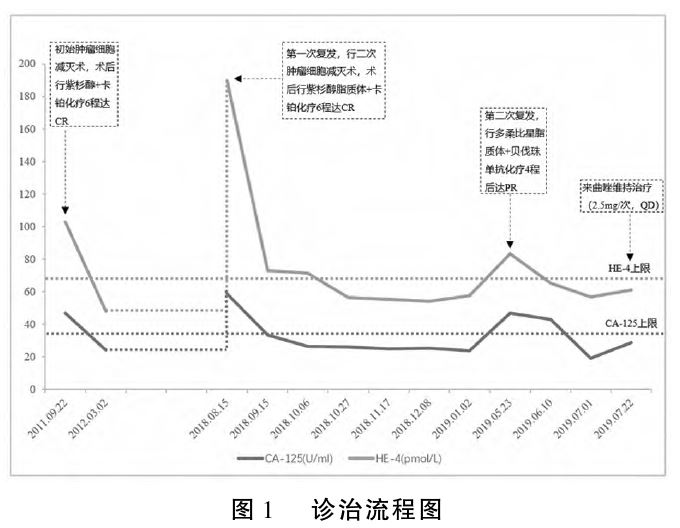
诊治过程见图1。
2 讨论
由于LGSOC临床少见,目前缺乏大规模前瞻性系统性的临床研究。一项来自国内的回顾性临床研究对381例SOC进行分析发现LGSOC约占9.2%,LGSOC较HGSOC相比发病年龄提前10岁(46岁vs.56岁,P<0.05)[15],与Matsuo等[16]报道美国LGSOC中位发病年龄43~47岁相当。Farrell等[17]报道澳大利亚和新西兰LGSOC年发病人数约占总EOC的5.6%和9.0%。在一项基于350名Ⅱ~Ⅳ期LGSOC患者的回顾性研究中,患者接受初始手术继以铂为基础的化疗后,中位PFS及OS分别为28.1月和101.7月,多因素分析显示与年龄小于35岁者相比,年龄大于35岁者死亡率下降47%(HR:0.53,95%CI:0.37⁃0.75)[18]。此外肥胖(HR:2.53,95%CI:1.19⁃5.38)、吸烟(HR:1.73,95%CI:1.03⁃2.92)、不满意的肿瘤细胞减灭术(HR:2.79,95%CI:1.67⁃6.70)、FIGOIV期(HR:3.15,95%CI:1.29⁃7.66)也是LGSOC的不良预后因素[19⁃20]。
2.1 LGSOC起源假说
传统理论经典的卵巢表面上皮化生学说认为所有的EOC均来源于卵巢本身,基于大量流病学研究发现分娩 和口服避孕药可明显降低卵巢癌风险,有研究提出排卵引起卵巢表面上皮持续性损伤和修复,导致DNA损伤及卵巢表面上皮或其内陷形成的皮质包涵体囊肿发生恶性转化的假说[21]。但有研究表明卵巢表面上皮与EOC在细胞形态学和免疫组化上无同源性,因此该理论被质疑[22]。随后Lauchlan[23]首次提出第二苗勒管起源理论,认为卵巢肿瘤来源于输卵管旁、卵巢旁的第二苗勒氏系统,即苗勒上皮残迹及其囊肿发生恶性病变。但该理论很难解释各种上皮性卵巢癌的起源。近年来,随着对具有BRCA基因突变的卵巢癌高危人群进行预防性输卵管卵巢切除,发现卵巢内无病变,而在输卵管中存在非浸润性或浸润性肿瘤,进而Piek等[24]提出输卵管来源学说。目前认为LGSOC的发生是一个连续的过程,即从卵巢上皮性包涵体到良性囊腺瘤,再到浆液性交界性肿瘤,最终发展为LGSOC[25]。Kurman等[26]基于91%的LGSOC患者输卵管上皮存在乳头状增生性病变,提出了输卵管乳头状增生来源学说,并成功构建相关模型。Laury等[27]在另一项研究中表明浆液性交界性肿瘤患者输卵管上皮较正常人输卵管上皮PAX⁃2阴性的分泌细胞呈现过度生长,为LGSOC输卵管来源提供了进一步的佐证。
和口服避孕药可明显降低卵巢癌风险,有研究提出排卵引起卵巢表面上皮持续性损伤和修复,导致DNA损伤及卵巢表面上皮或其内陷形成的皮质包涵体囊肿发生恶性转化的假说[21]。但有研究表明卵巢表面上皮与EOC在细胞形态学和免疫组化上无同源性,因此该理论被质疑[22]。随后Lauchlan[23]首次提出第二苗勒管起源理论,认为卵巢肿瘤来源于输卵管旁、卵巢旁的第二苗勒氏系统,即苗勒上皮残迹及其囊肿发生恶性病变。但该理论很难解释各种上皮性卵巢癌的起源。近年来,随着对具有BRCA基因突变的卵巢癌高危人群进行预防性输卵管卵巢切除,发现卵巢内无病变,而在输卵管中存在非浸润性或浸润性肿瘤,进而Piek等[24]提出输卵管来源学说。目前认为LGSOC的发生是一个连续的过程,即从卵巢上皮性包涵体到良性囊腺瘤,再到浆液性交界性肿瘤,最终发展为LGSOC[25]。Kurman等[26]基于91%的LGSOC患者输卵管上皮存在乳头状增生性病变,提出了输卵管乳头状增生来源学说,并成功构建相关模型。Laury等[27]在另一项研究中表明浆液性交界性肿瘤患者输卵管上皮较正常人输卵管上皮PAX⁃2阴性的分泌细胞呈现过度生长,为LGSOC输卵管来源提供了进一步的佐证。
2.2 LGSOC分子生物学特征
LGSOC中通常存在MAPK通路相关基因的突变,如KRAS、BRAF、NRAS、ERBB2,也会有活化PI3K⁃AKT⁃mTOR通路相关基因的驱动突变[12]。VanNievwenhuysen等[28]在对38例LGSOC肿瘤样本进行全基因组拷贝数和突变热点检测的研究中发现,24%的患者中存在KRAS突变,7.8%的患者存在BRAF突变,8.3%的患者存在NRAS突变。Grisham等[29]报道了1例经传统测序技术未能检出而经二代分子测序发现病灶中存在MAPK通路缺失和融合突变的病例,提示对于该类型患者尽量行二代测序进行相关基因的检查。Leskela等[30]在一项针对502例早期卵巢癌患者组织学类型及免疫组化特征的研究中发现,95%LGSOC患者WT1阳性,90%p53野生型,57%ER阳性,78%PR阳性。建议对该类型患者实施基于分子生物学特征为指导的靶向治疗,更好地制定个体化治疗方案以期提高患者生存率。
2.3 LGSOC的治疗
2.3.1 LGSOC的手术治疗 同HGSOC一样,手术仍然是LGSOC的主要治疗手段,且术后残留病灶的大小与预后显著相关。Nickles等[31]报道了189例LGSOC患者研究数据显示,手术达R0的患者PFS和OS分别为33.2月和96.9月,而术后残留病灶在0.1~1cm和>1cm的亚组,PFS和OS分别为14.7月、44.5月和14.1月、42.0月,且差异具有统计学意义。在相同数据的另一项研究中,Fader等[32]对CA125水平和患者预后进行评估发现,CA125在化疗1~3个周期后恢复正常的患者与4个周期后恢复正常或从未恢复正常者相比,疾病进展的可能性降低60%~64%(P≤0.024),且在第二程化疗前CA125就转阴的患者与疾病死亡风险呈显著负相关。这提示对于LGSOC患者,CA125可作为判断预后的潜在指标。Bogani等[20]在一项回顾性研究中报道了72例LGSOC患者临床资料发现,与接受CRS患者相比行IDS者预后更差(HR=2.95;95%CI=1.12⁃7.74),鉴于LGSOC对初始化疗易耐药的特性,研究者对IDS在LGSOC患者中的应用提出质疑,但该研究系回顾性研究,样本量较少且研究中缺少关于病灶累及部位及数量的记载,可能IDS组患者肿瘤负荷更大,临床分期更晚。所以,仍需要更多高质量的循证医学数据来证实IDS在LGSOC中的作用。虽然LGSOC远期预后较好,但约80%患者会发生疾病复发[33],Crane等[34]报道了41例接受二次肿瘤细胞减灭术的复发性LGSOC患者,术后无肉眼病灶残留者中位PFS为60.3月,而有肉眼残留病灶者仅10.7月。所以对于复发性LGSOC,满意的二次肿瘤细胞减灭术仍能使患者从中获益。Minig等[35]研究发现对于I期LGSOC,无论淋巴结阳性与否,患者PFS及OS并无显著差异,所以对于早期患者可不
行盆腔淋巴结清扫。关于晚期患者系统切除淋巴结是否获益仍有不同观点,Gockley等[36]报道晚期患者行淋巴结清扫可显著提高患者中位OS,而Aslan等[37]报道系统的淋巴结切除并不能改善患者的远期预后。
2.3.2 LGSOC的化学治疗 虽然LGSOC对化疗敏感性较低,但术后仍建议行全身静脉化疗。对于IA和IB期患者,术后可选择观察,IC期患者在充分知情的前提下可选择观察、化疗或内分泌治疗,而Ⅱ~Ⅳ期患者术后应辅以紫衫/卡铂化疗。复发患者对化疗的反应率更低,除激素治疗外化疗仍是重要治疗手段。对铂敏感复发患者仍推荐以铂为基础化疗方案,如紫杉醇/卡铂、多柔比星脂质体/卡铂。铂耐药患者首选非铂类化疗如:多西他赛单药、多柔比星脂质体±贝伐珠单抗、紫杉醇周疗±贝伐珠单抗等[38]。
2.3.3 LGSOC的内分泌及靶向治疗 内分泌治疗在LGSOC的治疗中具有重要的意义,2021NCCN指南将芳香化酶抑制剂纳入初始治疗首选方案中,与TC±贝伐珠单抗并列。常用的芳香化酶抑制剂包括阿那曲唑 、来曲唑、依西美坦
、来曲唑、依西美坦 、醋酸亮丙瑞林
、醋酸亮丙瑞林 、他莫昔芬
、他莫昔芬 等。Gershenson等[13]在一项针对Ⅱ~Ⅳ期LGSOC患者的回顾性研究中发现,在经过手术和化疗后,接受激素维持治疗组较未接受激素维持治疗组PFS获益更大(64.9月vs.26.4月,P<0.001),而OS在两组中相似(115.7月vs.102.7月,P=0.42)。一项针对复发性LGSOC的随机前瞻性Ⅱ期临床试验表明,对于ER/PR阳性的复发患者使用阿那曲唑治疗6个月后客观缓解率为14%,临床受益率为61%[39]。目前仍有很多针对激素治疗的临床研究。由于LGSOC患者对化疗应答率较低,激素治疗可能为LGSOC患者提供临床益处。目前部分证据支持MEKi、BRAF抑制剂治疗LGSOC的有效性[4],GOG⁃0239使用司美替尼
等。Gershenson等[13]在一项针对Ⅱ~Ⅳ期LGSOC患者的回顾性研究中发现,在经过手术和化疗后,接受激素维持治疗组较未接受激素维持治疗组PFS获益更大(64.9月vs.26.4月,P<0.001),而OS在两组中相似(115.7月vs.102.7月,P=0.42)。一项针对复发性LGSOC的随机前瞻性Ⅱ期临床试验表明,对于ER/PR阳性的复发患者使用阿那曲唑治疗6个月后客观缓解率为14%,临床受益率为61%[39]。目前仍有很多针对激素治疗的临床研究。由于LGSOC患者对化疗应答率较低,激素治疗可能为LGSOC患者提供临床益处。目前部分证据支持MEKi、BRAF抑制剂治疗LGSOC的有效性[4],GOG⁃0239使用司美替尼 治疗复发性LGSOC,ORR为15%,SD为65%,GOG⁃0281是一项评估曲美替尼
治疗复发性LGSOC,ORR为15%,SD为65%,GOG⁃0281是一项评估曲美替尼 在复发性LGSOC疗效的III期临床试验,在这项研究中,接受曲美替尼治疗的患者的中位PFS为13.0月,而对照组仅7.2月[33,40]。
在复发性LGSOC疗效的III期临床试验,在这项研究中,接受曲美替尼治疗的患者的中位PFS为13.0月,而对照组仅7.2月[33,40]。
本文报道的病例在最初明确诊断时患者仅28岁,较文献报道中位发病年龄偏低,但患者总生存期长达10余年,可能得益于患者两次满意的肿瘤细胞减灭术及激素维持治疗,这也为满意的肿瘤细胞减灭术及激素治疗使LGSOC生存获益提供了有力证据。但本病例在诊治过程中仍存在不足,例如激素维持治疗如果能更早应用,患者远期获益可能会更大,当然这也是由于在当时的治疗背景下激素治疗循证医学证据不足所致。此外,对该患者行二代测序进行相关基因的检测,实施基于分子生物学特征为指导的精准靶向治疗可能为患者带来更多获益。由于LGSOC临床少见,目前关于EOC的基础及临床研究绝大多数试验均源于HGSOC的研究。整体来看,手术仍是LGSOC的主要治疗手段,且R0切除对远期预后至关重要,虽然LGSOC对化疗敏感性较差,但手术后辅以铂类为主的化疗仍是一线治疗方案,随着对LGSOC认识的不断提高,内分泌激素治疗在LGSOC中逐渐起到了重要作用,MAPK及PI3K⁃AKT⁃mTOR通路相关的分子靶向治疗也为LGSOC的治疗寄予了新的希望,进一步研究LGSOC基因组学确定致癌过程中涉及的基因突变靶点,以期为LGSOC患者治疗提供有力佐证是迫切需要的。
利益冲突 作者均声明无利益冲突。
参考文献略。
来源:王小伟,宋玉琴,陆建荣,等.低级别浆液性卵巢癌1例并文献复习[J].中国计划生育和妇产科,2026,18(02):109-112.
