
胚胎植入前遗传学检测阻断男性染色体复杂重排1例报道
作者:李耀辉,李久洋,韩少华,焦泽华等,赤峰市妇产医院生殖医学中心
病例资料
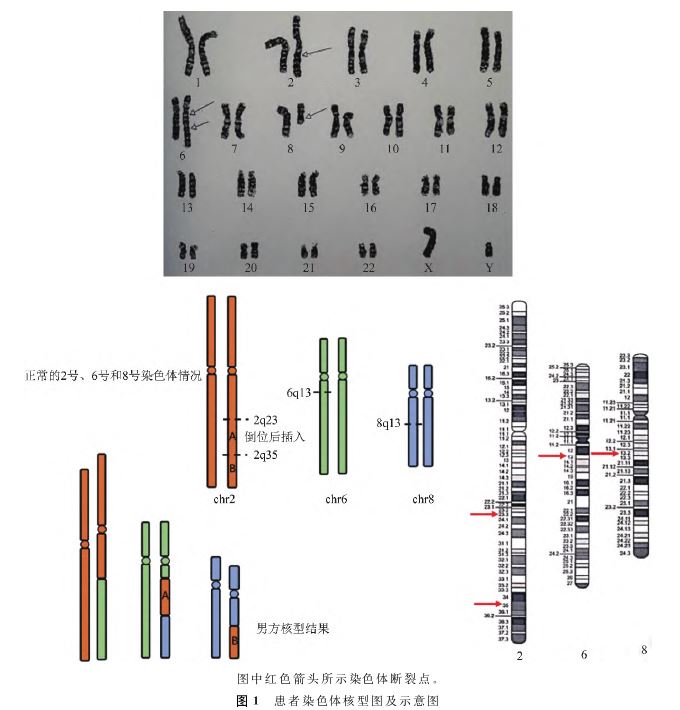
患者,男,31岁,已婚,2021年10月就诊我院,主诉未避孕未育6年,性生活每周1~2次,无性功能障碍,患者既往体健,无泌尿生殖系统感染,外生殖器未见畸形,无有毒有害物质接触史。2016年12月就诊北京大学第三医院,经查染色体细胞核型结果为:46XY,t(2;8;6)(2pter→2q23::6q13→6qter;8pter→8q13::2q35→2qter;6pter→6q13::2q35→ 2q23::8q13→8qter)(图1),Y染色体微缺失(Y AZF)未见缺失,可通过手淫正常取精,精液检测3次结果均提示为重度少弱精子症(即镜下见精子0~1条/每高倍视野,偶见前向运动精子),初步诊断:原发性男性不育,染色体核型异常。遗传咨询建议行胚胎植入前遗传学检测技术(PGT)。2017年8月,女方就诊北京大学第三医院,染色体细胞核型结果为:46,XX,输卵管造影提示双侧输卵管通畅,遂夫妻双方行PGT助孕,但未成功。于2021年10月就诊我院,男方父母进行染色体核型分析,结果分别为46,XY和46,XX,再次进行遗传咨询,同样建议行PGT助孕。
男方由于患少弱精子症,临床担心取卵当日无法获得可用精子,建议其提前冷冻精子,但因费用问题,男方拒绝冷冻。女方平素月经规律,5~6d/28d,无痛经,G0P0。血清雌二醇(E2)198.05pmol/L、卵泡刺激素(FSH)8.14U/L、黄体生成素(LH)3.34U/L、孕酮(P)3.46nmol/L、抗苗勒管激素(AMH)1.82ng/ml,甲功、血常规、肝肾功、血糖血脂、凝血功能等未见异常,彩超示窦卵泡数9枚,根据女方血清激素水平及阴道B超下双侧卵巢窦卵泡计数选择拮抗剂方案,于月经第2天开始促排卵,给予重组人促卵泡激素(金塞恒;长春金赛药业)300U/d启动,促排卵第6天加拮抗剂醋酸西曲瑞克(金塞捷;长春金赛药业)0.25mg qd,连续4d,共促排卵9d。使用250μg重组人绒毛膜促性腺激素(艾泽;默克雪兰诺,德国)+0.2mg醋酸曲普瑞林(金磊;长春金赛药业)扳机,扳机36h后取卵,取卵8枚。男方通过手淫取精,行卵胞浆内单精子注射(ICSI)授精,获得正常受精胚胎(2PN)6枚,继续行囊胚培养至D6,形成有冷冻价值的囊胚1枚。因男方染色体复杂平衡易位(CCRs)为新发型,需要≥3枚胚胎样本进行单体型构建分析,故此枚胚胎予冷冻保存,拟择期进行第二周期促排卵。2022年4月再次就诊我院行第二周期促排卵,同样选择拮抗剂方案,月经第2天开始促排卵,给予重组人促卵泡激素300U/d启动,促排第5天加拮抗剂醋酸西曲瑞克0.25mg qd,连续3d,共促排卵7d。扳机取卵同前,取卵4枚,行ICSI授精,其中正常受精胚胎(2PN)3枚,获得有冷冻价值的囊胚共2枚。PGT-SR检测结果:1枚为可移植胚胎即E1,2枚为不可移植胚胎。其中E2胚胎结果显示:2号染色体q23.3q37.1区域发生77.46Mb重复;6号染色体q13q27区域发生96.06Mb缺失;8号染色体q21.11q24.3区域发生69.44Mb重复。E3胚胎结果显示:1号、3-5号、7号、9-10号、12-22号染色体为3个拷贝;2号染色体p25.3q23.3区域为3个拷贝;2号染色体q23.3q37.1区域为2个拷贝;2号染色体q37.1q37.3区域为3个拷贝;6号染色体p25.3q13区域为3个拷贝;6号染色体q13q27区域为4个拷贝;8号染色体p23.3q21.11区域为3个拷贝;8号染色体q21.11q24.3区域为2个拷贝;11号染色体p15.5p11.2区域为2个拷贝;11号染色体p11.2q25区域为3个拷贝;X染色体为2个拷贝;Y染色体为1个拷贝。胚胎检测结果见表1和图2。
内膜准备及胚胎移植:自月经第4天开始口服雌二醇/地屈孕酮片(芬吗通;雅培,荷兰)砖红色片(含雌二醇2mg),1次1片tid。服药第15天监测子宫内膜厚度达8mm,开始转化内膜,口服芬吗通黄色片(含雌二醇2mg和地屈孕酮10mg),1片/次tid;并肌肉注射黄体酮注射液(浙江仙琚制药),60mg/次qd,进行内膜转化并黄体支持。于2022年7月移植囊胚1枚,移植后继续按照原剂量进行黄体支持。于移植术后14d检测血清β-HCG 1 112U/L,E24 164.59pmol/L,P 91.27nmol/L。移植术后22d血β-HCG为16 218U/L,E2560.12pmol/L,P 84.59nmol/L;超声检查示宫腔内可见1个妊娠囊回声,大小为1.1cm×0.6cm×0.5cm,未见胚芽及胎心搏动,提示宫内早孕(建议复查)。移植后32d超声示孕囊大小为4.0cm×3.0cm×3.1cm,可见胎心搏动,胚芽长1.1cm。孕18周行羊膜腔穿刺术取羊水行基因检测报告显示:未检出染色体非整倍体或100Kb以上已知的、明确致病的基因组拷贝数变异;染色体核型:46,XN。之后产检未见明显异常。患者孕36+6周胎心监护提示胎儿宫内缺氧,剖宫产分娩1女活婴,体重2 960g、身长50cm、Apgar评分10分,一般情况及查体正常。1周岁时电话随访结果:幼儿体重11kg,身高78cm,外观正常,生长发育及智力无异常。
讨 论
染色体是遗传物质的载体,人类染色体的正常结构和数目对于个体的健康和生殖功能至关重要。染色体异常是导致人类生殖障碍、先天性疾病和发育异常的重要原因之一。据报道,在自然流产的胚胎组织中,约50%存在染色体异常。其中,染色体结构重排是一类较为常见的染色体异常,包括易位、倒位、缺失、重复等。
染色体复杂重排(CCRs)是指有2条或2条以上染色体至少包括3个断裂点的染色体结构异常,并且在染色体间或染色体内单段插入或易位等。按遗传来源分为家族型和新发型,无论是家族型还是新发CCRs都极为少见。男性CCRs患者大多数无明显的外观或智力发育异常,往往因不育而就诊,由于精子生成障碍临床表现为无精子症或严重少弱精子症[1-3],这可能是因为“位置效应”(染色体畸变改变了一个基因与其邻近基因或与其邻近染色质的位置关系,从而使它的表型效应也发生变化的现象)或关键基因断裂而导致的亚临床表型。
本例患者核型分析显示46XY,t(2;8;6)(2pter→2q23::6q13→6qter;8pter→8q13::2q35→2qter;6pter→6q13::2q35→2q23::8q13→8qter),涉及3条染色体(2号、6号、8号)的4个断裂点(2q23、2q35、6q13、8q13)与3种衍生染色体组合。与简单易位相比,此类复杂重排在减数分裂时可形成多达27种配子组合。值得注意的是,断裂点2q35,含精子鞭毛轴螺旋蛋白2(SPEF2)基因,此基因编码精子鞭毛组装关键蛋白[4];断裂点6q13,靠近δ样蛋白1(DLL1)基因,DLL1作为Notch信号通路的关键配体,在精子发生中的作用尚未在现有文献中直接阐明。支持细胞可能通过分泌DLL1激活生殖细胞的Notch受体,调控精原干细胞分化或减数分裂进程。尽管尚无直接证据,但Notch通路在多种组织中的保守性提示其在精子发生中可能参与细胞间通路[5-6]。本例患者中这两个断裂点可能与精子发生调控有关,这也为患者严重少弱精子症临床表型原因增加了证据。
本例患者染色体核型涉及4个断裂点形成的三向易位,其减数分裂时可能形成六价体复合物。Pellestor等[7]通过大规模研究证实,CCRs的生殖风险与断裂点空间构象密切相关,根据该团队提出的“断裂点距离阈值理论”,当断裂点间距<10Mb时(如本例2q23与2q35相距约15Mb),染色体在减数分裂Ⅰ期可能发生异常折叠,从而显著增加相邻片段错误分离风险,CCRs产生不平衡配子的平均概率为80%左右,本文病例所获得的胚胎出现2/3异常胚胎率,与其结果相一致。
CCRs的来源仍不清楚,可能与电离辐射暴露、父亲高龄、妊娠前或妊娠期间使用免疫抑制药物以及母体染色体不稳定有关[8]。本例患者父母非近亲结婚,且父母染色体核型均正常,CCRs属于新发型,来源尚不确定。家系图谱详见图2。
以往认为与男性不育相关的染色体异常大多发生在性染色体上,但近年来不少学者认为常染色体的异常也可以导致精子的发生障碍[9]。在生殖细胞的发育进程中,常染色体出现畸变会对减数分裂产生阻碍,这种阻碍可能是完全的,也可能是部分的。
当初级精母细胞处于第一次减数分裂阶段时,同源染色体之间的互换概率会下降,同时在中变期,不对称的双价体、多价体以及单价体的数量会增加。这一系列变化会导致精子的生成过程在精母细胞阶段就陷入停滞,无法进一步分化为成熟的精子,进而对生精功能造成不良影响[10]。临床医生针对此类患者评估2~3次精液质量,确诊少弱精子症后,建议采集外周血进行染色体核型分析。男性生殖系统对于染色体异常更为敏感,因为精子发生过程涉及多次细胞分裂和染色体的精确分离。男性CCRs携带者的精子中,染色体不平衡的比例较高,使得自然受孕的几率大大降低,即使受孕,也容易出现胚胎发育异常和流产。传统的辅助生殖技术,如体外受精-胚胎移植(IVF-ET),对于CCRs携带者的助孕效果并不理想,因为这些技术无法对胚胎的染色体进行筛查,无法避免将染色体异常的胚胎移植入子宫,导致妊娠失败或不良妊娠结局。
PGT-SR是一种新兴的辅助生殖技术,它结合了体外受精和遗传学检测技术,在胚胎植入前对胚胎的染色体结构进行分析,筛选出染色体正常或平衡的胚胎进行移植,从而提高妊娠成功率,降低流产风险和染色体异常胎儿的出生率[11]。近年来,随着分子遗传学技术的不断发展,如二代测序技术(NGS)、单核苷酸多态性微阵列(SNP-array)等,PGT-SR的检测准确性和效率得到了显著提高[12-13]。既往研究表明,传统荧光原位杂交技术(FISH)对CCRs的检测存在近40%的假阴性率[7],这解释了为何本案例放弃常规FISH方案,转而采用全基因组SNP位点连锁分析法的策略,该改进使检测灵敏度显著提高。本例患者染色体异常比较少见,利用PGT-SR(SNP位点连锁分析法)技术成功获得一枚优质胚胎,并获得一健康后代。因此,男性CCRs患者建议行PGT-SR检测,有助于提高生育健康后代的几率。同时,由于CCRs临床表征为严重少弱精子症,采卵当天可能无法获得可用精子,建议提前冻存精子,以保证取卵当天有可用精子。
综上,基于SNP位点连锁分析法的PGT-SR技术,可以区分胚胎染色体是否携带与亲代相同的核型从而避免此类风险疾病的遗传[14-15]。本病例患者夫妇通过PGT-SR助孕成功获得了健康后代,提示该技术是CCRs携带者的有效助孕手段,同时避免了产前诊断的滞后性,是防止染色体疾病遗传后代的重要方法。针对CCRs患者,进行遗传咨询时,建议选择PGT-SR干预措施来选择优质胚胎,杜绝出生缺陷所带来的沉重负担。
本研究获得赤峰市妇产医院伦理委员会审查批准(伦理审批号:KY-2025-09-23-01)。
利益冲突 所有作者声明无利益冲突。
作者贡献 李耀辉负责资料收集与整理;李久洋负责技术支持、文章起草;焦泽华、韩少华负责行政、技术或材料支持;静双鹤、贾永强负责采集数据、分析数据;张明杰负责酝酿和设计实验以及文章的审阅、指导。
参考文献略。
来源:生殖医学杂志2026年3月第35卷第3期
