
CAR-T治疗的全程管理之桥接治疗(下篇)
嵌合抗原受体T细胞(CAR-T)治疗过程中在单采和清淋治疗之间存在一定的时间间隔,用于CAR-T细胞的制备。不同CAR-T产品的制备时间有所差异,约为3-8周1,2。有临床试验数据显示,大约7%的患者在等待CAR-T细胞制备完成时未能存活3,提示了桥接治疗的潜在重要性。本文综述了桥接治疗相关文献,包括桥接对疗效的影响、方案的选择及注意事项等。
一、桥接治疗对疗效的影响
桥接治疗的疗效在各种研究中并不统一(图1)。对这些患者的数据进行进一步分析,显示接受桥接治疗的患者,基线状态更差,存在明显选择偏倚。
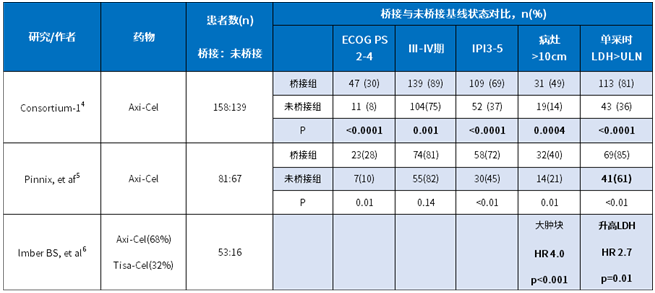
图1. 桥接治疗的研究汇总
二、桥接治疗方案的选择
桥接治疗方案包括化疗/免疫化疗、放疗、靶向治疗、激素治疗等,但在临床实践中,患者应遵循个体化治疗原则选择合适的桥接治疗方案。
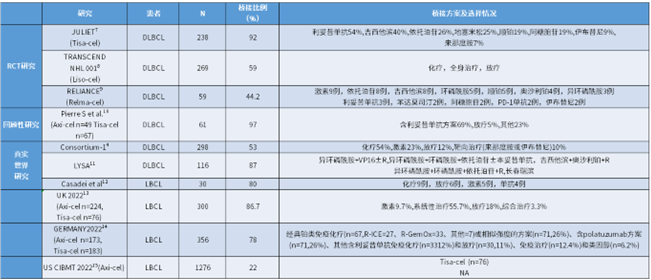
图2. 部分针对R/R LBCL的临床研究和真实世界研究所用的方案
研究显示,不同桥接方案治疗R/R LBCL患者,无进展生存期(PFS)和总生存期(OS)均无显著差异16,17。
另外,Pinnix CC.5报道了在R/R LBCL患者Axi-Cel治疗中使用不同桥接方案的疗效对比,研究发现相较于系统治疗,放疗桥接治疗患者的PFS有所改善 (P=0.05);相较于综合治疗,放疗桥接治疗患者的OS更优 (P=0.02)。
2.1不同类型桥接方案介绍
2.1.1 放疗桥接方案
Penny,Q.F通过对几项含放疗(RT)桥接放疗的回顾性研究以及一些早期研究进行了分析,在细胞治疗前考虑RT桥接治疗时,结合实际情况需注意:
• 放疗应尽可能在单采后进行,以尽量减少对T细胞适应性的影响;
• 如果可以安全地以最小毒性进行更全面的放疗,可能会有所帮助;
• 通常大分割方案安全可行,并可能重塑更有利的免疫微环境;从而降低类固醇方案的毒性18。
2.1.2 系统治疗桥接方案
在目前的临床研究和真实世界数据中,化疗联合的系统治疗是成人R/R LBCL中使用最广泛的桥接治疗方案,比例范围为38%-100%7-16,19。
一项回顾性研究纳入26个中心治疗的105例B细胞淋巴瘤患者的数据,其中41例患者在CAR-T细胞之前接受了(Polatuzumab Vedotin,下文简称Pola)作为桥接治疗。按预期接受CAR-T细胞的28名患者的6个月OS率为77.9%,12个月OS率为58.5%。在这些患者中,>50%的患者接受化疗联合Pola治疗。表明Pola单药或联合治疗是一种有价值的桥接治疗方案18。
在使用化疗/免疫化疗药物进行桥接治疗时,需要注意:
• 需要仔细确定可能受益于系统桥接化疗的患者亚组、方案的强度和CAR-T细胞输注前恢复的最佳时间20;
• 单独或联合使用化疗药物的患者随后将接受淋巴细胞清除治疗,并有发生特定CAR-T细胞相关并发症的风险,如细胞因子释放综合征 (CRS)、脑病和肿瘤溶解综合征。因此,理想情况下,桥接治疗不会引起严重并发症,例如感染、出血 或任何可能干扰计划中的淋巴清除疗法和CAR-T细胞输注的器官功能障碍21;
或任何可能干扰计划中的淋巴清除疗法和CAR-T细胞输注的器官功能障碍21;
• 接受桥接免疫治疗的患者是否应该接受靶向相同抗原的CAR-T细胞仍存在争议,ZUMA1中,Axi-Cel输注前排除经过抗CD19治疗的患者20;
• 有些桥接治疗也可能导致某些器官特异性毒性(例如蒽环类多柔比星 的心脏毒性或 CD22靶向抗体-药物偶联物inotuzumab ozogamicin的肝毒性),这可能会损害患者耐受CAR-T细胞输注后可能发生的CRS的能力20;
的心脏毒性或 CD22靶向抗体-药物偶联物inotuzumab ozogamicin的肝毒性),这可能会损害患者耐受CAR-T细胞输注后可能发生的CRS的能力20;
• 此外,还需常用桥接药物的主要不良反应谱(FDA label),在选择药物时要充分考虑药物的不良反应可能对后续CAR-T治疗造成的影响(图3)。
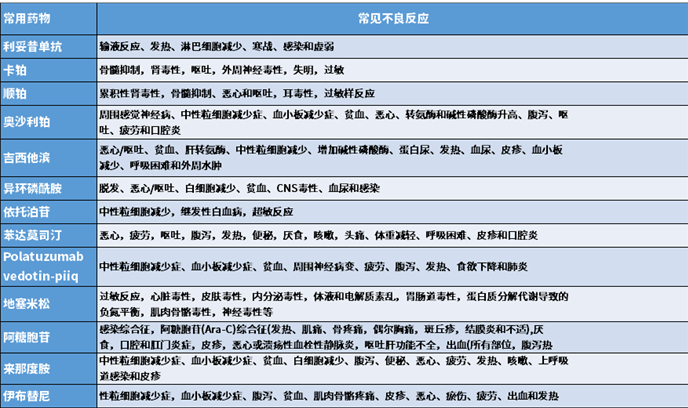
图3. 常用药物的常见不良反应汇总
总结
CAR-T细胞输注前的桥接治疗可用于高危患者,如高IPI评分、LDH升高、巨块型疾病等,以控制疾病进展19,21。不同桥接方案对疗效的影响存在争议,具体方案选择应遵循个体化原则。
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。
审批编号:NP-NHL-Axi-Cel-2023.02-24 valid until 2025.02
