
2025 ESMO前瞻|精准进阶,FLAURA2研究预后不良亚组OS结果即将重磅揭晓
前言
2025年欧洲肿瘤内科学会年会(ESMO)将于10月17日至21日在德国柏林召开。届时ESMO年会将公布众多前沿科研成果,共同促进临床肿瘤学的发展与进步。在肺癌领域,随着表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)的更新迭代,EGFR突变(Ex19del/L858R)晚期非小细胞肺癌(NSCLC)的一线治疗取得突破。但预后不良人群的治疗仍面临诸多挑战,如何优化一线治疗策略以满足这类人群的临床需求,已成为当前研究和临床实践的重点。2025 ESMO年会中,FLAURA2研究预后不良亚组的总生存期(OS)结果即将公布[1],有望为预后不良人群的一线治疗决策提供参考。
挑战尚存,
EGFR突变晚期NSCLC的临床困境
肺癌是我国及世界发病率和死亡率最高的恶性肿瘤,NSCLC约占85%[2]。与西方人群不同,亚裔肺腺癌人群的EGFR突变发生率高达40-60%[3]。随着靶向药物的发展,三代EGFR-TKI一线标准治疗已显著改善了EGFR突变(Ex19del/L858R)晚期NSCLC患者的预后[4]。然而,随着临床应用的深入,EGFR-TKI单药治疗在部分预后不良患者中暴露出一定的局限性,例如对于合并脑转移、L858R突变、TP53共突变或高肿瘤负荷等高危人群,单药治疗往往难以实现深度且持久的疾病控制,患者更易出现早期耐药和疾病进展。
既往研究显示,约20%的EGFR突变NSCLC患者在初诊时即存在脑转移,疾病全程中脑转移发生率可达50%[5]。而L858R突变是临床公认的较为难治的分子亚型,约占所有EGFR突变肺癌的40%[6]。TP53共突变是肺癌中最常见的伴随基因改变之一,EGFR突变晚期NSCLC患者中17.3%-72.5%存在 TP53 共突变,预后往往较差[7]。此外,高肿瘤负荷是晚期NSCLC患者的不良预后因素,初诊时高肿瘤负荷(≥3个转移部位)约占30%,其中肝转移和骨转移的发生率分别约为10%-20%和30%-40%[8]。这些不良因素常常相互叠加,进一步加剧了临床管理的复杂性与治疗难题。在此背景下,仅依赖EGFR-TKI单药治疗难以满足这类患者对长期生存和疾病控制的需求,临床亟需更优化的一线治疗策略以满足当前巨大的临床挑战。
一线优化,
三代EGFR-TKI联合化疗助力精准升级
临床前研究提示,EGFR-TKI联合化疗可通过增强对不同耐药细胞群的细胞杀伤能力来提高协同作用,克服肿瘤细胞的异质性,从而延缓耐药,进一步延长患者的PFS[9-10]。这一靶化联合治疗理念在临床试验中得到了验证。FLAURA2研究是全球首个探索三代EGFR-TKI联合化疗一线治疗EGFR突变晚期NSCLC的随机对照III期临床试验,评估了奥希替尼 联合含铂化疗对比奥希替尼单药作为EGFR突变(Ex19del/L858R)晚期NSCLC一线治疗的疗效和安全性,主要终点是由研究者评估的无进展生存期(PFS)[11]。结果显示,无论是研究者评估(25.5 vs 16.7个月;HR=0.62 ,95% CI 0.49-0.79,P<0.0001)还是盲法独立中央审查(BICR)评估(29.4 vs 19.9个月;HR=0.62,95% CI 0.48-0.80,P=0.0002),奥希替尼联合化疗组的PFS较奥希替尼单药组均延长约9个月,疾病进展或死亡风险下降38%(图1)。在安全性方面,奥希替尼联合化疗组和奥希替尼单药组任意级别不良事件(AE)发生率相近(100% vs 97%),联合治疗组治疗相关的≥3级AE发生率较高(53% vs 11%),奥希替尼联合化疗的整体安全性可控。
联合含铂化疗对比奥希替尼单药作为EGFR突变(Ex19del/L858R)晚期NSCLC一线治疗的疗效和安全性,主要终点是由研究者评估的无进展生存期(PFS)[11]。结果显示,无论是研究者评估(25.5 vs 16.7个月;HR=0.62 ,95% CI 0.49-0.79,P<0.0001)还是盲法独立中央审查(BICR)评估(29.4 vs 19.9个月;HR=0.62,95% CI 0.48-0.80,P=0.0002),奥希替尼联合化疗组的PFS较奥希替尼单药组均延长约9个月,疾病进展或死亡风险下降38%(图1)。在安全性方面,奥希替尼联合化疗组和奥希替尼单药组任意级别不良事件(AE)发生率相近(100% vs 97%),联合治疗组治疗相关的≥3级AE发生率较高(53% vs 11%),奥希替尼联合化疗的整体安全性可控。
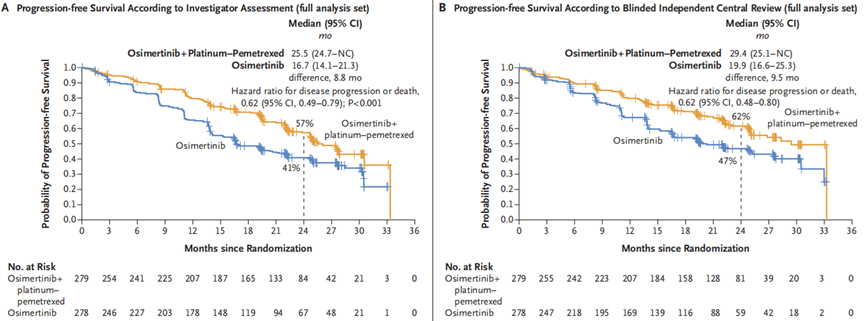
图1. 基于研究者和BICR评估的PFS结果
在EGFR-TKI单药一线治疗陷于瓶颈之际,FLAURA2研究的亚组分析结果显示,所有预后不良亚组均取得了一致性的PFS获益趋势。在伴脑转移的EGFR突变晚期NSCLC患者中,奥希替尼联合化疗可延长中位PFS约11个月(24.9 vs 13.8个月,HR=0.47,95% CI 0.33-0.66)[11]。针对EGFR L858R突变人群,奥希替尼联合化疗同样可延长中位PFS约11个月(24.7 vs 13.9个月,HR=0.63,95%CI 0.44-0.90)[11]。在基线高肿瘤负荷(≥3个转移部位)的患者中,奥希替尼联合化疗带来了PFS改善趋势(24.9 vs 16.4个月,HR=0.57,95% CI 0.43-0.77),同时靶化联合在伴中枢神经系统转移、肝转移及骨转移患者中均展现出一致的临床获益趋势[12]。此外,在TP53共突变的患者中,奥希替尼联合化疗同样观察到获益趋势(HR=0.57,95% CI 0.29-1.12)[13]。这些结果为靶化联合方案在多类预后不良人群中的应用提供了重要支持,有望进一步优化EGFR突变晚期NSCLC的个体化治疗体系。
此外,针对EGFR突变晚期NSCLC的其他靶化联合方案,如第三代EGFR-TKI阿美替尼 联合化疗方案也在EGFR突变晚期NSCLC患者的一线治疗中取得了成果,III期AENEAS2研究显示,阿美替尼联合化疗的中位PFS较阿美替尼单药显著改善(28.9 vs 18.9个月,HR=0.47,95% CI 0.37-0.60,P<0.0001)[14]。在安全性方面,两组≥3级AE的发生率分别为75.7%和23.7%,因AE导致阿美替尼停药的发生率分别为3.0%和1.3%。期待随着研究的进一步开展,更多高级别循证证据的涌现为EGFR-TKI联合化疗方案的临床应用注入信心,为预后不良的患者带来更深度和持久的获益。
联合化疗方案也在EGFR突变晚期NSCLC患者的一线治疗中取得了成果,III期AENEAS2研究显示,阿美替尼联合化疗的中位PFS较阿美替尼单药显著改善(28.9 vs 18.9个月,HR=0.47,95% CI 0.37-0.60,P<0.0001)[14]。在安全性方面,两组≥3级AE的发生率分别为75.7%和23.7%,因AE导致阿美替尼停药的发生率分别为3.0%和1.3%。期待随着研究的进一步开展,更多高级别循证证据的涌现为EGFR-TKI联合化疗方案的临床应用注入信心,为预后不良的患者带来更深度和持久的获益。
从PFS到OS,
一线EGFR-TKI联合化疗策略再添新证
在临床研究及实践中,OS一直是评估抗肿瘤药物疗效的“金标准”,尤其是在晚期肿瘤治疗中,OS的延长代表着患者真实且最终的临床获益,也是临床追求的最终目标。FLAURA2研究率先开启第三代EGFR-TKI联合化疗一线治疗的探索后,于2025 WCLC公布了最终OS结果[15]。研究显示,相较于奥希替尼单药,奥希替尼联合化疗的中位OS显著延长至47.5个月(vs 37.6个月,HR=0.77,95% CI 0.61-0.96,P=0.02,图2),且奥希替尼联合化疗在各个预设亚组(包括性别、种族、年龄、吸烟史、EGFR突变类型、体力状况及基线脑转移状态)中均展现出一致的获益趋势。此外,奥希替尼联合化疗组的安全性整体可控,在超过2年的额外随访中未观察到新的不良反应信号。在OS获益这一重要命题上,FLAURA2研究的长生存获益提供了首个EGFR-TKI联合化疗的III期高级别循证证据,进一步夯实了靶化联合策略的临床应match用价值。
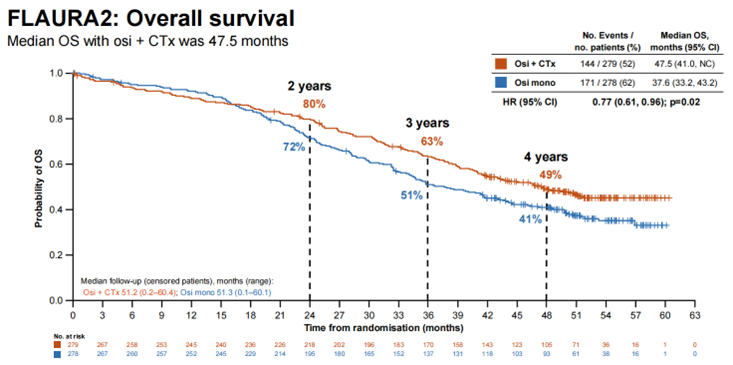
图2. FLAURA2研究OS结果(图片源自2025 WCLC)
在即将举行的2025 ESMO年会上,FLAURA2研究将继续公布具有预后不良因素亚组的OS结果(图3),有望进一步揭示预后不良人群的生存获益情况。期待这一数据的公布推动EGFR突变晚期NSCLC的一线治疗迈向基于分子特征和临床风险的精准分层,为EGFR突变晚期NSCLC的一线治疗决策提供更坚实的循证依据。

图3. FLAURA2研究预后不良亚组OS结果即将公布(图片源自2025 ESMO)
当然,临床也应理性认识FLAURA2研究的局限性,FLAURA2研究入组人群以PS评分良好、符合严格入排标准的患者为主,而真实世界中可能存在更多高龄及合并症复杂的患者,尚需进一步通过真实世界研究和前瞻性探索来验证这一靶化联合策略在更广泛人群中的适用性与长期获益。
本材料由阿斯利康提供,仅供医疗卫生专业人士参考
审批号:CN-169093
有效期:2026-01-09
参考文献
[1]Pasi A Jänne, et al. FLAURA2: exploratory overall survival (OS) analysis in patients with poor prognostic factors treated with osimertinib ± platinum-pemetrexed chemotherapy as first-line treatment for EGFR-mutated advanced NSCLC.2025 ESMO. LBA77.
[2]Qiu H, Cao S, Xu R. Cancer incidence, mortality, and burden in China: a time-trend analysis and comparison with the United States and United Kingdom based on the global epidemiological data released in 2020. Cancer Commun (Lond). 2021;41(10):1037-1048.
[3]Zhou Q, Zhao H, Lu S, et al. Consensus on the lung cancer management after third-generation EGFR-TKI resistance. Lancet Reg Health West Pac. 2024;53:101260.
[4]中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南. 2025版.
[5]Rangachari D, Yamaguchi N, VanderLaan PA, et al. Brain metastases in patients with EGFR-mutated or ALK-rearranged non-small-cell lung cancers. Lung Cancer. 2015. 88(1): 108-11.
[6]Harrison PT, Vyse S, Huang PH. Rare epidermal growth factor receptor (EGFR) mutations in non-small cell lung cancer. Semin Cancer Biol. 2020;61:167-179.
[7]Liu S, Yu J, Zhang H, Liu J. TP53 Co-Mutations in Advanced EGFR-Mutated Non-Small Cell Lung Cancer: Prognosis and Therapeutic Strategy for Cancer Therapy. Front Oncol. 2022;12:860563.
[8]Li Y, Zheng Z, Wang L, et al. Association of mutation profiles with metastasis in patients with non-small cell lung cancer. Front Oncol. 2024;14:1451576.
[9]Yang Z, Tam KY. Combination strategies using EGFR-TKI in NSCLC therapy: Learning from the gap between pre-clinical results and clinical outcomes. Int J Biol Sci. 2018;14(2):204-216.
[10]Rebuzzi SE, Alfieri R, Monica SL, et al. Combination of EGFR-TKIs and chemotherapy in advanced EGFR mutated NSCLC: Review of the literature and future perspectives. Crit Rev Oncol Hematol. 2020;146:102820.
[11]Planchard D, Jänne PA, Cheng Y, et al. Osimertinib with or without Chemotherapy in EGFR-Mutated Advanced NSCLC. N Engl J Med. 2023;389(21):1935-1948.
[12]N. Valdiviezo,et al. FLAURA2: Impact of Tumor Burden on Outcomes of 1L Osimertinib ± Chemotherapy in Patients with EGFR-mutated Advanced NSCLC. 2024 WCLC. MA12.04.
[13]J.C. Yang,et al. FLAURA2: Resistance, and Impact of Baseline TP53 Alterations in Patients Treated With 1L Osimertinib ± Platinum-Pemetrexed. 2024 WCLC. MA12.03.
[14]S Lu, et al. Aumolertinib with or without chemotherapy as first line treatment in locally advanced or metastatic NSCLC with sensitizing EGFR mutations (AENEAS2). 2025 AACR.CT053.
[15]D. Planchard,et al. First-Line Osimertinib + Chemotherapy Versus Osimertinib Monotherapy in EGFRm Advanced NSCLC: FLAURA2 Final Overall Survival.2025 WCLC. PL02.06.
