
研究解读:基于WES与ctDNA测序揭示内分泌治疗耐药乳腺癌的基因组进化图谱

激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)乳腺癌 在乳腺癌亚型中占比较高,但约20-40%的患者在接受辅助内分泌治疗后会发生复发或转移,且绝大多数转移性病例最终发展为耐药[1]。此前,发表在Breast Cancer Research and Treatment杂志的一项研究[2]中采用全外显子组测序(WES)技术,对配对的初治与复发部位肿瘤组织及胚系DNA进行了深度分析,并结合自研的336基因靶向二代测序技术对循环肿瘤DNA(ctDNA)进行检测,旨在全面绘制内分泌治疗耐药型与敏感型患者的基因组图谱,从而深入剖析治疗耐药的内在与获得性分子机制。
在乳腺癌亚型中占比较高,但约20-40%的患者在接受辅助内分泌治疗后会发生复发或转移,且绝大多数转移性病例最终发展为耐药[1]。此前,发表在Breast Cancer Research and Treatment杂志的一项研究[2]中采用全外显子组测序(WES)技术,对配对的初治与复发部位肿瘤组织及胚系DNA进行了深度分析,并结合自研的336基因靶向二代测序技术对循环肿瘤DNA(ctDNA)进行检测,旨在全面绘制内分泌治疗耐药型与敏感型患者的基因组图谱,从而深入剖析治疗耐药的内在与获得性分子机制。
本研究为单中心前瞻性研究,收集了经组织病理学证实为乳腺癌的患者的样本和数据,这些患者经免疫组化检测为ER和/或PR阳性,且经免疫组化或荧光原位杂交检测为HER2阴性。所有早期或局部晚期乳腺癌(LABC)患者均接受了标准根治性治疗,包括手术,联合或不联合(新)辅助化疗、放疗(如有指征)以及辅助内分泌治疗。如果患者在开始内分泌治疗后至少2年内无复发,则被归类为内分泌治疗敏感型。采集了这些患者诊断时的血液、口腔拭子样本和先前存档的肿瘤组织。如果在内分泌治疗期间出现疾病进展或在开始内分泌治疗2年内出现疾病复发,则患者被归类为内分泌治疗耐药型疾病。同样收集了这些患者的血液、口腔拭子和最易获取的复发部位的肿瘤组织(图1)。
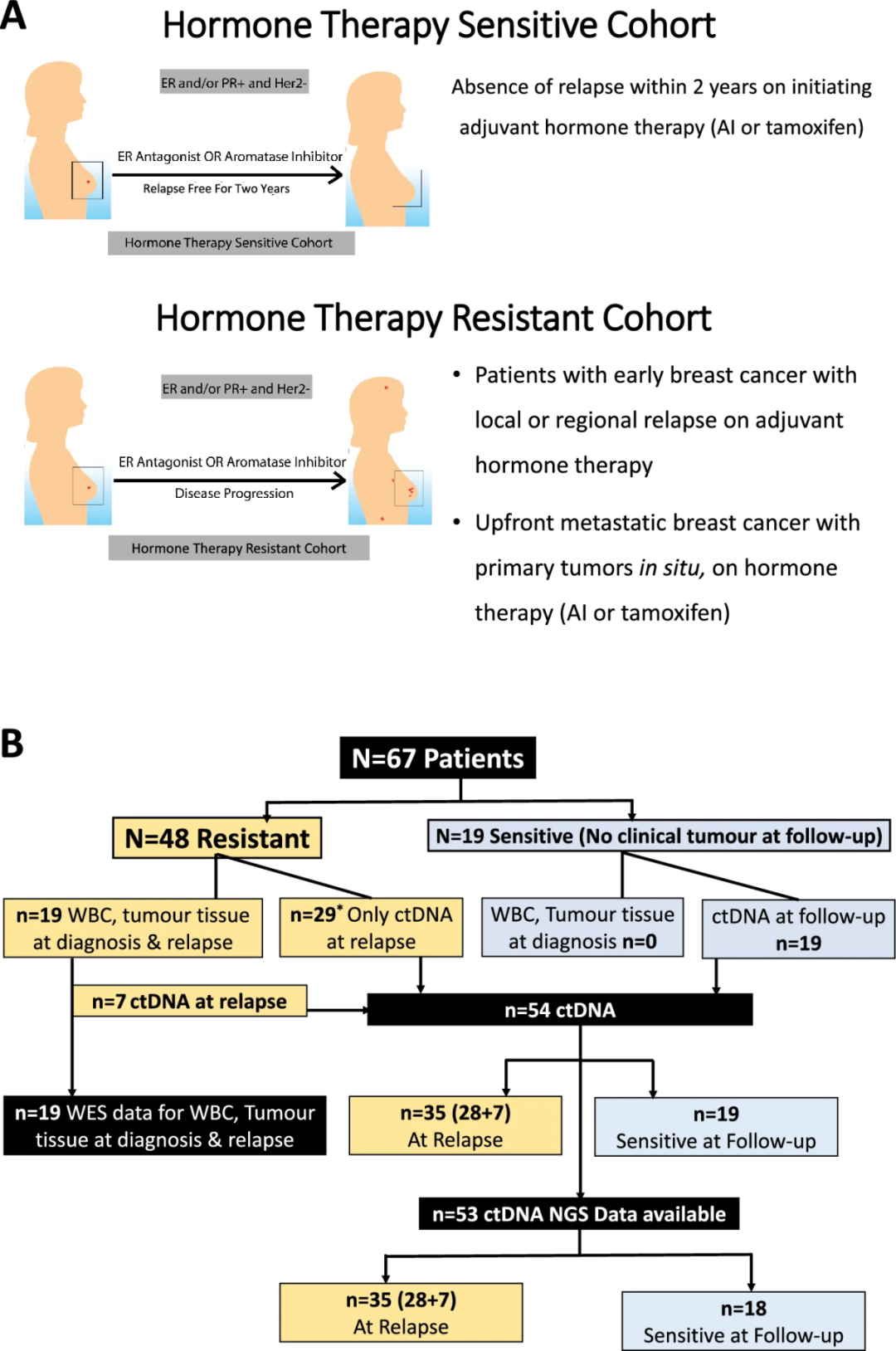
图1. 研究设计和患者招募流程图[2]
分析纳入了2017年至2023年间招募的334例患者,其中135例患有内分泌治疗耐药型疾病,199例患有内分泌治疗敏感型疾病。在这334例患者中,有298例患者(耐药119,敏感179)可获得血浆样本,其中254例患者(耐药116,敏感138)检测到血浆核酸。254例患者中的250例(耐药116,敏感134)检测到细胞游离DNA(cfDNA,定义为50-700bp)。250例患者中的136例(耐药116,敏感24)检测到ctDNA(定义为50-350bp),其中118例患者(耐药98,敏感20)其50%的cfDNA片段长度介于50-350bp之间,表明ctDNA富集。内分泌治疗耐药型患者中ctDNA的检出率更高,116例耐药患者中有98例(84.5%)检测到ctDNA,而138例内分泌治疗敏感型患者中仅有20例(14.5%)检测到。
19例内分泌治疗耐药型患者拥有配对体细胞样本(初治和复发肿瘤)的WES数据,其中7例耐药患者同时拥有可用的ctDNA NGS数据。因此,最终分析集包含66例患者(耐药47,敏感19)的NGS数据,包括12例仅有配对体细胞组织的耐药患者,28例仅有ctDNA数据的耐药患者,7例同时拥有配对体细胞组织和ctDNA数据的耐药患者,以及19例仅有ctDNA数据的敏感患者。
所有患者均为女性,中位年龄51(27-70)岁,从入组到最后一次随访的中位随访时间为57个月。耐药组患者 vs. 敏感组患者,在样本采集时的III级肿瘤比例(76.5% vs. 47.1%)和IV期疾病比例(39% vs. 2%)更高。除1例在初次就诊时即患有原发性转移性疾病且伴有多器官转移的患者外,所有患者均接受了根治性手术。内分泌治疗耐药型疾病患者在样本采集时已接受了中位数为三线的系统治疗。5例患者曾接受过CDK4/6抑制剂治疗。在绝经前亚组中,8例患者接受了卵巢功能抑制。
总体而言,治疗后复发肿瘤的突变率(中位数0.883突变/mb,范围0.51–3.41)高于初治诊断肿瘤(中位数0.655突变/mb,范围0.31–2.09)(p值0.03)。
针对19例患者的38个肿瘤样本(包括初治和复发部位组织),在1608个基因中识别了1886个独特的体细胞变异,其中1562个基因中的1810个突变被注释为具有功能影响。经欧洲肿瘤内科学会分子靶点临床可操作性量表(ESCAT)分析,将1810个突变中的64个注释为已确认的驱动突变(图2)。初治样本中驱动突变的中位数为2个,复发肿瘤中为3个;31个驱动突变同时存在于初治和复发部位样本中,12个突变在复发时丢失,而21个驱动突变在复发时获得,包括ESR1、PIK3R2、ATR、EZH2和POLE等基因中的潜在可靶向改变。

图2. ESCAT分析确定的19例内分泌治疗耐药患者的可靶向驱动突变[2]
内分泌治疗耐药患者的初治肿瘤样本呈多克隆性,突变负荷各异(图3),由一个原始克隆分化为亚克隆(图4)。这种“分支进化”模式在18例(94.7%)患者中观察到。其余1例(5.3%)患者的初治肿瘤为双克隆,并在复发时保持不变。我们根据原始克隆中是否存在PIK3CA和/或TP53突变对患者进行分类。13例(68.4%)患者的原始克隆携带PIK3CA或TP53突变,或两者兼有。A组患者包括3例(15.8%)原始克隆中同时存在TP53和PIK3CA突变的患者(图4A),这些患者的原始克隆中缺乏其他驱动突变,表明PIK3CA和TP53突变在其整个临床过程中且持续存在,驱动治疗耐药。这3例患者中的1例(5.3%)(P038R)在复发时获得了ESR1突变(p.Y537S)。B组患者包括3例(15.8%)仅携带TP53突变且无PI3K通路突变的患者(图4B)。这些患者的原始克隆中有额外的GATA3、RAD54和AMER1突变。C组包含8例(42.1%)患者,其原始克隆中仅有PIK3CA突变,而无TP53突变(图4C)。其中5例(26.3%)患者的原始克隆中存在其他原癌基因(JAG1、RAF1、KRAS和FOXA1)的额外突变;2例(10.5%)患者存在DNA损伤修复(DDR)基因(RAD18、XRCC5)、原癌基因(MAP3K21、MAP2K5、PDGFRL)和抑癌基因(PTEN)的突变;1例(5.3%)患者存在ESR2突变(R220W);1例(5.3%)患者在复发时获得了两个TP53突变(R141C和E66X)。D组包含5例(26.3%)患者,其原始克隆中缺乏TP53或PIK3CA突变(图4D),但存在FOXA2、NOTCH1、PTEN、GATA3、MEN1、FRG1和MAP3K等已知驱动突变。2例(10.5%)D组患者的复发部位肿瘤组织获得了一个ESR1热点突变。此外,在2例(10.5%)患者(P080R和P069R)中,原始克隆中未发现任何已知的驱动突变。
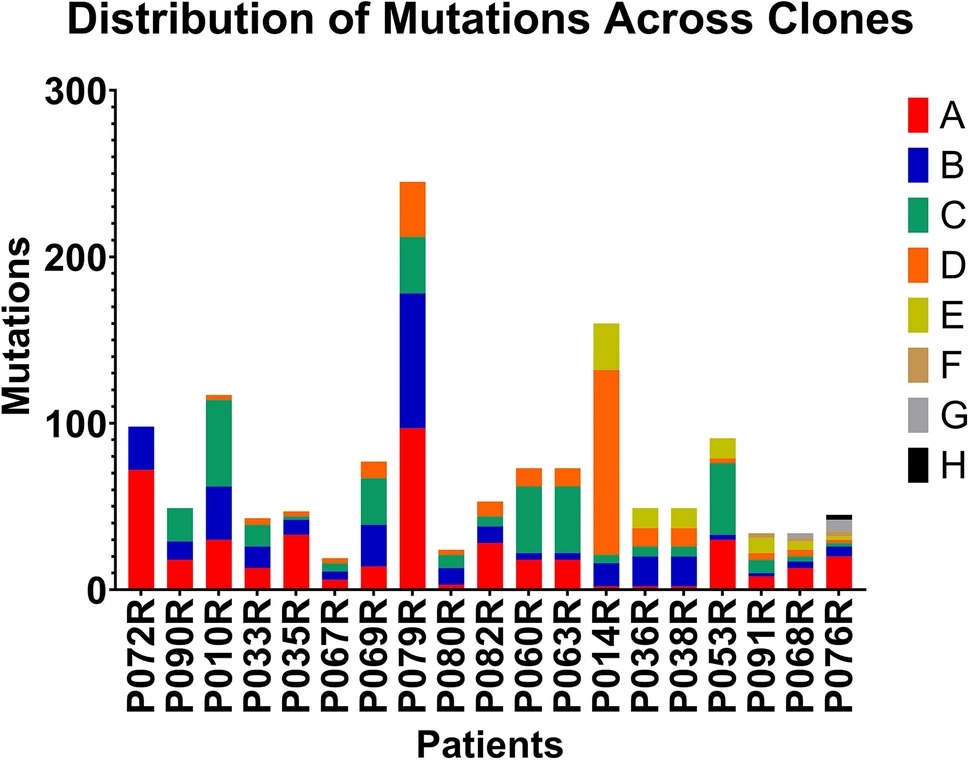
图3. 19例患者配对初治和复发部位组织活检WES数据中各克隆的突变分布[2]
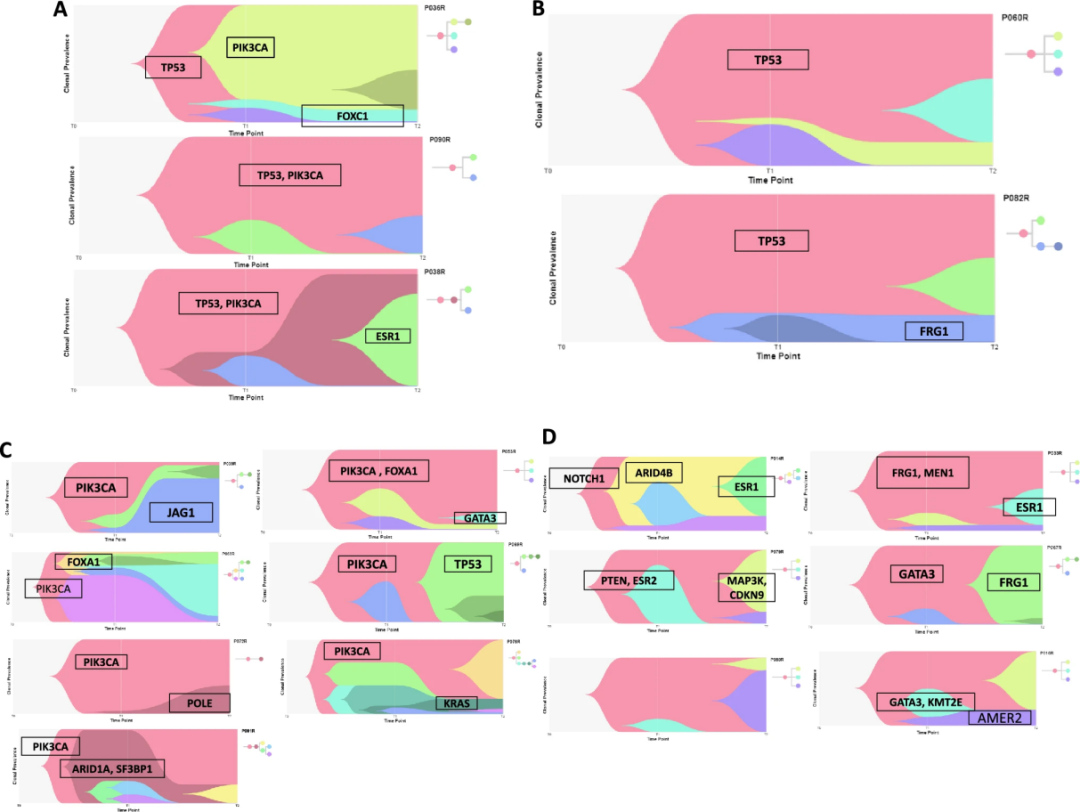
图4. 18例具有初治和复发部位组织活检WES数据患者的克隆图谱[2]
在54例具有ctDNA NGS数据(耐药35,敏感19)的患者中,53例(耐药35,敏感18)至少有一个变异通过了硬过滤(根据一定的逻辑原则,对注释结果中特定列信息进行筛选,通常为阈值或类筛选,尽可能缩小候选变异范围),共有23,113个独特变异。其中12,761个为同义突变或被注释为“未知”,因此从进一步分析中剔除;而10,352个被注释为“非同义”、“移码”、“终止缺失”或“终止获得”的变异被进一步分析。其中,805个在单核苷酸多态性(dbSNP)数据库和癌症体细胞突变目录(COSMIC)中均不存在,表明它们可能是种族特异性的胚系多态性;而2328个变异仅存在于dbSNP中,表明它们是胚系多态性。在这2328个可能的胚系多态性中,11/54(20.4%)例患者在7个基因(BRCA1、CHEK2、MLH3、MMP9、SOX2、AR和ZFHX3)中的变异被注释为致病性或可能致病性。在10,352个变异中,7219个存在于COSMIC中,其中6969个被注释为“良性”、“可能良性”或“致病性不确定”,被排除在进一步分析之外;而53例患者中7219个变异里的250个被注释为“致病性”或“可能致病性”,并进行了进一步分析。在这250个变异中,170个出现在超过30例患者中,表明它们可能是多态性,因此从进一步分析中排除。
在剩余80个致病变异中,有22个基因的42个独特变异存在于35例内分泌治疗耐药患者中的32例中。在这35例患者中,15例(42.9%)有PIK3CA热点突变,9例(25.7%)有TP53热点突变,3例(8.6%)两者皆有。ESCAT分析确定,42个变异中有12个基因的27个变异在25例(71.4%)耐药患者中是可靶向的。耐药患者中任意可靶向的驱动改变包括PIK3CA p.H1047X、AKT1 p.E17K、CDH1 p.R63X、CDKN2A p.X50*、ERBB2 p.D769Y、ESR1 p.E380Q、GATA3 p.R367X、KRAS p.G12A、KRAS p.G12D、PTEN p.D24H和SF3B1 p.K700E。
在19例内分泌治疗敏感患者中,10例(52.6%)中发现了8个基因的10个独特致病变异。3例(15.8%)出现PIK3CA热点突变,1例(5.3%)出现TP53热点突变。通过ESCAT分析,这10个变异中有3个基因的4个变异在6例敏感患者中被确定为驱动突变,包括PIK3CA p.H1047X和KRAS p.G12A。
因此,总体而言,这54例患者中有31例(耐药27,敏感4,57.4%)携带PIK3CA或TP53突变,其中28例(耐药25,敏感3,51.9%)患者可见潜在的可靶向改变。
在ctDNA分析中,3例(耐药1,敏感2,5.6%)患者携带致病性BRCA1变异,而1例(1.9%)耐药患者携带致病性BRCA2变异。一例敏感患者的一个致病性BRCA1变异仅标注了dbSNPID,表明这可能是一个胚系变异;该患者也报告了乳腺癌家族史。其他两个BRCA1变异(耐药1,敏感1)和耐药患者中唯一的BRCA2变异也存在于COSMIC数据库中,表明它们可能是体细胞或胚系变异,由于缺乏口腔拭子DNA作为胚系对照,无法确认。
在19例内分泌治疗敏感患者(采血时影像学和临床均无病)中的10例(52.6%)的ctDNA中检测到了TP53、KRAS、PIK3CA、BRCA1、SF3B1、AR、MSH6和MEN1的已知驱动突变。在这10例患者中,8例在分析时存活且无病,其他2例中一例携带已知的MEN1致病突变,另一例携带PIK3CA和KRAS两个驱动突变,经历了疾病复发并死亡。在9例ctDNA分析中未发现任何已知驱动突变的患者中,1例失访,其余8例(占无驱动突变者的88.9%)在分析时存活且无病。
7例患者拥有配对(初治和复发部位)体细胞肿瘤组织及复发时ctDNA的NGS数据。体细胞组织中共有1608个独特基因发生突变,其中59个基因包含在靶向ctDNA面板中。在7例(100%)患者的肿瘤组织中,有7个基因通过ESCAT分析检测出10个驱动突变。在1例(14.3%)患者中,2个驱动突变仅在初治样本中检测到,而在复发部位组织和ctDNA中缺失;在2例(28.6%)患者中,2个驱动突变仅在复发部位组织中检测到,而在复发时的ctDNA中缺失;在1例(14.3%)患者中,1个驱动突变在复发部位组织和复发时的ctDNA中均被检测到;在4例(57.1%)患者中5个驱动突变(均存在于这些患者的原始克隆中)在初治和复发部位组织以及复发时的ctDNA中均被检测到。患者P068R和P038R原始克隆中的FOXA1和ESR1驱动突变未在相应的ctDNA样本中识别出来。
总体而言,研究共纳入66例(耐药47,敏感19)具有可分析NGS数据的患者,其中在47例(耐药40,敏感6,71.2%)患者的至少一种检测(WES或ctDNA,图5)中识别出16个基因的47个独特的可靶向驱动突变。

图5. ESCAT分析确定的66例患者(结合WES和ctDNA数据)的可靶向驱动突变[2]
在47例内分泌治疗耐药患者中,6例(12.7%)同时具有PIK3CA和TP53热点突变,14例(29.7%)仅有PIK3CA突变,4例(8.5%)仅有TP53突变。因此,24例(51.1%)内分泌治疗耐药患者携带PIK3CA或TP53突变,5例(10.6%)耐药患者携带ESR1突变,2例(4.3%)耐药患者各携带PTEN、CDKN2A或KRAS突变,而各有一例(2.1%)耐药患者携带BRCA1、BRCA2、SF3B1、ERBB2、AKT1或ATR突变。
在19例内分泌治疗敏感患者中,没有患者同时具有TP53和PIK3CA突变,4例(21.1%)仅有PIK3CA突变,3例(15.8%)仅有TP53突变。总体而言,在66例患者的整个队列中,6例(9.1%)具有PIK3CA和TP53基因突变,18例(27.3%)患者仅有PIK3CA突变,7例(10.6%)患者仅有TP53突变。
本研究通过对内分泌治疗耐药及敏感乳腺癌患者进行WES和高深度ctDNA测序,揭示了耐药肿瘤在诊断及复发时表现为多克隆特征,并遵循分支进化模式。研究发现,包含TP53和/或PIK3CA突变的原始克隆可能共存并持续存在,其中TP53突变可能足以驱动转移克隆的播种,而PIK3CA突变往往需协同其他基因改变以促进增殖;相比之下,ESR1突变主要在复发时获得。临床转化方面,71%的耐药患者在复发时的ctDNA中存在可靶向突变,且激素敏感型患者ctDNA中驱动突变的检出与复发风险显著相关,证实了液体活检在指导精准治疗及疾病监测中的重要价值,尤其适用于难以进行组织活检的病例。
技术层面上,10,000×深度的ctDNA测序对识别TP53、PIK3CA等原始克隆驱动突变具有高灵敏度,但在捕获复发时低频亚克隆突变(如ESR1)方面可能存在局限,未来更高深度(50,000×–100,000×)的测序可能有助于更全面地评估突变负荷。尽管本研究在样本量和部分配对数据上存在一定局限,但基于临床表型明确的队列分析,强调了早期靶向原始克隆的重要性,并表明中等覆盖度的ctDNA测序虽不能完全替代组织检测,但作为一种极具潜力的非侵入性工具,能有效提供关键的临床基因组信息。
参考文献
1.Ghosh A, et al. Genomic hallmarks of endocrine therapy resistance in ER/PR+HER2- breast tumours. Commun Biol. 2025;8(1):207.
2.Chaubal R, et al. Genomic landscape of hormone therapy-resistant HR-positive, HER2-negative breast cancer. Breast Cancer Res Treat. 2025;213(2):247-259.
审批编号:CN-178599
有效期至:2027-02-05
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
