
当EGFR遇上TP53突变:肺癌遭遇"双重打击"下的治疗挑战与临床探索

TP53是人类肿瘤中最常发生突变的抑癌基因之一,在非小细胞肺癌 (NSCLC)中亦具有重要的生物学与临床意义。既往研究显示,表皮生长因子受体(EGFR)突变晚期NSCLC患者中约40%-65%存在TP53共突变,且与更具侵袭性的疾病特征及较差的临床预后相关。随着精准治疗时代的到来,如何针对EGFR-TP53共突变这一预后不良人群优化一线治疗策略,已成为当前临床研究的重要方向。
(NSCLC)中亦具有重要的生物学与临床意义。既往研究显示,表皮生长因子受体(EGFR)突变晚期NSCLC患者中约40%-65%存在TP53共突变,且与更具侵袭性的疾病特征及较差的临床预后相关。随着精准治疗时代的到来,如何针对EGFR-TP53共突变这一预后不良人群优化一线治疗策略,已成为当前临床研究的重要方向。
1979年,纪念斯隆·凯特琳 癌症中心Lloyd Old团队鉴定出一种识别53 kDa肿瘤抗原的肿瘤特异性抗体,并将其命名为p53。同年,另两个研究团队独立报道:在致癌病毒SV40转化的细胞中,一种53或54 kDa宿主蛋白是癌蛋白大T抗原的结合伴侣。我们现在已知,这一宿主蛋白与p53肿瘤抗原实为同一物质。在随后十年中,p53在肿瘤发生中的确切作用尚不明确,但1989年约翰·霍普金斯大学Bert Vogelstein团队发现,TP53(编码p53的基因)在人类癌症中常发生突变。携带TP53突变等位基因的出生者患有Li-Fraumeni综合征,并在年轻时发生癌症;p53基因敲除小鼠同样出现早发性肿瘤。这些发现确立了p53在癌症中的抑癌功能,此后数十年的研究证实,TP53是人类癌症中最常突变的基因之一[1]。
癌症中心Lloyd Old团队鉴定出一种识别53 kDa肿瘤抗原的肿瘤特异性抗体,并将其命名为p53。同年,另两个研究团队独立报道:在致癌病毒SV40转化的细胞中,一种53或54 kDa宿主蛋白是癌蛋白大T抗原的结合伴侣。我们现在已知,这一宿主蛋白与p53肿瘤抗原实为同一物质。在随后十年中,p53在肿瘤发生中的确切作用尚不明确,但1989年约翰·霍普金斯大学Bert Vogelstein团队发现,TP53(编码p53的基因)在人类癌症中常发生突变。携带TP53突变等位基因的出生者患有Li-Fraumeni综合征,并在年轻时发生癌症;p53基因敲除小鼠同样出现早发性肿瘤。这些发现确立了p53在癌症中的抑癌功能,此后数十年的研究证实,TP53是人类癌症中最常突变的基因之一[1]。
TP53基因编码抑癌蛋白p53,与其他抑癌基因类似,肿瘤发生通常需要两个等位基因均丧失功能(即两次"打击")。野生型p53蛋白 半衰期短且表达水平低,而突变型p53通常半衰期延长并在癌细胞中积累。p53蛋白是一种转录因子,通过结合并激活特定靶基因来控制数百个下游基因的表达,从而发挥抑癌作用;突变型p53因无法结合并激活靶基因,其抑癌功能明显减弱或丧失[1]。
半衰期短且表达水平低,而突变型p53通常半衰期延长并在癌细胞中积累。p53蛋白是一种转录因子,通过结合并激活特定靶基因来控制数百个下游基因的表达,从而发挥抑癌作用;突变型p53因无法结合并激活靶基因,其抑癌功能明显减弱或丧失[1]。
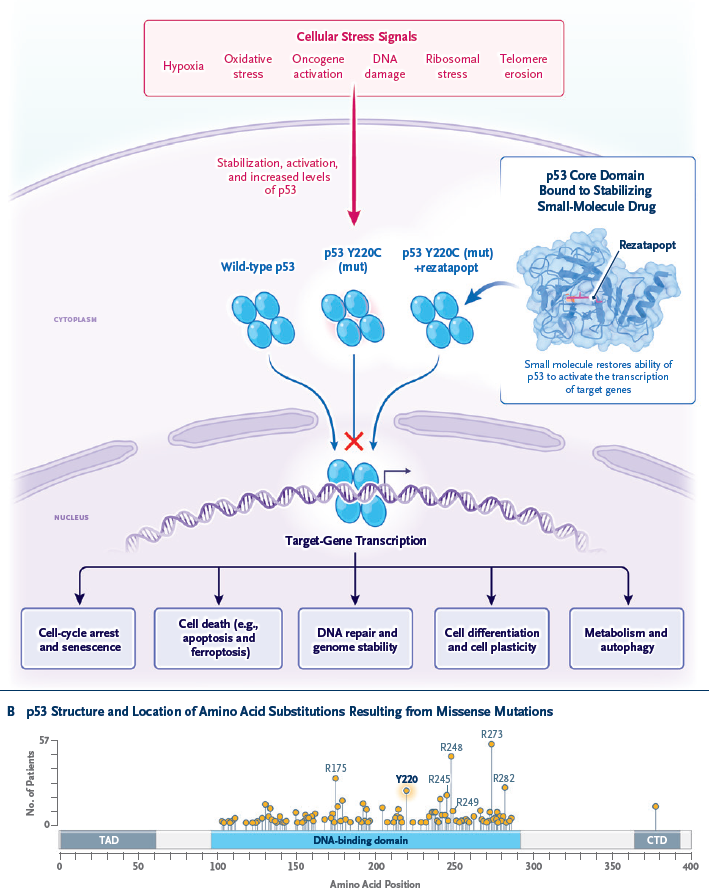
图. P53的功能与结构
当p53作为"基因组守护者"的功能因突变而瓦解,其介导的细胞周期阻滞与凋亡能力显著受损。这一缺陷在肿瘤驱动基因EGFR突变NSCLC中尤为致命。既往研究显示,约40%-65%的EGFR突变NSCLC患者存在TP53共突变[2-4]。这种EGFR-TP53共突变形成"双重打击"效应,即EGFR信号持续激活肿瘤细胞增殖,而p53失活则削弱了细胞对致癌应激的防御屏障。
此外,在EGFR突变NSCLC的特定高危亚组中,TP53共突变的发生率通常较高[5]。同时,TP53共突变可能与更具侵袭性的临床特征相关。在EGFR L858R突变人群中,TP53突变患者的脑转移(BM)发生率显著高于TP53野生型患者(59.1% vs 37.0%,P=0.016),提示EGFR-TP53共突变可能与更高的中枢神经系统转移风险相关[6]。
EGFR-TP53共突变的晚期NSCLC患者的预后往往更差。既往研究表明,携带EGFR-TP53共突变的NSCLC患者较TP53野生型患者具有更高的疾病进展和死亡风险,TP53突变与较短的无进展生存期(PFS)(HR=1.51,95% CI 1.33-1.71,P<0.001)和总生存期(OS)(HR=1.64,95% CI 1.33-2.02,P<0.001)显著相关[7]。真实世界研究亦显示,EGFR-TP53共突变患者的PFS和OS显著低于TP53野生型(PFS HR=1.4,P=0.0196;OS HR=1.6,P=0.0088)[8]。进一步分析发现,EGFR-TKI单药在这一人群中的疗效亦相对有限。既往研究表明,EGFR-TP53共突变患者接受EGFR-TKI单药治疗的临床获益欠佳,中位PFS仅为6.5-11.2个月,中位OS仅为21-28个月[9]。
值得注意的是,TP53共突变是EGFR突变NSCLC患者的独立不良预后因素,与TP53突变类型无关。研究表明,无论TP53突变发生于何种突变类型(如错义突变与非错义突变)或功能亚型(如破坏性与非破坏性突变),TP53共突变均与EGFR突变NSCLC较差的预后相关[9]。上述结果提示,该预后不良人群仍存在显著未满足的治疗需求。
联合治疗与精准检测并行,
探索EGFR-TP53共突变治疗新路径
在此背景下,通过联合治疗强化疗效逐渐成为重要探索方向。近年来,EGFR-TKI联合治疗策略取得的进展为EGFR-TP53共突变晚期NSCLC患者带来了治疗希望。FLAURA2研究显示,相较于奥希替尼 单药,奥希替尼联合培美曲塞
单药,奥希替尼联合培美曲塞 和含铂化疗一线治疗EGFR突变(Ex19Del/L858R)晚期NSCLC显著改善了PFS和OS(PFS HR=0.62,95% CI 0.49-0.79,P<0.0001;OS HR=0.77,95% CI 0.61-0.96,P=0.02)[10]。对于EGFR-TP53共突变患者,FLAURA2研究探索性分析显示,奥希替尼联合化疗组对比单药组显示出降低疾病进展和死亡风险的趋势(PFS HR=0.57,95% CI 0.29-1.12)[11];中位OS为51.1个月vs 43.1个月(HR=0.71,95% CI 0.40-1.27)[12]。此外,MARIPOSA研究显示,埃万妥单抗
和含铂化疗一线治疗EGFR突变(Ex19Del/L858R)晚期NSCLC显著改善了PFS和OS(PFS HR=0.62,95% CI 0.49-0.79,P<0.0001;OS HR=0.77,95% CI 0.61-0.96,P=0.02)[10]。对于EGFR-TP53共突变患者,FLAURA2研究探索性分析显示,奥希替尼联合化疗组对比单药组显示出降低疾病进展和死亡风险的趋势(PFS HR=0.57,95% CI 0.29-1.12)[11];中位OS为51.1个月vs 43.1个月(HR=0.71,95% CI 0.40-1.27)[12]。此外,MARIPOSA研究显示,埃万妥单抗 联合兰泽替尼治疗也可降低疾病进展或死亡风险(HR=0.65,95% CI 0.48-0.87)[13]。上述结果初步展示了联合治疗模式在EGFR-TP53共突变晚期NSCLC中的治疗潜力。然而,目前针对该人群的循证医学证据仍相对有限,临床实践仍亟需更具针对性的研究进一步明确治疗策略。
联合兰泽替尼治疗也可降低疾病进展或死亡风险(HR=0.65,95% CI 0.48-0.87)[13]。上述结果初步展示了联合治疗模式在EGFR-TP53共突变晚期NSCLC中的治疗潜力。然而,目前针对该人群的循证医学证据仍相对有限,临床实践仍亟需更具针对性的研究进一步明确治疗策略。
值得关注的是,精准治疗检测先行。既往研究中,TP53检测的方法包括ARMS、NGS及PCR等,检测样本可来源于肿瘤组织或外周血循环肿瘤DNA(ctDNA)。然而,目前针对TP53突变的检测策略尚无统一标准。《NCCN非小细胞肺癌临床实践指南(2026.V5)》建议,对于晚期或转移性NSCLC患者,在治疗初期须开展多基因panel检测,以全面评估EGFR等关键驱动基因及共突变情况,从而为精准治疗决策提供依据[14]。
为了进一步明确EGFR-TKI联合治疗模式对EGFR-TP53共突变患者的获益,TOP研究进行了探索。这是一项III期随机开放标签试验,纳入携带EGFR突变(Ex19del/L858R)和TP53突变的晚期非鳞状NSCLC患者,体能状态(PS)0-1分,计划接受一线治疗。符合条件患者按1:1随机分配至奥希替尼单药组(奥希替尼80 mg每日口服)或联合治疗组(奥希替尼80 mg每日口服+培美曲塞500 mg/m²+卡铂 AUC 5静脉给药,每3周一次共4周期,后续予培美曲塞和奥希替尼维持治疗)。随机分组按PS评分(0 vs 1)、脑转移状态(是 vs 否)和突变类型(Ex19del vs L858R)分层。主要终点为研究者评估的RECIST 1.1标准PFS。次要终点包括总生存期、客观缓解率、缓解持续时间、不良事件及生活质量。探索性终点为TP53外共突变与疗效的相关性,以及动态ctDNA分析揭示的联合治疗耐药机制[15]。
AUC 5静脉给药,每3周一次共4周期,后续予培美曲塞和奥希替尼维持治疗)。随机分组按PS评分(0 vs 1)、脑转移状态(是 vs 否)和突变类型(Ex19del vs L858R)分层。主要终点为研究者评估的RECIST 1.1标准PFS。次要终点包括总生存期、客观缓解率、缓解持续时间、不良事件及生活质量。探索性终点为TP53外共突变与疗效的相关性,以及动态ctDNA分析揭示的联合治疗耐药机制[15]。
该研究设计已于2024 ASCO大会公布,其关键研究结果即将在2026 ELCC大会首次发布,有望为EGFR-TP53共突变晚期NSCLC患者的一线治疗提供新的循证依据。

图. 2026 ELCC:TOP研究
参考文献(向上滑动查看):
[1] Lu X. Restoring Function to a Variant of p53 in Solid Tumors. N Engl J Med. 2026;394(9):922-925.
[2] Guo Y, Song J, Wang Y, et al. Concurrent Genetic Alterations and Other Biomarkers Predict Treatment Efficacy of EGFR-TKIs in EGFR-Mutant Non-Small Cell Lung Cancer: A Review. Front Oncol. 2020;10:610923.
[3] Blakely CM, Watkins TBK, Wu W, et al. Evolution and clinical impact of co-occurring genetic alterations in advanced-stage EGFR-mutant lung cancers. Nat Genet. 2017;49(12):1693-1704.
[4] Skoulidis F, Heymach JV. Co-occurring genomic alterations in non-small-cell lung cancer biology and therapy. Nat Rev Cancer. 2019 Sep;19(9):495-509.
[5] Jiao XD, He X, Qin BD, et al. The prognostic value of tumor mutation burden in EGFR-mutant advanced lung adenocarcinoma, an analysis based on cBioPortal data base. J Thorac Dis. 2019;11(11):4507-4515.
[6] Wei L, Lao Y, Fu T, et al. Distinct Role of TP53 Co-mutations in Different EGFR Subtypes Mediating the Response to EGFR Tyrosine Kinase Inhibitors in Non-Small Cell Lung Cancer. Clin Lung Cancer. 2025;26(6):478-491.e7.
[7] Lan B, Zhao N, Du K, Leng B. Concurrent TP53 mutations predict a poor prognosis of EGFR-mutant NSCLCs treated with TKIs: An updated systematic review and meta-analysis. Oncol Lett. 2022 Sep 15;24(5):384.
[8] Le X, Molife C, Leusch MS, et al. TP53 Co-Mutation Status Association with Clinical Outcomes in Patients with EGFR-Mutant Non-Small Cell Lung Cancer. Cancers (Basel). 2022;14(24):6127.
[9] Liu S, Yu J, Zhang H, Liu J. TP53 Co-Mutations in Advanced EGFR-Mutated Non-Small Cell Lung Cancer: Prognosis and Therapeutic Strategy for Cancer Therapy. Front Oncol. 2022 Apr 4;12:860563.
[10] Jänne PA, Planchard D, Kobayashi K, et al. Survival with Osimertinib plus Chemotherapy in EGFR-Mutated Advanced NSCLC. N Engl J Med. 2026;394(1):27-38.
[11] J.C. Yang,et al. FLAURA2: Resistance, and Impact of Baseline TP53 Alterations in Patients Treated With 1L Osimertinib ± Platinum-Pemetrexed. 2024 WCLC. MA12.03.
[12] Pasi A. Jänne, et al, FLAURA2: exploratory overall survival analyses in patients with poorer prognostic factors treated with osimertinib ± platinum–pemetrexed as first-line treatment for EGFR-mutated advanced NSCLC. 2025 ESMO. LBA77.
[13] Felip E, Cho BC, Gutiérrez V, et al. Amivantamab plus lazertinib versus osimertinib in first-line EGFR-mutant advanced non-small-cell lung cancer with biomarkers of high-risk disease: a secondary analysis from MARIPOSA. Ann Oncol. 2024;35(9):805-816.
[14] NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®). Non Small Cell Lung Cancer. Version 5. 2026.
[15] Yunpeng Yang, et al. TOP:A phaseIII,multicentre,randomized controlled study comparing Osimertinib in combination with carboplatin and pemetrexed to osimertinib monotherapy for untreated patients with advanced non-squamous (Non-sq) non-small cell lung cancer (NSCLC) with concurrent EGFR and TP53 mutations. 2025ASCO. TPS8662.
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
审批编号:CN-180313
有效期:2026-06-17
撰写:Coco
审核:Coco
排版:Babel
执行:Faline

