
前列腺癌当代管理全景:从全球流行病学到个体化精准诊疗的演进

前列腺癌 是全球男性健康领域的重大挑战,在三分之二的国家中已成为男性最常见的恶性肿瘤。过去三十年,影像技术、手术、放疗及系统性疗法的持续革新,推动诊疗格局重塑,现已建立起以精准化风险分层为核心的个体化管理体系。本文基于CA:A Cancer Journal for Clinicians的一篇综述《The contemporary management of prostate cancer》[1],系统梳理其核心观点,旨在呈现前列腺癌从筛查、诊断到分期治疗的全流程管理策略,以飨读者。
是全球男性健康领域的重大挑战,在三分之二的国家中已成为男性最常见的恶性肿瘤。过去三十年,影像技术、手术、放疗及系统性疗法的持续革新,推动诊疗格局重塑,现已建立起以精准化风险分层为核心的个体化管理体系。本文基于CA:A Cancer Journal for Clinicians的一篇综述《The contemporary management of prostate cancer》[1],系统梳理其核心观点,旨在呈现前列腺癌从筛查、诊断到分期治疗的全流程管理策略,以飨读者。


前列腺癌全球每年约150万新发病例,近40万人死亡[2]。预计未来20年内发病率和死亡率将翻倍,且发病率在北欧、澳大利亚/新西兰、加勒比及北美等地区最高。死亡率与发病率不匹配,主要归因于不同国家间筛查、诊断和治疗资源的差异。
风险因素方面,年龄增长、非裔/加勒比裔血统、阳性家族史及特定遗传突变是明确的风险因素。超过70%的病例诊断于65岁以上男性。BRCA1/2、HOXB13等基因的种系突变显著增加患病风险。有前列腺癌家族史的男性,其患病风险显著增高。


前列腺癌的筛查从前列腺特异性抗原 (PSA)初筛到磁共振成像
(PSA)初筛到磁共振成像 (MRI)引导整合策略的革新。PSA是主要筛查工具,但由于其特异性不足、假阳性率高,且10年内未能显示出明确的死亡率获益,反而易引发过度诊断(约40%低危患者无需治疗),现已不推荐全民常规筛查。当代筛查策略已转向精准化与整合化。通过整合临床变量、PSA动态变化、多参数活检前MRI、风险计算器及遗传标记的综合策略,其中PSA+多参数MRI联合筛查,仅对MRI提示的可疑病灶进行靶向活检,可使临床惰性疾病诊断率减半。欧盟正试点PSA+MRI风险评估标准化筛查方按,鼓励早期发现和诊断前列腺癌。
(MRI)引导整合策略的革新。PSA是主要筛查工具,但由于其特异性不足、假阳性率高,且10年内未能显示出明确的死亡率获益,反而易引发过度诊断(约40%低危患者无需治疗),现已不推荐全民常规筛查。当代筛查策略已转向精准化与整合化。通过整合临床变量、PSA动态变化、多参数活检前MRI、风险计算器及遗传标记的综合策略,其中PSA+多参数MRI联合筛查,仅对MRI提示的可疑病灶进行靶向活检,可使临床惰性疾病诊断率减半。欧盟正试点PSA+MRI风险评估标准化筛查方按,鼓励早期发现和诊断前列腺癌。
前列腺的诊断流程需结合PSA检测、影像学检查及病理评估。诊断通常始于血清PSA水平异常,或患者因排尿异常、性功能障碍 (早期)乃至骨痛、神经压迫症状(晚期)就医。影像学评估是诊断关键,多参数MRI是活检前的首选,可使25%以上患者避免后续无效活检。当MRI结果可疑(PI-RADS≥3分)时,需进行靶向联合系统活检。对于高危患者的基线分期或生化复发的探查,PSMA-PET/CT在敏感性和特异性上均显著优于传统成像(CT、骨扫描),全身MRI对骨转移评估灵敏度也更高。病理诊断基于腺体结构异常和细胞核异型性等特征,采用Gleason评分(3-5分)和分级组(GG1-5)对肿瘤侵袭性进行量化评估,为后续治疗决策提供核心依据。
(早期)乃至骨痛、神经压迫症状(晚期)就医。影像学评估是诊断关键,多参数MRI是活检前的首选,可使25%以上患者避免后续无效活检。当MRI结果可疑(PI-RADS≥3分)时,需进行靶向联合系统活检。对于高危患者的基线分期或生化复发的探查,PSMA-PET/CT在敏感性和特异性上均显著优于传统成像(CT、骨扫描),全身MRI对骨转移评估灵敏度也更高。病理诊断基于腺体结构异常和细胞核异型性等特征,采用Gleason评分(3-5分)和分级组(GG1-5)对肿瘤侵袭性进行量化评估,为后续治疗决策提供核心依据。
风险分层是临床管理的指南针。目前,前列腺癌采用美国癌症联合委员会(AJCC)《癌症分期手册》(2018年第8版)分类标准进行分期(详见表1),风险分级标准见表2。这一分层体系直接指导后续的治疗方案选择与预后判断。
表1 前列腺癌AJCC的TNM分期系统(第八版,2018年)


表2 前列腺癌的预后风险分组
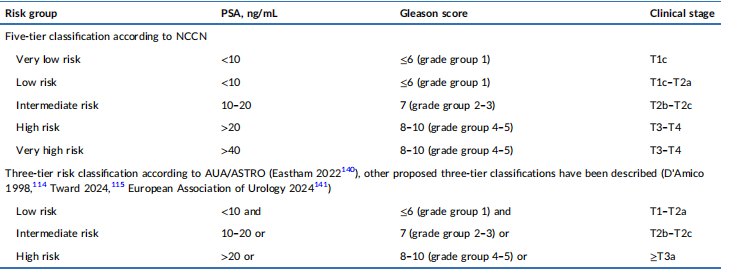


(一)局限性前列腺癌的治疗策略
•主动监测:对于低危及部分预后良好的中危患者,主动监测是首选,可避免过度治疗。通过每6个月PSA检测、每12-24个月多参数MRI和必要时活检进行严密监测。
•手术治疗:是中危、高危局部前列腺癌且预期寿命>10年患者的主要选择。机器人辅助前列腺切除术为常用术式,其神经保留技术还可保护勃起功能。术后,患者应在6个月时检查PSA,之后5年内每6个月一次,之后每年进行一次。
•放疗:对于中危、高危的患者,放疗是核心治疗手段。现代放疗技术(如中度大分割放疗和超大分割/立体定向体部放疗)在保证疗效的同时缩短了疗程。根治性放疗后,前5年间每6个月检查一次PSA,此后每年检查一次。此外,中高风险患者可考虑近距离放疗(低剂量永久性或高剂量率)。
•联合治疗:对于中危、高危患者,放疗联合雄激素剥夺疗法(ADT)可增强疗效,显著改善无转移生存期和总生存期。ADT疗程根据风险分级:中危患者为4-6个月,高危患者为18-36个月。
(二)生化复发与寡转移前列腺癌的治疗策略
根治性治疗后PSA升高定义为生化复发。PSMA-PET/CT可以精准定位复发部位,检出率随PSA升高而增加。若复发灶局限于前列腺床或盆腔,首选挽救性放疗±短期ADT。
针对寡转移前列腺癌(通常定义为≤5个转移灶)的患者,通过转移灶定向治疗延长疾病控制时间,延缓进入广泛转移阶段。
(三)转移性激素敏感性前列腺癌(mHSPC)的治疗策略
约有5%–15%的前列腺癌在就诊时为转移性,而在医疗服务可及性有限的国家,这一比例可升至20%–25%甚至更高。ADT治疗是转移性前列腺癌治疗的基石。
对于大多数mHSPC患者,都应在ADT基础上,联合雄激素受体通路抑制剂(ARPI)或多西他赛 化疗进行强化治疗,可显著延长生存期。对于高瘤负荷患者,采用ADT+多西他赛+ARPI的三联方案能进一步提升疗效,但需谨慎权衡其带来的毒性及对生活质量的影响。对于低瘤负荷患者,在全身治疗基础上对前列腺进行原发灶放疗可带来明确生存获益,同时降低泌尿生殖系统严重事件发生率并延缓疾病进展。
化疗进行强化治疗,可显著延长生存期。对于高瘤负荷患者,采用ADT+多西他赛+ARPI的三联方案能进一步提升疗效,但需谨慎权衡其带来的毒性及对生活质量的影响。对于低瘤负荷患者,在全身治疗基础上对前列腺进行原发灶放疗可带来明确生存获益,同时降低泌尿生殖系统严重事件发生率并延缓疾病进展。
(四)去势抵抗性前列腺癌(CRPC)的治疗策略
去势抵抗性前列腺癌定义为血清睾酮去势水平(<50 ng/dL或1.7 nmol/L)时疾病仍出现进展。
•非转移性去势抵抗性前列腺癌(nmCRPC)
新型ARPI联合ADT有助于改善nmCRPC患者的无转移生存期(MFS)和总生存期(OS)。
•转移性去势抵抗性前列腺癌(mCRPC)
当疾病进展到转移性去势抵抗阶段时,治疗需综合考量患者年龄、体能状况、肿瘤负荷、既往治疗史、基因特征及PSMA表达水平等多重因素,且ADT仍需持续进行。
CRPC的化疗以紫杉类药物为主。多西他赛是最常用的化疗药物,对于多西他赛治疗后进展的mCRPC患者,卡巴他赛可作为后续治疗选择(低剂量方案兼顾疗效与安全性);对于具有侵袭性表型或特殊组织学类型(如小细胞或间变型)的前列腺癌,可考虑含铂化疗方案。ARPI适用于初始治疗者。放射性核素治疗中,镭-223用于有症状的骨转移mCRPC患者,并需与骨保护剂联用。近年来,PSMA放射配体治疗发展迅速,特别是177Lu-PSMA-617已在国内获批双适应证:既往接受过ARPI和紫杉烷类治疗的PSMA阳性患者;既往接受过ARPI但未接受过紫杉烷类治疗的PSMA阳性患者。在这两类患者中,该疗法均展现出优于标准治疗的生存获益。多达20%–30%的mCRPC患者中存在DNA修复缺陷[3-4],因此建议对所有mCRPC患者进行基因检测,对于检测到同源重组修复(HRR)基因突变的患者,建议使用聚二磷酸腺苷核糖聚合酶(PARP)抑制剂或与ARPI联合使用。目前这些治疗策略的最佳应用顺序尚无统一共识。同时,除临床试验外,现有证据尚不足以支持免疫治疗在前列腺癌中的常规应用。
此外,当前还在进行多种新的临床研究,探索新的治疗靶点,包括用于微卫星不稳定性高肿瘤的PD-1抑制剂、选择性PARP1抑制剂、抑制类固醇生物合成的药物、小分子蛋白降解剂,以及靶向PSMA相关抗原(如激肽释放酶2、STEAP1)的T细胞结合剂和针对神经内分泌分化标志物(如DLL-3、EZH2)的靶向治疗等。
(五)特殊人群:虚弱患者老年与衰弱患者的治疗策略
治疗决策应基于生理年龄和整体健康状况,而非仅看实际年龄。70岁以上或存在衰弱迹象的患者,建议进行老年综合评估,并相应调整治疗强度,如缩短ADT疗程、选择副作用更小的放疗方案或调整药物剂量。
前列腺癌临床异质性显著,涵盖了从低风险疾病(治疗只能伤害而无法延长生命)到致命疾病(全球仍夺走太多生命)的广泛谱系,风险分层和个体化治疗是管理核心。目前已形成“筛查分层-精准诊断-个体化治疗-长期生存管理”的完整体系,新兴数据和新疗法将继续完善治疗范式,改善前列腺癌患者的精准化管理和治疗效果。
参考文献
[1]Chakrabarti D, Albertsen P, Adkins A, et al. The contemporary management of prostate cancer. CA Cancer J Clin. 2025; 75(6): 552-586. doi:10.3322/caac.70020.
[2]Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024;74(3):229-263.
[3]Robinson D, Van Allen EM, Wu YM, et al. Integrative clinical genomics of advanced prostate cancer. Cell. 2015;161(5):1215-1228.
[4]Shui, I.M., Burcu, M., Shao, C. et al. Real-world prevalence of homologous recombination repair mutations in advanced prostate cancer: an analysis of two clinico-genomic databases. Prostate Cancer Prostatic Dis 27, 728–735 (2024).
审批编号:CN-179885
有效期至:2026-06-20
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
