
2020 EBMT | 常红教授解读RACE研究:艾曲泊帕联合IST一线治疗SAA
医脉通编译整理,未经授权请勿转载。
受新冠疫情影响,血液病治疗领域的年度盛会——第46届欧洲血液和骨髓移植学会(EBMT)年会于2020年8月29日至9月1日首次以线上形式举办。在本届EBMT年会上,RACE研究1的初步结果重磅发布,进一步支持艾曲泊帕 联合标准免疫抑制疗法(IST)作为不适合移植的重型/极重型再生障碍性贫血
联合标准免疫抑制疗法(IST)作为不适合移植的重型/极重型再生障碍性贫血 (SAA/vSAA)患者的一线治疗新选择。医脉通特邀四川大学华西医院的常红教授对RACE研究结果进行解读。
(SAA/vSAA)患者的一线治疗新选择。医脉通特邀四川大学华西医院的常红教授对RACE研究结果进行解读。
研究介绍
RACE研究是首个国际性、研究者发起的、开放标签、随机对照的Ⅲ期试验,比较了标准IST联合或不联合艾曲泊帕作为SAA/vSAA患者一线治疗的疗效和安全性。
从2015年7月至2019年4月,招募了197例15岁以上的初治的SAA/vSAA患者(来自6个国家,24个研究中心)。患者随机分配至A组(标准IST组,n=101),治疗方案为马抗胸腺细胞球蛋白(hATG)40mg/kg x 4天+环孢菌素A(CsA)5mg/kg/天,1年后CsA减量,或B组(标准IST联合艾曲泊帕组,n=96),治疗方案为在上述标准IST的基础上,从第14天开始联合艾曲泊帕150mg/天,直到6个月(若早期达到CR则为3个月)。
研究的主要终点是3个月时血液学完全缓解(CR)率;次要终点包括至首次血液学反应时间、6/12/18/24个月时的血液学反应、总生存期(OS)、无事件生存期(EFS)、克隆演变、复发率和安全性。
研究结果
两组患者基线特征相当,中位年龄53岁。中位随访时间为18个月。研究主要终点已达到,A组和B组的3个月时血液学CR率分别为9.9%和21.9%(p=0.012);3个月时的总缓解率(OR=CR+PR)分别为31.7%和59.4%(图1)。截至进行分析时,对于存活、未移植和无克隆演变的患者,6个月时的OR分别为44.8%和71.8%。
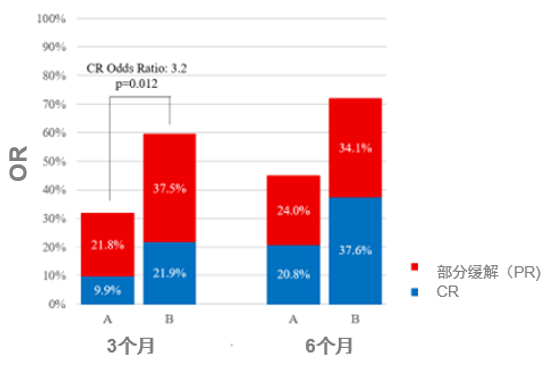
图1:血液学反应
在研究期间,共有22例患者死亡(A组14例,24个月时OS率为83.2%;B组8例,24个月时OS率为86.3%)(p=0.142)(图2)。
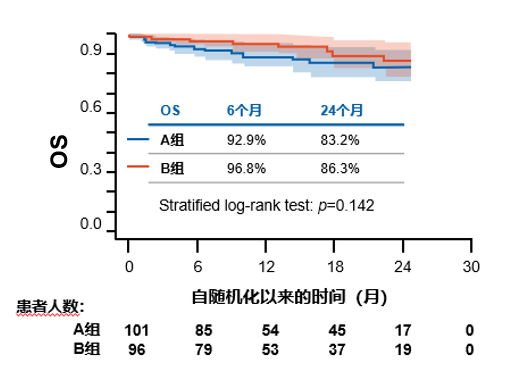
图2:OS
两组的严重不良事件(SAEs)相似。克隆演变方面,两组各有1例进展为MDS,各有7例核型异常。对31个基因进行了高灵敏度NGS分析,纳入163例患者的基线样本和132例患者的6个月随访样本,发现两组患者在体细胞髓系突变方面没有显著差异。
专家解读
SAA/vSAA是一种严重危及生命的骨髓造血衰竭性疾病。对于不适合进行异基因造血干细胞移植的SAA/vSAA患者,ATG联合CsA是标准的IST。然而,IST作为一线治疗疗效有限,约三分之一的患者对IST反应不佳或出现疾病复发。2
艾曲泊帕是一种口服小分子血小板生成素受体激动剂(TPO-RA),对于IST难治/复发的再生障碍性贫血(AA)患者,艾曲泊帕单药治疗可使40-50%的患者获得血液学应答,且其中35-50%可获得三系血细胞应答。3,4因此,临床开始探索联合应用标准IST和艾曲泊帕作为SAA/vSAA患者的一线治疗,以提高CR率并改善长期预后。这种联合治疗方案的有效性和安全性已在Ⅰ期和Ⅱ期临床试验中得到了验证。2
本文介绍的RACE Ⅲ期研究显示,与标准IST相比,标准IST联合艾曲泊帕作为不适合移植的SAA/vSAA患者的一线治疗,具有更优的血液学反应。本研究中CR定义与NIH研究相同,而PR定义比NIH研究更严格(要求脱离输血 依赖);用药方案中艾曲泊帕从IST后第14天开始应用,与NIH研究2中的队列1类似,两组患者的6个月时CR率类似(本研究的6个月时CR率为38%,NIH研究中这一队列的6个月时CR率为33%),提示了NIH研究的可重复性。此外,本研究也证实,艾曲泊帕联合IST方案,安全性良好,未见到克隆演变风险增加。因此,本Ⅲ期试验支持标准IST联合艾曲泊帕作为不适合移植的SAA/vSAA患者的一线治疗。
依赖);用药方案中艾曲泊帕从IST后第14天开始应用,与NIH研究2中的队列1类似,两组患者的6个月时CR率类似(本研究的6个月时CR率为38%,NIH研究中这一队列的6个月时CR率为33%),提示了NIH研究的可重复性。此外,本研究也证实,艾曲泊帕联合IST方案,安全性良好,未见到克隆演变风险增加。因此,本Ⅲ期试验支持标准IST联合艾曲泊帕作为不适合移植的SAA/vSAA患者的一线治疗。
参考文献:
1. De Latour RP ,et al. EBMT 2020 abstract.
2. Danielle M. Townsley, et al. N Engl J Med 2017; 376:1540-1550
3. Desmond R, et al. Blood. 2014;123:1818-25
4. Winkler T, et al. Blood. 2019; 133:2575-85.

