
冠脉狭窄<50%的心梗,该如何判别病因?
作者:蓝鲸晓虎
本文为作者授权医脉通发布,未经授权请勿转载。
非阻塞性冠状动脉粥样硬化所致心肌梗死(MINOCA)又称冠状动脉非阻塞性心肌梗死,其特征为血管造影 示冠状动脉狭窄<50%的情况下出现心肌损伤。
示冠状动脉狭窄<50%的情况下出现心肌损伤。
MINOCA占全部心肌梗死(MI)的5.9%-7.8%,17%-33%存在ST段抬高。与MI和阻塞性冠状动脉疾病(CAD)患者相比,MINOCA患者更年轻,多见于无冠心病危险因素的女性,血清肌钙蛋白 峰值水平更低,合并心衰、终末期肾病、房颤或慢性肺病的比例较高。
峰值水平更低,合并心衰、终末期肾病、房颤或慢性肺病的比例较高。
MINOCA的病理生理机制概述
排除有明确诱因的急性心梗(如临床表现典型的心肌炎 或肺栓塞),行侵入性冠状动脉造影
或肺栓塞),行侵入性冠状动脉造影 后方能诊断MINOCA。
后方能诊断MINOCA。
MINOCA的病理生理机制包括:
➤对应于1型心梗的与缺血相关的自发性MI(动脉粥样硬化斑块破裂、血栓形成、斑块侵蚀、冠状动脉夹层);
➤对应于2型心梗的心肌氧供减少或需求增加(冠状动脉痉挛、微血管痉挛、冠状动脉栓塞);
➤其他可表现为MINOCA的非缺血性疾病(Takotsubo心肌病或心肌炎)。
MINOCA的病因有哪些?
1.斑块破裂
斑块破坏是MINOCA相对常见的原因,在动脉粥样硬化早期,冠状动脉斑块可通过使血管壁向外扩张而聚集,保护血管腔。随着时间的推移,这些斑块可能表现出易损特征(脂质核厚、正性重构和纤维帽薄),因此更可能破裂。
事实上,大多数导致MI的斑块在血管造影下仅表现为轻度,MI通常是由斑块破坏或侵蚀引起的。
2.冠脉痉挛
28%的MINOCA患者存在冠状动脉痉挛,与血管平滑肌细胞对内源性血管痉挛刺激的高反应性相关,但也可能在短暂接触外源性血管痉挛药物(如可卡因)后发生。
通过标准化冠状动脉内麦角新碱 或乙酰胆碱激发试验
或乙酰胆碱激发试验 进行诊断——心外膜血管收缩>75% 伴心绞痛症状和ECG或超声心动图
进行诊断——心外膜血管收缩>75% 伴心绞痛症状和ECG或超声心动图 证实的心肌缺血时为阳性。
证实的心肌缺血时为阳性。
值得注意的是,男性、吸烟者、弥漫性冠状动脉粥样硬化和MINOCA患者的心外膜痉挛更常见,而微血管痉挛更常与稳定型心绞痛和舒张功能障碍相关。
出于安全性原因,通常避免在MI急性期进行激发痉挛试验;此外应注意麦角新碱静脉给药后多支血管痉挛时间延长的风险。
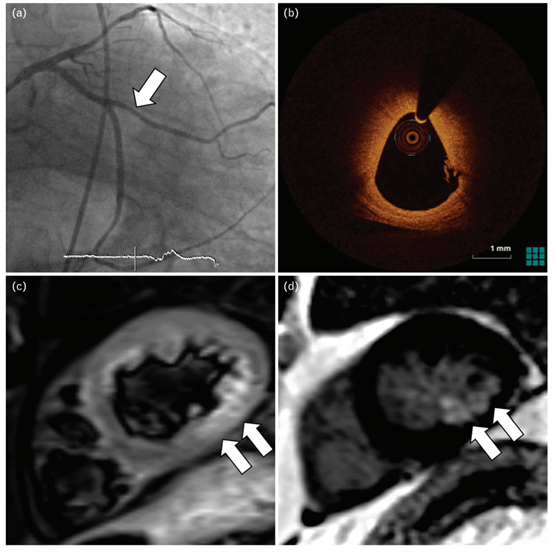
冠状动脉血栓形成患者的影像学检查
(a)冠状动脉造影显示非ST段心肌梗死患者的大钝缘支轻度病变(箭头); (b)光学相干断层扫描显示血栓覆盖纤维斑块; (c)心脏磁共振成像 共振显示对应于心肌水肿
共振显示对应于心肌水肿 的T2高信号(↖)以及(d)下侧壁心内膜下晚期钆增强(↖)
的T2高信号(↖)以及(d)下侧壁心内膜下晚期钆增强(↖)
3.冠脉栓塞
可能由冠状动脉斑块破裂或全身血栓(如房颤、心脏瓣膜病、心尖血栓、感染性心内膜炎 、反常栓塞)引起,或与遗传性或获得性血栓疾病相关。血栓形成倾向筛查显示,14%的MINOCA患者存在遗传性血栓性疾病(主要为蛋白C
、反常栓塞)引起,或与遗传性或获得性血栓疾病相关。血栓形成倾向筛查显示,14%的MINOCA患者存在遗传性血栓性疾病(主要为蛋白C 缺陷症或凝血因子V Leiden突变)。
缺陷症或凝血因子V Leiden突变)。
此外,在获得性抗磷脂综合征患者中,MINOCA的患病率可高达所有MI的20%。
少数情况下,冠状动脉栓塞起源于瓣膜赘生物、心脏肿瘤、粘液瘤或医源性空气栓等。
值得注意的是,涉及冠状动脉血栓形成的各种机制(即斑块破坏、冠状动脉痉挛和冠状动脉栓塞)可能互相交织,加大诊断难度。
4.冠脉夹层
自发性冠脉夹层(SCAD)是指非动脉粥样硬化导致的心外膜冠状动脉壁自发性分离,涉及中膜夹层伴壁内血肿形成,随后管腔压迫伴或不伴内膜撕裂。大部分SCAD患者为绝经前和围绝经期女性,多无心血管疾病风险因素,但焦虑、抑郁和偏头痛 的患病率较高。
的患病率较高。
当无法确定诊断时,冠脉造影期间行冠脉成像至关重要,但是由于医源性夹层的风险增加,必须谨慎。
5.Takotsubo心肌病
Takotsubo心肌病占MINOCA病例的14%,大多为绝经后女性,Takotsubo心肌病患者中抑郁和焦虑的发生率较高。
Takotsubo心肌病的病理生理机制包括阵发性冠状动脉微血管功能障碍 和儿茶酚胺
和儿茶酚胺 诱导的心肌顿抑等。ECG变化通常包括新发的ST段抬高和/或T波倒置,心肌肌钙蛋白轻度升高,大多与ECG异常不成比例。
诱导的心肌顿抑等。ECG变化通常包括新发的ST段抬高和/或T波倒置,心肌肌钙蛋白轻度升高,大多与ECG异常不成比例。
Takotsubo心肌病的诊断需通过左心室造影或超声心动图检测到的左心室壁运动异常排除阻塞性CAD。左心室中段一过性运动功能减退或运动不能伴基底段高动力是典型表现。急性期行CMR示典型的局部室壁运动异常,伴有心肌水肿,但无晚期钆增强。
如何明确MINOCA患者的病因?
超声心动图和/或左心室造影是明确MINOCA初步诊断的重要手段。识别室壁运动异常的范围(局部或整体)、分布[累及左心室中段(或伴心尖)]和可逆性有助于区分缺血性疾病、Takotsubo心肌病和心肌炎,并决定进一步检查。
冠状动脉磁共振成像(CMR)联合晚期钆增强(LGE)是体内识别MI相关心肌纤维化(瘢痕)的金标准。心内膜下的LGE区域意味着缺血性心肌损伤,而LGE的心外膜下或中壁定位表明非缺血性原因。由于LGE在MI急性期范围最广,因此在MINOCA诊断后最初几天内准确度最高。
然而CMR不能特异性地确定心肌损伤的确切病理机制。使用冠状动脉内成像,包括血管内超声 (IVUS)和光学相干断层扫描(OCT)
(IVUS)和光学相干断层扫描(OCT) ,允许探查冠状动脉壁,并且有助于识别隐匿性斑块破坏、血栓形成或冠状动脉夹层。
,允许探查冠状动脉壁,并且有助于识别隐匿性斑块破坏、血栓形成或冠状动脉夹层。
与IVUS相比OCT提供了更高的轴向分辨率(100-200 mm vs 10-20 mm),是唯一允许详细评估粥样纤维帽完整性的检查手段。
根据MINOCA病因划分的血管造影结果、诊断检查和相应治疗手段
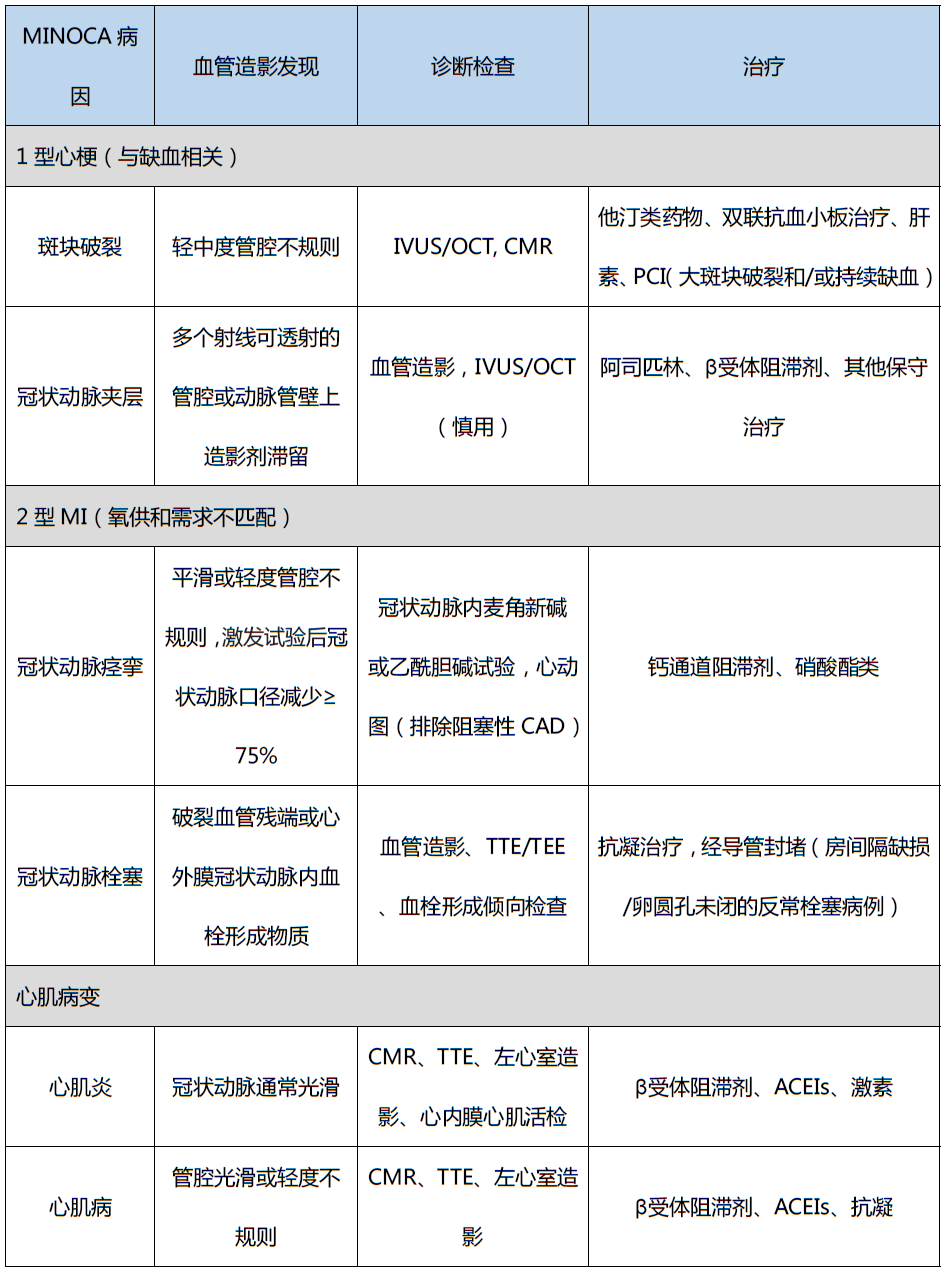
ACEIs,肾素血管紧张素系统阻滞剂;CAD,冠状动脉疾病;CMR,心脏磁共振;IVUS,血管内超声;MINOCA,心肌梗死伴非阻塞性冠状动脉粥样硬化;OCT,光学相干断层扫描;PCI,经皮冠状动脉介入治疗;TEE,经食管超声心动图;TTE,经胸超声心动图。
患者预后如何?
根据病因,MINOCA的预后各不相同,3.5年随访时心肌病的死亡率最高(15%),其次是MI(4%)、心肌炎(2%)和CMR正常(2%)者。
观察性研究表明,他汀类药物和ACEIs长期治疗及定期随访可显著改善预后。
小结
MINOCA是一种存在多种潜在病因的综合征,目前尚无明确指南指导其临床治疗。对于冠脉造影正常的MINOCA患者,经常被误诊为非心脏疾病,错失最佳治疗时机。因此要综合考虑病史、超声心动图、心肌酶、冠脉造影和左心室造影等检查,鉴别其发病原因后,再进行风险分层和实施最合适的治疗方案。
参考文献
1. Opolski MP. Mechanisms of myocardial infarction with nonobstructive coronary atherosclerosis: a multifaceted play of different actors with guarded prognosis [published online ahead of print, 2020 Aug 26]. Curr Opin Cardiol. 2020; 10.1097/HCO.0000000000000787.
2. Opolski MP, Spiewak M, Marczak M, et al. Mechanisms of myocardial infarction in patients with nonobstructive coronary artery disease: results from the optical coherence tomography study. JACC Cardiovasc Imaging 2019; 12: 2210–2221.
3. Nordenskjo AM, Lagerqvist B, Baron T, et al. Reinfarction in patients with myocardial infarction with nonobstructive coronary arteries (MINOCA): coronary fifindings and prognosis. Am J Med 2019; 132:335– 346.
4. Eggers KM, Hjort M, Baron T, et al. Morbidity and cause-specifific mortality in first-time myocardial infarction with nonobstructive coronary arteries. J Intern Med 2019; 285: 419–428.
5. Eggers KM, Hadziosmanovic N, Baron T, et al. Myocardial infarction with nonobstructive coronary arteries: the importance of achieving secondary prevention targets. Am J Med 2018; 131: 524–531.
6. 杨超君,杨俊.非阻塞性冠状动脉粥样硬化发生急性心肌梗死的机制和诊疗方案[J]. 中国老年学杂志, 2015, (19): 5642-5643.
