
“氏”说新语,大咖解惑|听王晓稼教授聊聊新型SERD类药物
临床上,约80%的乳腺癌 检测雌激素
检测雌激素 受体(ER)呈阳性1,这类乳腺癌细胞的增殖严重依赖ER。近年来,由于激素受体的检测普及以及新的内分泌药物的临床应用,内分泌治疗为ER+乳腺癌患者带来了临床获益。然而,已有的内分泌药物尚存在一些问题,如不能完全抑制ER信号传导,从而导致肿瘤细胞继续增生;或者由于肌肉注射的给药方式限制了药物的临床应用,因此ER+乳腺癌患者亟需新的治疗选择。近日,医脉通有幸邀请到中国科学院大学附属肿瘤医院的王晓稼教授,就“乳腺癌的内分泌治疗进展——新型SERD类药物“进行分享。
受体(ER)呈阳性1,这类乳腺癌细胞的增殖严重依赖ER。近年来,由于激素受体的检测普及以及新的内分泌药物的临床应用,内分泌治疗为ER+乳腺癌患者带来了临床获益。然而,已有的内分泌药物尚存在一些问题,如不能完全抑制ER信号传导,从而导致肿瘤细胞继续增生;或者由于肌肉注射的给药方式限制了药物的临床应用,因此ER+乳腺癌患者亟需新的治疗选择。近日,医脉通有幸邀请到中国科学院大学附属肿瘤医院的王晓稼教授,就“乳腺癌的内分泌治疗进展——新型SERD类药物“进行分享。

王晓稼 教授
中国科学院大学附属肿瘤医院(浙江省肿瘤医院)院长助理
乳腺内科主任
博士、博士生导师、主任医师
国家卫健委合理用药专家组成员兼乳腺癌实践基地主任
国家肿瘤质控中心乳腺癌专家委员
浙江省肿瘤诊治质控中心副主任
CSCO乳腺癌专家委员会副主任委员
中国抗癌协会乳腺癌专业委员会常委
浙江省抗癌协会肿瘤内科专业委员会主任委员
医脉通:请您介绍一下目前ER+乳腺癌都有哪些内分泌治疗药物?
王晓稼教授:ER+乳腺癌现有的内分泌治疗药物包括:芳香化酶抑制剂(AI)、选择性雌激素受体调节剂(SERM)、选择性雌激素受体下调剂(SERD)、促性腺激素释放激素(LHRH)类似物和孕激素 类药物。
类药物。
• SERMs以他莫昔芬为代表,可竞争性与ER结合,具有拮抗雌激素的作用,但同时有部分雌激素激动作用;其他SERM类药物有托瑞米芬 、雷洛昔芬
、雷洛昔芬 ,临床应用并不广泛。
,临床应用并不广泛。
• 氟维司群是目前唯一获批的SERD类药物,与SERM不同,SERD只有ER的拮抗作用,而无激动作用,可阻断雌激素与ER结合并下调ER的表达;
• AIs包括非甾体类的来曲唑 、阿那曲唑
、阿那曲唑 ,和甾体类的依西美坦
,和甾体类的依西美坦 ;芳香化酶是催化雄激素向雌激素转化的关键酶和限速酶,AIs可通过使芳香化酶失活从而抑制雄激素向雌激素转化;
;芳香化酶是催化雄激素向雌激素转化的关键酶和限速酶,AIs可通过使芳香化酶失活从而抑制雄激素向雌激素转化;
• LHRH类似物包括戈舍瑞林 、亮丙瑞林
、亮丙瑞林 等,适用于绝经前期及围绝经期乳腺癌患者,可减少黄体生成素(LH)及滤泡刺激素(FSH)的分泌,从而抑制卵巢雌激素的产生;
等,适用于绝经前期及围绝经期乳腺癌患者,可减少黄体生成素(LH)及滤泡刺激素(FSH)的分泌,从而抑制卵巢雌激素的产生;
• 临床最常应用的孕激素类药物为甲地孕酮 ,同样具有降低雌激素水平的作用。
,同样具有降低雌激素水平的作用。
医脉通:Giredestrant(GDC-9545)是一种新型SERD类药物,能否请您介绍一下与其他内分泌治疗药物相比,它有什么特点?
王晓稼教授:Giredestrant(GDC-9545)是一种高效的非甾体口服SERD,通过与ER强效结合,导致ER无法激活靶向基因的转录,并促使ER蛋白降解,从而更彻底地阻断ER信号传导,抑制肿瘤细胞增殖(图1);这一效果不受ESR1突变状态的影响2-3。
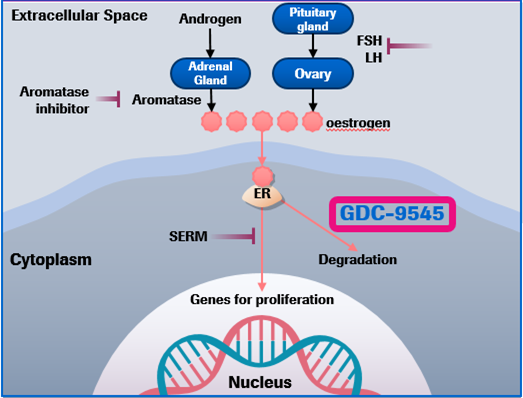
图1 Giredestrant(GDC-9545)的作用机制(点击可放大)
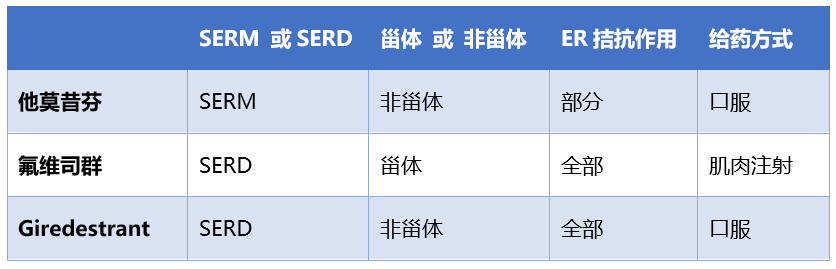
与他莫昔芬相比,Giredestrant对ER信号通路具有更强的抑制作用4;而相较于氟维司群的肌肉注射给药,Giredestrant口服给药具有更高的药物暴露剂量2(表1)。此外,由于Giredestrant对野生型和突变型ER均具有亲和力,因此同时具有有效治疗ESR1野生型或突变型HR+乳腺癌的潜力。目前正在进行多项临床试验,以评估Giredestrant单药或联合治疗的安全性和有效性。
表1 Giredestrant与他莫昔芬和氟维司群的对比2,4-6
医脉通:您能否介绍一下Giredestrant(GDC-9545)到目前为止的临床研究成果?
王晓稼教授:目前Giredestrant的首个I期临床研究及进一步的Ib期研究结果已公布,提示Giredestrant单药或联合治疗的耐受性良好且具有抗肿瘤活性。
I期试验采用3 + 3剂量递增设计,主要目的是确定Giredestrant单药用于绝经后ER+/HER2-转移性乳腺癌患者的安全性、药代动力学(PK)、药效学(PD)和II期推荐剂量3。从2017年11月27日至2019年9月4日,共29例患者入组治疗。Giredestrant以4种不同剂量给药:10mg、30mg、90mg和250mg,均为每日一次(QD)。在所有剂量下,Giredestrant治疗耐受性良好,无剂量限制性毒性、特别关注的不良事件(AE)和与治疗相关的严重AE出现。没有患者因不良事件而减少剂量或停止治疗。
PK分析显示,Giredestrant的血浆暴露剂量与服药剂量成比例地增加,终末消除半衰期(terminal half-life)约30-40个小时,支持每日一次的给药方式。在可评估的8例患者中,通过治疗前后的配对活检,观察到Giredestrant给药后患者的ER、PR、Ki67蛋白水平和ER通路标志评分降低(图2)。
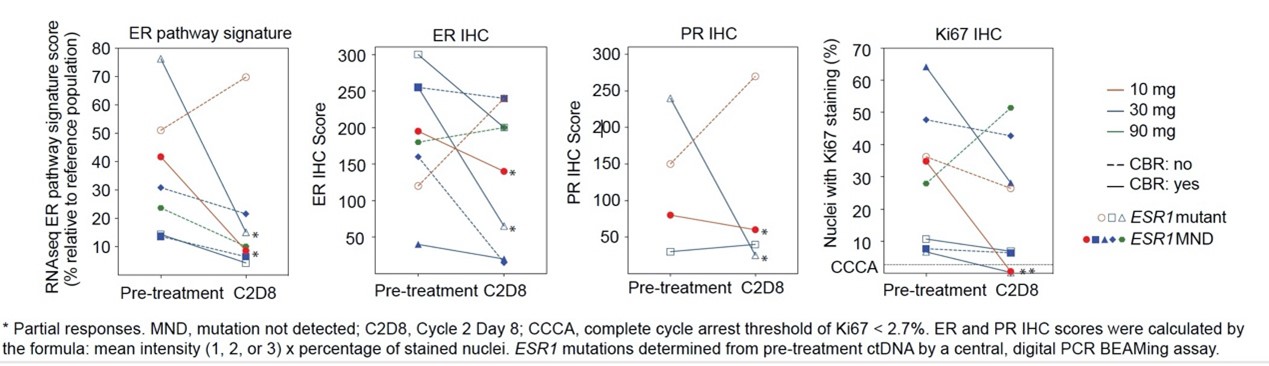
图2 配对活检后ER、PR、Ki67蛋白水平和ER通路标志评分(点击可放大)
2020年ASCO会议公布了Giredestrant的Ib期研究结果7。该研究纳入了既往接受过≤2种治疗的局部晚期或转移性ER+/HER2-乳腺癌患者,并被分为了两组队列,其中队列A接受Giredestrant(100mg,每日一次)±LHRH激动剂方案;队列B接受Giredestrant(100mg)+哌柏西利 (125mg,21天治疗/7天停药)±LHRH激动剂方案。
(125mg,21天治疗/7天停药)±LHRH激动剂方案。
截至2020年1月31日,共有88例患者入组,队列A有40人,队列B有48人。队列A和队列B中均有58%的患者发生与Giredestrant相关的AE,一般为1-2级,其中队列A的3级AE有疲劳、转氨酶升高和腹泻 事件。PK分析表明,Giredestrant与哌柏西利间无临床相关的药物间相互作用。在可评估的12例患者中,通过治疗前后的配对活检,观察到ER(83%),PR(88%),Ki67(75%)蛋白水平和ER通路标志评分(67%)的降低。A、B队列临床获益(CR、PR或24周时或之后首次观察到疾病进展)率分别为55%和81%。在这两个队列中,先前接受氟维司群治疗的患者,以及入组时可检测到的ESR1突变的患者均观察到临床获益(图3)。
事件。PK分析表明,Giredestrant与哌柏西利间无临床相关的药物间相互作用。在可评估的12例患者中,通过治疗前后的配对活检,观察到ER(83%),PR(88%),Ki67(75%)蛋白水平和ER通路标志评分(67%)的降低。A、B队列临床获益(CR、PR或24周时或之后首次观察到疾病进展)率分别为55%和81%。在这两个队列中,先前接受氟维司群治疗的患者,以及入组时可检测到的ESR1突变的患者均观察到临床获益(图3)。
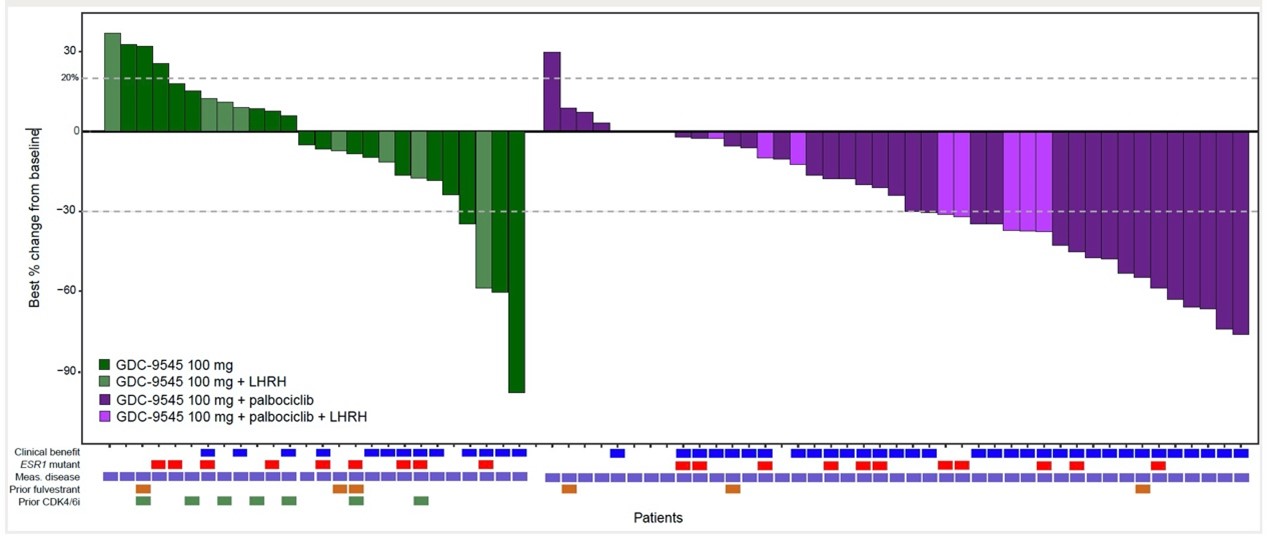
图3 Giredestrant单药或联合治疗表现出抗肿瘤活性(点击可放大)
医脉通:目前还开展了哪些Giredestrant(GDC-9545)相关临床研究?
王晓稼教授:除上述研究外,在clinicaltrials上可看到包含新辅助治疗、用于晚期患者在内的多项Giredestrant临床研究,目前这些研究均处在入组阶段。
GO39932是一项多中心、开放标签、剂量递增、剂量扩展、Ia/Ib期研究,用于评估Giredestrant单药或与哌柏西利和/或LHRH激动剂联用,在局部晚期或转移性ER+/HER2-乳腺癌患者中的安全性、PK、PD活性和初步的抗肿瘤活性8。如上文提到,2020年ASCO会议公布了GO39932研究的中期分析结果,目前研究还在进行中。
WO42133是一项随机、多中心、开放标签、双臂、II期研究,旨在评估Giredestrant对比阿那曲唑(窗口期),以及Giredestrant+哌柏西利对比阿那曲唑+哌柏西利(新辅助治疗阶段)用于未经治疗的绝经后ER+/HER2-乳腺癌患者的疗效、安全性和PK。这项研究预计入组215例受试者9。
WO42312 是一项随机、开放标签、多中心的II期研究,将评估与医生选择的内分泌单药相比,Giredestrant单药用于局部晚期或转移性ER+/HER2-乳腺癌患者的疗效和安全性,纳入的受试者既往已在接受过1线或2线系统治疗(包含一种内分泌治疗)(图4)。研究将共入组300例受试者10。
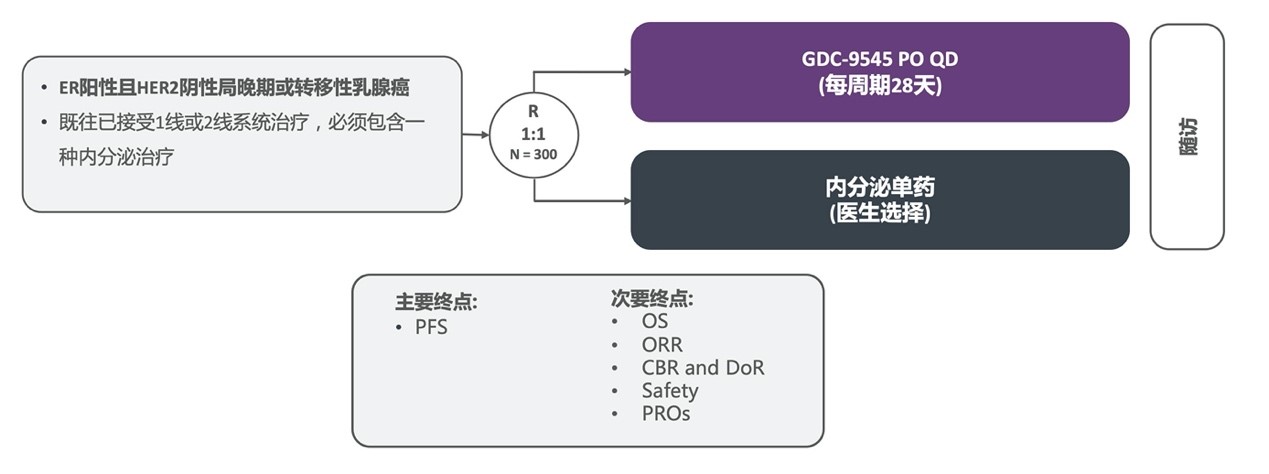
图4 WO42312研究设计(点击可放大)
BO41843 是一项随机、双盲、安慰剂对照的多中心III期研究,目的是评估Giredestrant+哌柏西利对比来曲唑+哌柏西利在局部晚期或转移性ER+/HER2-乳腺癌患者中的疗效和安全性(图5)。该研究的计划入组受试者最多,有978例 11。
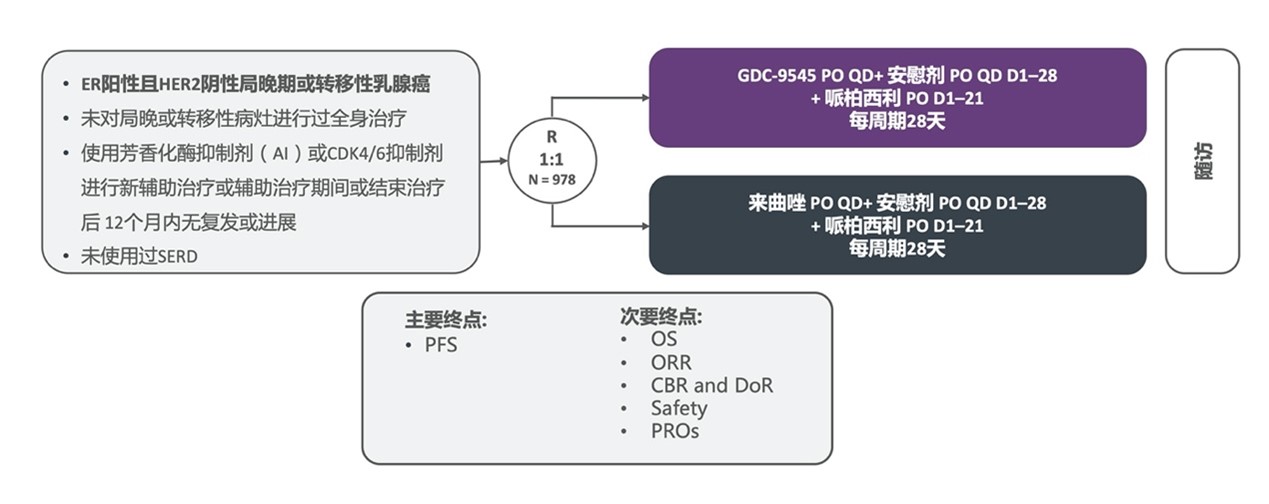
图5 BO41843研究设计(点击可放大)
值得一提的是,中国参与了WO42312和BO41843这两项研究。PI分别是复旦大学附属肿瘤医院的吴炅教授和中国医学科学院肿瘤医院的徐兵河教授。我们中国科学院大学附属肿瘤医院有望加入WO42312和BO41843研究中。也就是说,将来会有中国患者人群的数据分析以指导我们的临床。
结语
目前,治疗HR+乳腺癌患者的常用手段是抗ER类药物(包括SERM类他莫昔芬和SERD类氟维司群)。然而,这些药物或不能完全抑制ER信号传导导致肿瘤细胞继续增殖,或由于肌肉注射给药存在药物暴露量受限的问题。Giredestrant(GDC-9545)作为一种高效的口服SERD药物,具有彻底阻断ER信号传导的优势,同时口服给药,药物暴露剂量充分。目前全球已有多项Giredestrant临床试验正在开展,其中中国参与了WO42312和BO41843两项临床试验。十分期待这些研究成果为乳腺癌患者带来更多的福音!
参考文献:
1. Lumachi F, et al. World J Biol Chem. 2015 Aug 26;6(3):231-9.
2. Metcalfe C, et al. SABCS 2018 (Abstract P5-04-07)
3. Jhaveri K, et al. SABCS 2019 (Abstract PD7-05)
4. Metcalfe C, et al. AACR 2020 (Abstract 3406)
5. 枸橼酸他莫昔芬片 说明书
说明书
6. 氟维司群注射液 说明书
说明书
7. Lim et al. ASCO 2020 (Abstract 1023)
8. https://www.clinicaltrials.gov/ct2/show/NCT03332797?term=GO39932&draw=2&rank=1
9. https://www.clinicaltrials.gov/ct2/show/NCT04436744?term=WO42133&draw=2&rank=1
10. https://www.clinicaltrials.gov/ct2/show/NCT04576455?term=WO42312&draw=2&rank=1
11. https://www.clinicaltrials.gov/ct2/show/NCT04546009?term=BO41843&draw=2&rank=1

