
自发性冠状动脉夹层的管理,你要的流程图来了
自发性冠状动脉夹层(spontaneous coronary artery dissection,SCAD)是指非医源性创伤、非动脉粥样硬化 性病因所致冠状动脉夹层分离,继而形成假腔压迫真腔,减少甚至完全阻塞冠状动脉血流的冠状动脉疾病。SCAD是年轻女性急性冠状动脉综合征
性病因所致冠状动脉夹层分离,继而形成假腔压迫真腔,减少甚至完全阻塞冠状动脉血流的冠状动脉疾病。SCAD是年轻女性急性冠状动脉综合征 (ACS
(ACS )和猝死
)和猝死 的常见原因。尽管人们对SCAD的认识不断提高,但仍缺乏SCAD急性期和长期管理的研究数据。
的常见原因。尽管人们对SCAD的认识不断提高,但仍缺乏SCAD急性期和长期管理的研究数据。
2021年11月,克利夫兰诊所心血管科的Pristera N博士等在《克利夫兰医学期刊》(Cleveland Clinic Journal of Medicine)发表了一篇综述,回顾了现有的关于SCAD治疗的文献,并全面总结了管理策略,包括血管重建、药物治疗和长期随访。
危险因素
由于诊断不足,SCAD的真实患病率尚不明确。SCAD多见于女性,尤其是缺乏典型心血管危险因素的年轻女性。男性SCAD所占比例仅为10%,通常由运动或搬运重物等躯体压力因素诱发。研究表明,SCAD占ACS病例总数的1%-4%,占围产期ACS的15%-20%,占60岁以下女性ACS的35%。
与SCAD关联最密切的疾病是肌纤维发育不良,慢性全身炎症性疾病、结缔组织病、妊娠 和甲状腺功能减退
和甲状腺功能减退 症等疾病也与SCAD有关。最近,研究者确定了一些与SCAD风险增加有关的遗传位点。此外,已报道的SCAD诱发因素包括:违禁药物使用、情绪波动、剧烈运动、反胃、Valsalva动作、用力和其他身体压力。
症等疾病也与SCAD有关。最近,研究者确定了一些与SCAD风险增加有关的遗传位点。此外,已报道的SCAD诱发因素包括:违禁药物使用、情绪波动、剧烈运动、反胃、Valsalva动作、用力和其他身体压力。
影像学诊断
对所有发生ACS年轻患者,特别是缺乏典型心血管危险因素的年轻女性,都应该高度怀疑SCAD。各种影像学检查有助于SCAD的诊断,然而,冠脉造影等检查与夹层扩大的风险相关,因此,冠状动脉内成像多仅用于明确诊断或指导经皮冠状动脉介入治疗(PCI)。
1.冠脉造影
冠脉造影是SCAD最常用的诊断方法,也是诊断的金标准。SCAD病变部位的冠脉造影表现为多条放射线、造影剂染色并延迟清除,以及弥漫性的长狭窄,而其他冠状动脉无明显动脉粥样硬化的证据。如果冠脉造影不能确诊SCAD,可进一步行血管内超声 (IVUS)或光学相干断层成像(OCT)检查。
(IVUS)或光学相干断层成像(OCT)检查。
2.光学相干断层成像
光学相干断层成像的优势在于其高空间分辨率(<10 μm),可用于检测真腔和假腔、壁内血肿和夹层入口。然而,光学相干断层成像需要额外的强对比剂注射和更快的回拉速度,可能会导致夹层扩大。
3.血管内超声
血管内超声比光学相干断层成像的可及性更高,使用更广泛。
4.冠脉CTA
冠脉CTA可以显示SCAD的夹层皮瓣和壁内血肿,但由于冠状动脉缺损可能很细微,远端血管的可视化程度很低,经常得出假阴性的检查结果。冠脉CTA在评估疾病复发或随访中具有潜在的作用,但由于缺乏足够的敏感度,排除急性期SCAD的敏感性不够。
SCAD的治疗
SCAD与动脉粥样硬化性ACS的治疗策略不同,病变部位的血运重建是动脉粥样硬化性ACS治疗的基石,但大多数临床稳定的SCAD患者的管理主要是药物治疗。两者存在治疗策略差异的主要原因有以下两点:
➤ SCAD的病变血管会自发性地逐渐愈合,多数患者(73%-97%)的病变在4-6周内完全愈合。
➤在动脉壁完整性损坏的情况下,血运重建术与高失败率和不良预后有关。对病变血管进行器械操作,可能会使疾病恶化并阻碍愈合。导丝进入病变动脉时可能误入假腔,导致夹层范围扩大;球囊扩张可导致近端或远端壁内血肿的延伸或迁移;血管愈合和结构改变会导致支架位置不当,可导致远期并发症,如支架血栓形成。
推荐使用如图1所示的SCAD管理流程。
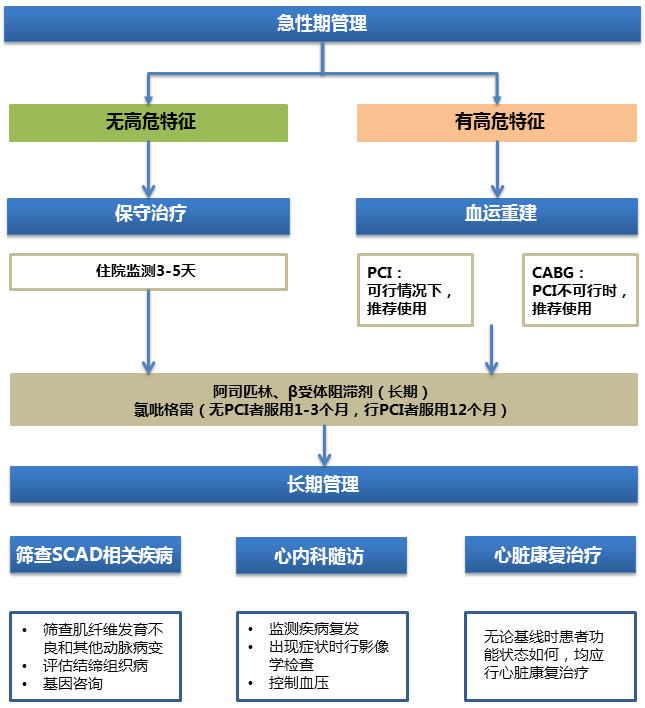
图1 SCAD的管理流程
1.研究数据支持保守治疗
观察性研究一致表明,对SCAD患者而言,PCI与更差的预后和高并发症率有关。一项纳入了189名SCAD患者的回顾性研究显示,PCI治疗的手术失败率为53%。除手术失败以外,PCI还与紧急冠状动脉旁路移植(CABG)高风险有关。
2.部分患者可行血运重建
血运重建术可能适用于有以下高风险特征的SCAD患者:
➤左主干冠状动脉夹层;
➤持续心肌缺血;
➤近端血管TIMI 0-1级血流;
➤血流动力学不稳定;
➤难治性心律失常 。
。
3.心源性休克 的器械支持治疗
的器械支持治疗
对于合并心源性休克的SCAD,可根据非SCAD ACS治疗的指南共识进行器械循环支持治疗。虽然有病例报告表明,主动脉内球囊泵和体外膜氧合 可以安全地用于SCAD患者,但仍应谨慎使用。
可以安全地用于SCAD患者,但仍应谨慎使用。
药物治疗
SCAD的药物治疗主要包括抗血小板药物和β受体阻滞剂(见表1)。对于不能耐受β受体阻滞剂的患者,应考虑使用非二氢吡啶类钙通道阻滞剂。
表1 SCAD的治疗药物

根据专家共识,在没有其他明确的抗凝指征(如左心室血栓或其他血栓栓塞性疾病)的情况下,确诊SCAD后应停用抗凝剂。少数已发表的SCAD合并左心室血栓的病例报告表明,抗凝治疗是安全的。
SCAD患者中,溶栓治疗是禁忌。在没有其他降脂治疗指征的情况下,SCAD患者不常规使用他汀类药物。
长期管理
SCAD的长期管理需要关注几个方面,包括筛查肌纤维发育不良、监测胸痛 症状和疾病复发,以及心脏康复治疗。
症状和疾病复发,以及心脏康复治疗。
1.筛查肌纤维发育不良和其他动脉病变
肌纤维发育不良是一种特发性的动脉病变,常见于中等大小的血管,是最常见的与SCAD相关的疾病,在SCAD患者中肌纤维发育不良的患病率为25%-86%。与SCAD相关的其他动脉疾病包括马方综合征 、Loeys-Dietz综合征、血管型Ehlers-Danlos综合征、α-1抗胰蛋白酶
、Loeys-Dietz综合征、血管型Ehlers-Danlos综合征、α-1抗胰蛋白酶 缺乏症和多囊肾
缺乏症和多囊肾 病。建议对所有SCAD患者进行血管医学评估,包括全面的血管病史、体格检查和从脑部到骨盆的影像学检查。
病。建议对所有SCAD患者进行血管医学评估,包括全面的血管病史、体格检查和从脑部到骨盆的影像学检查。
2.监测胸痛症状和疾病复发
虽然SCAD患者的长期预后良好,但仍然存在慢性心绞痛 、复发性SCAD和非心源性胸痛的风险。要达到对患者的最佳管理,还需要有SCAD治疗经验的心脏病
、复发性SCAD和非心源性胸痛的风险。要达到对患者的最佳管理,还需要有SCAD治疗经验的心脏病 专家定期随访。
专家定期随访。
3.心脏康复治疗
心脏康复治疗是SCAD长期管理的一个重要组成部分,但尚未得到应有的重视。心脏康复对SCAD患者的身心健康有显著的短期和长期益处,而且是安全的。因此,研究者建议将所有稳定的SCAD患者转诊至心脏康复治疗。
有氧运动计划包括根据最初的运动压力测试,将训练设定在相当于50%-70%心率储备的目标心率区。心脏康复和有氧运动的参与频率应以每周至少3次,每次20-30分钟为起始点。此外,有SCAD病史的患者应避免肌肉等长收缩的阻力训练,且不应使用高强度的间歇训练方法。
问题与展望
一般而言,SCAD的治疗与动脉粥样硬化性ACS的治疗类似,但由于SCAD具有独特的病理生理学特征,临床医生应该考虑其他治疗策略。近年来,越来越多的观察性和回顾性研究对SCAD的优化管理有一定的帮助,但缺乏随机对照试验和侧重于SCAD管理的大规模前瞻性研究,且很少有研究报告夹层发生1年后的临床结局。由于缺乏有可信度的文献数据,SCAD的管理并不规范,相关临床指南在很大程度上仍然基于专家共识。
目前,还需要更多的前瞻性研究和随机对照研究数据来优化SCAD的治疗方案。对SCAD患者而言,DAPT的作用和持续时间、他汀类药物的使用以及血运重建的适应证和时机都尚未明确,需要进一步研究来提供循证依据。随着临床医生对SCAD认识的提高和血管造影 技术的进步,SCAD的诊断率可能会继续增长,亟需规范SCAD的诊疗流程。
技术的进步,SCAD的诊断率可能会继续增长,亟需规范SCAD的诊疗流程。
文献来源:Pristera N, Chaudhury P, Van Iterson EH, et al. Spontaneous coronary artery dissection: Principles of management. Cleve Clin J Med. 2021 Nov 2; 88(11): 623-630. doi: 10.3949/ccjm.88a.20162. PMID: 34728488.
