
从皮肤型红斑狼疮发生机制入手,探索治疗新方法 ▏综述速览
皮肤型红斑狼疮(CLE)是一种炎症性和自身免疫性皮肤病。根据CLE发生时有无系统性疾病参与,分为系统性红斑狼疮(SLE)相关CLE和原发性CLE。CLE病变具有异质性,但病变发展的驱动因素尚不明确。最近,学者对CLE发病机制的理解取得了一定的进展,有望改善患者的治疗方案。本文将讨论CLE流行病学、疾病分类、发病机制以及可能的治疗方向。
流行病学
CLE发生时伴或不伴全身性疾病受累,分别称为SLE相关CLE和原发性CLE。皮肤受累是SLE最常见的临床特征之一,高达70%的SLE患者出现皮肤受累。20%初始诊断为CLE的患者从原发性CLE发展为SLE。据估计,CLE的发病率约为0.04‰,但在某些人群中,其发病率与SLE相当。与SLE相似,CLE也具有性别差异,男女比例为1:3。与SLE发病率调查结果一致,美国黑人原发性CLE发病率高于白人个体,表明狼疮的发病具有种族差异。
CLE分类
CLE病变主要根据组织学发现、病变发展和存在的时间过程以及患者的临床特征进行分类。CLE有三个主要类型为:慢性CLE(CCLE)、急性CLE(ACLE)和亚急性CLE(SCLE)。CCLE亚组可进一步分为盘状红斑狼疮(DLE)、深在性红斑狼疮(LEP)、肿胀性红斑狼疮(LET)以及冻疮样红斑狼疮(CHLE)。其中DLE是CLE最常见的类型,病变通常局限于面部和头皮。DLE病变的光敏性稍低于其他亚型,但通常会导致疤痕、色素沉着变化和脱发。ACLE与SCLE均出现在身体的紫外线暴露部位。ACLE不会导致疤痕或色素沉着变化,SCLE会发生色素沉着变化,但病变不会形成瘢痕。
潜在致病机制
在CLE皮肤中,I型干扰素(IFN)的基础表达和紫外线(UV)诱导分泌均增加,并被认为在促进角质形成细胞死亡以及细胞因子诱导的扩增中发挥核心作用。在UV暴露后,角质形成细胞分泌IL-6、TNF-α和IL-1β促进炎性细胞浸润和病变发展,SLE中还发现趋化因子如CXCL9、CXCL10、CXCL11、CXCL12和CCL27的产生增强。这些趋化因子介导记忆和效应T细胞以及浆细胞 样树突状细胞(pDC)进入皮肤,导致炎症反应增强。此外,I型IFN对Foxp3+CD4+调节性T细胞(Treg)的抑制也有助于UV暴露后全身T细胞活化增强。总的来说,UV暴露下,DNA损伤、细胞死亡、自身抗原可及性以及细胞因子和趋化因子的增加均能促进皮肤炎症反应(图1)。
样树突状细胞(pDC)进入皮肤,导致炎症反应增强。此外,I型IFN对Foxp3+CD4+调节性T细胞(Treg)的抑制也有助于UV暴露后全身T细胞活化增强。总的来说,UV暴露下,DNA损伤、细胞死亡、自身抗原可及性以及细胞因子和趋化因子的增加均能促进皮肤炎症反应(图1)。
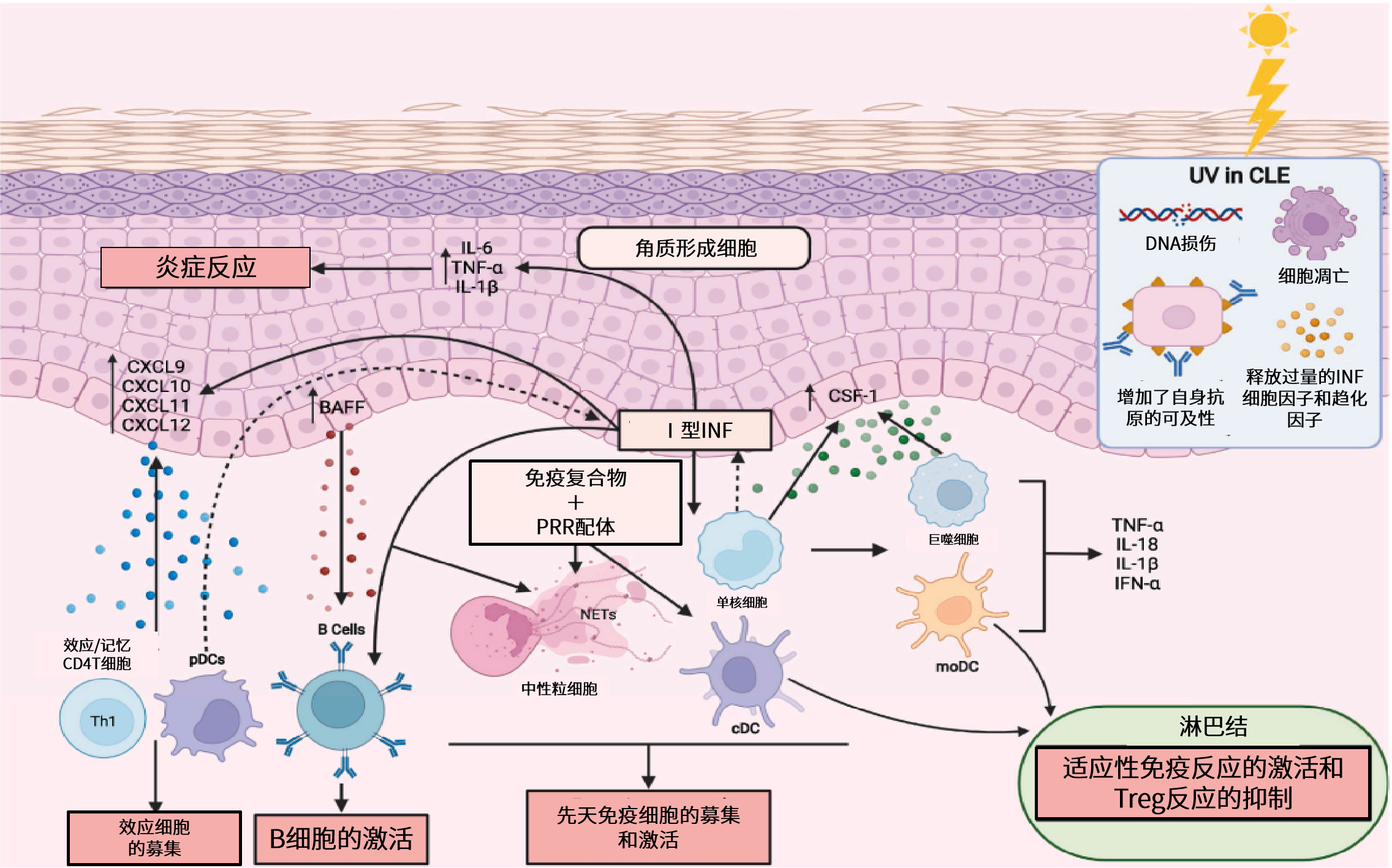
图1 皮肤中浸润性炎症细胞群、异常炎症和IFN反应之间的致病机制
1. 皮肤细胞异常
损伤的发展可能始于促炎性表皮,其条件是产生过量的I型干扰素(IFN),以及在紫外线照射后细胞死亡和炎性细胞因子产生增加。早期IFN失调在疾病发展中存在潜在作用,即I型IFN的表达增加可能使CLE中健康皮肤更易发展为病变皮肤。研究发现,在角质形成细胞和成纤维细胞中释放的I型和III型IFN,均能促进皮肤炎症反应。但目前缺乏研究证明成纤维细胞与皮肤型红斑狼疮的相关性。
2. 免疫细胞群异常
▶ B细胞和自身抗体:B细胞耐受性的丧失和自身反应性B细胞异常激活是SLE的发病机制之一,可由 IFN驱动。且循环B细胞表型可能作为CLE患者存在SLE风险的预后标志物。了解B细胞的异质性和B细胞在狼疮皮肤炎症中的作用对于开发针对性红斑狼疮的靶向治疗至关重要。
IFN驱动。且循环B细胞表型可能作为CLE患者存在SLE风险的预后标志物。了解B细胞的异质性和B细胞在狼疮皮肤炎症中的作用对于开发针对性红斑狼疮的靶向治疗至关重要。
▶ T细胞:T细胞在驱动CLE发病的机制中具有重要作用。CD8+T和CD4+T细胞在CLE发病机制中具有潜在作用,但确切机制有待进一步研究,且CD4+T细胞的特定亚群对病变炎症环境的影响仍存在争议。Treg是维持自身耐受性的关键,其可能成为预防紫外线暴露后皮肤炎症的治疗靶点,γδT细胞可能促进CLE皮肤中IFN的异常产生,但其在CLE发病机制中的作用有待进一步研究。虽然pDC也能促进I型INF产生,但这一发现受到新研究数据的质疑。单核细胞、树突状细胞、巨噬细胞、朗格汉斯细胞、中性粒细胞、肥大细胞以及嗜碱性细胞均在CLE发展中发挥作用,但他们的具体机制仍有待研究。此外,自然杀伤(NK)细胞被认为有助于CLE中的角质形成细胞死亡。
3. 光敏性
暴露于紫外线可触发小鼠模型和SLE患者的免疫细胞募集和皮肤损伤。紫外线照射在皮肤上引起的异常炎症反应,称为光敏性。剖析光敏性的原因是预防CLE的关键。 总的来说,DNA损伤和细胞死亡的增加,自身抗原可及性的增加,以及细胞因子和趋化因子的更高诱导,似乎对光敏皮肤中共同作用,导致了通常由紫外线暴露诱导的免疫抑制途径的重写。
潜在治疗药物
目前,FDA暂未批准用于治疗CLE的药物。对CLE致病机制进一步的了解,促进了越来越多涉及靶向上述途径和细胞的药物研究的发展。许多用于炎性疾病和SLE的药物(如抗疟药)能改善某些CLE损伤。anifrolumab可阻断I型IFN,从而显著改善CLE皮肤活性评分。阻断I型干扰素和其他细胞因子途径的其他口服JAK/STAT抑制剂、抑制pDC产生IFNα靶向血液DC抗原2(BDCA2)的抗体,均显示出改善CLE的治疗前景。靶向淋巴细胞转录因子Ikaros和Aiolos,降解Cereblon蛋白配体的iberdomide,也显示出改善SLE患者CLE皮肤活动性的作用。
结论
在过去十年中,学界对CLE的驱动因素有了更深的认识。对非损伤性皮肤的研究证实了一种涉及I型干扰素的慢性过度产生和持续的先天性炎性细胞募集的炎性表型,这为对紫外线等诱因产生异常反应提供了准备。适应性免疫途径的激活会引发更多的抗原特异性反应,从而导致进一步的组织损伤、纤维化,并可能导致系统性免疫激活。目前还未有FAD批准的专门针对CLE的疗法,所以需要进一步的研究以获得更好的、毒性更小的治疗方法来预防和治疗CLE损伤。
参考文献:Maz MP, Martens JWS, Hannoudi A, Reddy AL, Hile GA, Kahlenberg JM. Recent advances in cutaneous lupus[J]. J Autoimmun. 2022 Jul 17:102865. doi: 10.1016/j.jaut.2022.102865.PMID: 35858957.
