
梅恒教授:详细解读阿伐曲泊帕用于中国成人慢性ITP Ⅲ 期研究结果
阿伐曲泊帕 用于治疗成人慢性免疫性血小板减少症(immune thrombocytopenia, ITP)的上市申请已于2022年底获国家药品监督管理局药品审评中心(Center For Drug Evaluation, NMPA)正式受理。继先后被FDA和EMA获批用于成人ITP适应症后,阿伐曲泊帕用于中国成人慢性ITP患者Ⅲ期研究结果将助力其在国内ITP适应症获批。近期该研究结果在2023年EHA会议上公布,全文刊发在即。在此,特别荣幸邀请到本研究组长单位执行PI——梅恒教授深入解读《阿伐曲泊帕用于中国成人慢性ITP Ⅲ 期研究》。
用于治疗成人慢性免疫性血小板减少症(immune thrombocytopenia, ITP)的上市申请已于2022年底获国家药品监督管理局药品审评中心(Center For Drug Evaluation, NMPA)正式受理。继先后被FDA和EMA获批用于成人ITP适应症后,阿伐曲泊帕用于中国成人慢性ITP患者Ⅲ期研究结果将助力其在国内ITP适应症获批。近期该研究结果在2023年EHA会议上公布,全文刊发在即。在此,特别荣幸邀请到本研究组长单位执行PI——梅恒教授深入解读《阿伐曲泊帕用于中国成人慢性ITP Ⅲ 期研究》。
研究方法
本研究是一项在年龄≥18岁的中国成人慢性ITP患者中开展的评估阿伐曲泊帕疗效和安全性的中国多中心、随机双盲、安慰剂对照、扩展研究。研究将72例符合全部入排标准的受试者随机以2:1的比例给予阿伐曲泊帕或安慰剂治疗。起始剂量为20mg阿伐曲泊帕或安慰剂,每日给药一次。允许研究者根据受试者对研究药物的个体反应进行剂量滴定上调(阿伐曲泊帕或匹配的安慰剂,最大剂量每天40mg)或下调(阿伐曲泊帕或匹配的安慰剂,最小剂量每周20mg)。所有剂量调整的总体目标均是维持外周血小板计数在50×109/L-150×109/L水平之间。
主要疗效终点:治疗6周时的血小板反应率(定义如下:6周血小板反应率是指在无补救治疗情况下,治疗6周时血小板计数≥50×109/L的受试者比例;将缺失第6周血小板计数或在第6周前使用补救治疗的受试者视为血小板无应答者)。
研究结果
本研究共筛选103例受试者,29例受试者筛选失败,74例受试者筛选成功,阿伐曲泊帕组48例,安慰剂组26例。
1、主要终点
治疗6周时阿伐曲泊帕组应答率77.08%(37/48,95%CI:62.29-87.97),安慰剂组应答率7.69%(2/26,95%CI:0.95-25.13),p<0.001。
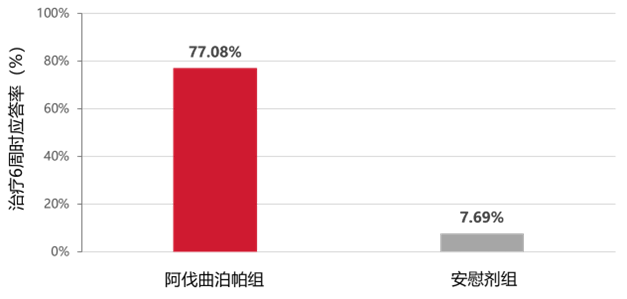
阿伐曲泊帕组和安慰剂组治疗6周时应答率
2、次要终点
① 治疗第8天时阿伐曲泊帕组应答率72.92%(35/48,95%CI:58.15-84.72),安慰剂组应答率3.85%(1/26,95%CI:0.10-19.64),p<0.001;
② 核心研究期内,阿伐曲泊帕组和安慰剂组累计应答中位时长分别为4.1周和0周,累计应答平均时长分别为3.5周和0.3周,均p<0.001;
③ 接受阿伐曲泊帕给药后5-14天,PLT较治疗前明显上升,随后PLT平稳,基本都维持在50×109/L以上;
④ 阿伐曲泊帕组21/48(43.75%)例受试者获得持久性血小板反应(在无补救治疗情况下,治疗时间段内至少≥75%时间血小板计数≥50×109/L),安慰剂组无;
⑤ 阿伐曲泊帕组43/48(89.6%)例受试者出现血小板反应,至出现血小板反应的中位时间为8.0(95% CI:8.0-9.0)天;安慰剂组 4/26(15.4%)例受试者出现血小板反应,因安慰剂组中事件数较少至血小板反应的中位时间未达到;
⑥ 核心研究期内两组暴露时间校正后的TEAEs(治疗期间出现的不良事件)发生率相当,其中阿伐曲泊帕暴露天数共计1386天,安慰剂暴露天数共计915天。
研究结论
本研究支持阿伐曲泊帕治疗中国成人慢性ITP受试者的疗效优于安慰剂。次要目标也已达成,针对次要疗效终点的分析也支持了主要疗效终点分析的结果。通过扩展阶段的研究,对阿伐曲泊帕长期治疗(合计26周)的有效性、安全性和耐受性结果也证明与国外关键性研究结果保持一致。

梅恒 教授
华中科技大学同济医学院附属协和医院 教授、主任医师、博士生导师、血液病研究所副所长
教育部青年长江学者
中华血液学会青年委员会副主任委员、血栓与止血学组副组长
中国研究型医院细胞研究与治疗委员会副主委员
湖北省临床肿瘤学会血液分会副主委
《British Journal of Haematology》副主编
主要从事血液肿瘤及出凝血疾病的临床与基础研究
主持科技部重点研发、湖北省杰青、国家自然科学基金等项目10余项
发表第一及通讯SCI 论文40余篇,授权发明专利3项
参编《血液病诊断及疗效标准》、参译《威廉姆斯血液学》
获国家科技进步二等奖1项,教育部及湖北省科技进步一等奖2项
审批号:NP-MA-20230608-CN-AVA-00003
本资讯旨在用于医学专业人士间的学术交流,请勿随意转发或转载。文中相关内容不能以任何方式取代专业的医疗指导。医学专业人士对文中提到的任何药品进行处方时,请严格遵循该药品在批准使用的说明书。

