
临研寻踪丨刘强教授谈T-DXd的漫漫征途,DESTINY-Breast系列研究概览
2022年3月,中国国家药品监督管理局(NMPA)药品审评中心(CDE)受理德曲妥珠单抗(T-DXd)的上市申请1,并在次年2月正式批准注射用德曲妥珠单抗 上市,适应证为治疗既往接受过一种或以上抗人表皮生长因子受体2(HER2)药物治疗的不可切除或转移性HER2阳性成人乳腺癌
上市,适应证为治疗既往接受过一种或以上抗人表皮生长因子受体2(HER2)药物治疗的不可切除或转移性HER2阳性成人乳腺癌 患者。这也标志着在全球肿瘤界备受瞩目的抗体药物偶联物(ADC)T-DXd正式进入我国临床实践。
患者。这也标志着在全球肿瘤界备受瞩目的抗体药物偶联物(ADC)T-DXd正式进入我国临床实践。
图1. T-DXd上市申请获CDE受理
该项获批基于DESTNY-Breast 03研究的主要结果,实际上,DESTNY-Breast系列研究(以下简称“DB研究”)是T-DXd在乳腺癌领域大获成功的关键所在。然而,对于一系列琳琅满目的DB研究该如何解读,每一项研究的目标、结果和结论是什么?很多读者朋友还是会一头雾水。今天,让我们一起跟随中山大学孙逸仙纪念医院刘强教授梳理DB系列研究,希望可以让您更加了解这一“闪闪发光”的HER2靶向ADC。
DB-01研究
初探HER2+乳腺癌后线治疗
DB-01是一项开放标签、单臂、多中心的II期临床研究,旨在评估T-DXd治疗既往接受恩美曲妥珠单抗 (T-DM1)治疗的HER2+、不可切除和/或转移性乳癌患者的疗效及安全性。主要研究终点是独立评审委员会(BICR)评估的客观缓解率(ORR),次要终点包括疾病控制率(DCR)、临床获益率(CBR)、缓解持续时间(DoR)、无进展生存期(PFS)、总生存期(OS)以及安全性。
(T-DM1)治疗的HER2+、不可切除和/或转移性乳癌患者的疗效及安全性。主要研究终点是独立评审委员会(BICR)评估的客观缓解率(ORR),次要终点包括疾病控制率(DCR)、临床获益率(CBR)、缓解持续时间(DoR)、无进展生存期(PFS)、总生存期(OS)以及安全性。
结果显示2,在中位既往治疗线达6线的情况下,184例患者接受5.4mg/kg剂量T-DXd治疗,ORR达到60.9%,DCR和CBR分别达97.3%和76.1%,中位DoR和PFS分别为14.8个月和16.4个月。安全性方面相对可控。
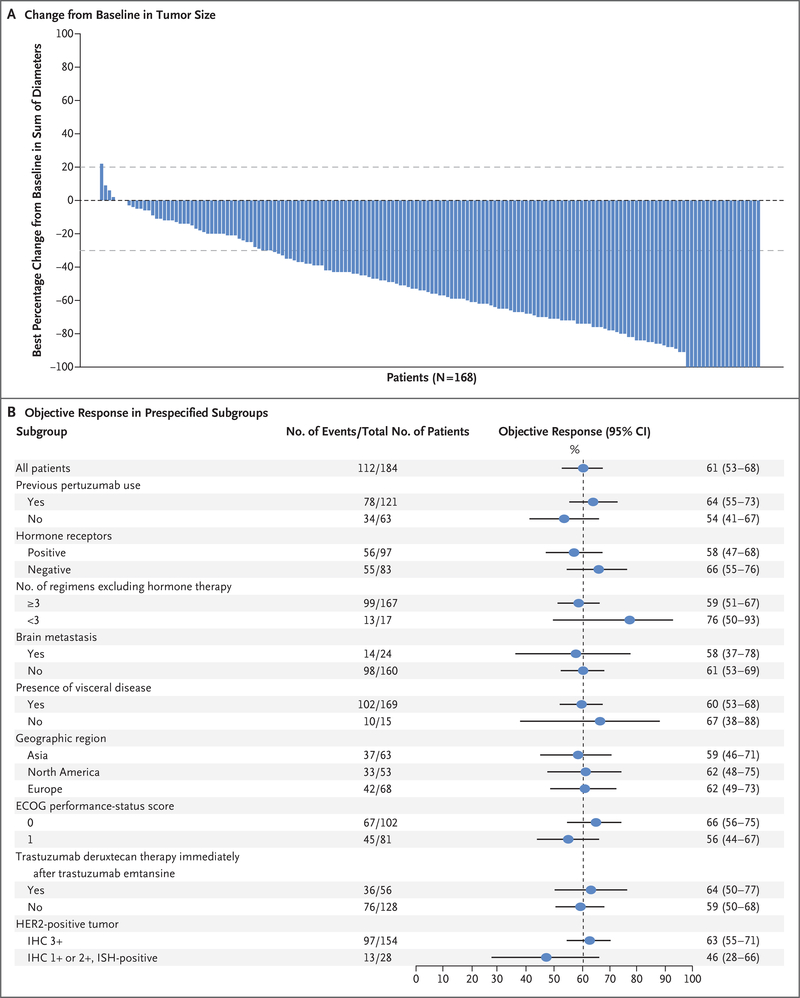
图2. DB-01研究主要结果:A. 自基线肿瘤大小变化,B. ORR亚组分析
DB-02研究
随机对照收获PFS和OS双阳
确证T-DXd为HER2+乳腺癌后线优效选择
DB-02是一项随机对照、多中心、开放性III期临床试验,旨在比较T-DXd与医生选择的治疗方案(TPC)的疗效和安全性。作为DB-01的确证性研究,DB-02同样纳入了T-DM1经治的不可切除或转移性HER2+乳腺癌患者,并按2:1随机分配至T-DXd组和TPC组,其中TPC组接受曲妥珠单抗联合卡培他滨 或拉帕替尼
或拉帕替尼 联合卡培他滨的治疗。主要研究终点为BICR评估的PFS,次要终点包括OS、ORR、DoR、研究者评估的PFS,以及探索性终点CBR和PFS2等。
联合卡培他滨的治疗。主要研究终点为BICR评估的PFS,次要终点包括OS、ORR、DoR、研究者评估的PFS,以及探索性终点CBR和PFS2等。
DB-02研究3共纳入608例患者HER2阳性晚期乳腺癌患者(T-DXd组 406例;TPC组 202例),结果显示,T-DXd组中位PFS为17.8个月,而TPC组为6.9个月,疾病进展或死亡风险降低了64%。
OS数据方面,T-DXd组患者的中位OS为39个月,TPC组中位OS为26.5个月,与TPC组相比,T-DXd组患者的死亡风险下降34%。T-DXd组的ORR为69.7%,显著高于TPC组的29.2%。
安全性上,因药物不良事件(AE)停止治疗的患者中,T-DXd组为14%,TPC组为5%。
DB-03研究
挑战标准,列席HER2+晚期乳腺癌二线优选治疗
DB-03是一项随机对照、多中心、开放性III期试验,旨在比较T-DXd与T-DM1二线治疗HER2阳性转移性乳腺癌的疗效和安全性。研究纳入既往接受过曲妥珠单抗和紫杉类药物治疗的HER2阳性不可切除和/或转移性乳腺癌患者,按1:1随机接受T-DXd(5.4mg/kg q3w)或T-DM1(3.6mg/kg q3w)治疗。主要终点为BICR评估的PFS,关键次要终点为OS。
研究4共纳入524例患者(T-DXd组 261例;T-DM1组 263例),T-DXd组12个月PFS率为75.8%,T-DM1组为34.1%。T-DXd组12个月OS率为94.1%,T-DM1组为85.9%。接受T-DXd治疗的患者ORR达79.7%,而T-DM1为34.2%。T-DXd组和T-DM1组的药物相关AE发生率分别为98.1%和86.6%,3-4级药物相关AE发生率分别为45.1%和39.8%。
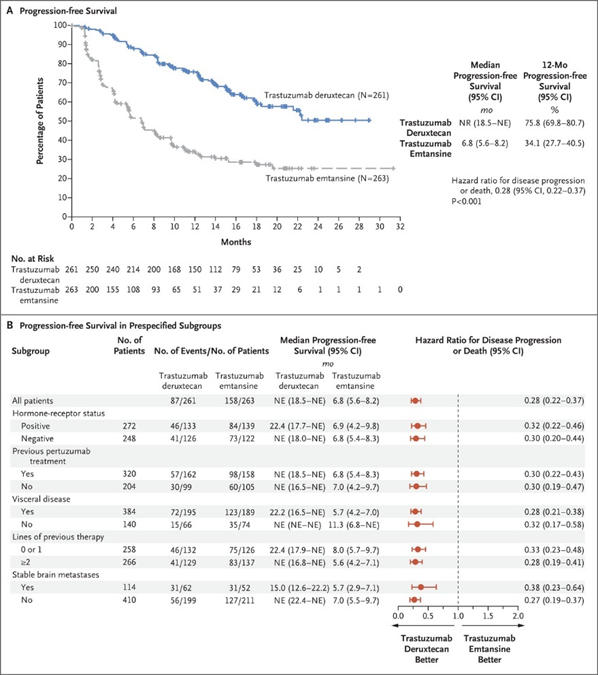
图3. DB-03主要结果:A. PFS K-M曲线;B. PFS的亚组分析
DB-04研究
扩大战场,试水HER2低表达乳腺癌群体
DB-04研究是一项开放标签、多中心、随机对照III期临床试验5,旨在评价T-DXd对比TPC方案用于HER2低表达晚期乳腺癌的疗效和安全性。纳入既往接受过1-2线化疗的激素受体(HR)+或HR-、HER2低表达的不可切除和/或转移性乳腺癌患者,按2:1随机分入T-DXd组或TPC组(卡培他滨、艾立布林 、吉西他滨
、吉西他滨 、紫杉醇
、紫杉醇 或白蛋白结合型紫杉醇)。主要终点是BICR评估的HR+队列的PFS。
或白蛋白结合型紫杉醇)。主要终点是BICR评估的HR+队列的PFS。
在接受随机分组的557例患者(T-DXd组 373例;TPC组 184例)中,494例(88.7%)为HR+,在该队列中,T-DXd组的中位PFS为10.1个月显著长于TPC组的5.4个月。中位OS方面,T-DXd组为23.9个月,TPC组为17.5个月。在全人群中,T-DXd组的中位PFS为9.9个月,TPC组为5.1个月。中位OS分别为23.4个月和16.8个月。安全性方面,T-DXd组≥3级AE发生率为52.6%,TPC组为67.4%。
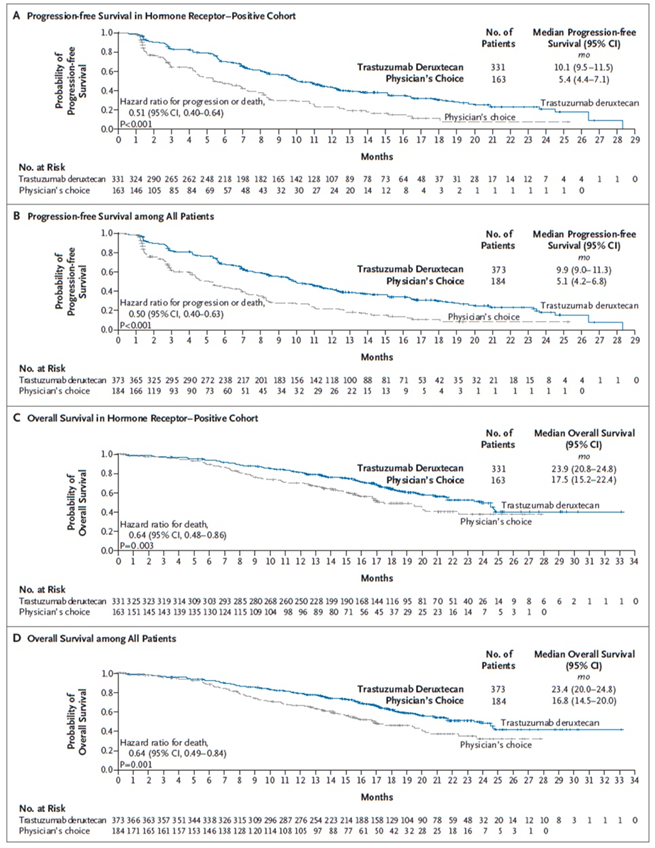
图4. DB-04研究结果:A. HR+队列PFS;B. HR+队列OS;C. 全人群PFS;D. 全人群OS
DB-05研究
挑战早期HER2+辅助强化治疗标准,期待更多治愈
DB-05是一项多中心、开放标签、随机、III期临床试验6,旨在比较HER2+、伴侵袭性疾病、且新辅助治疗后乳腺或腋窝淋巴结残留浸润性病变病理证据的乳腺癌患者中,T-DXd与T-DM1的疗效和安全性。患者入组后以1:1随机分配到T-DXd组或T-DM1组。主要终点为基于研究者评估的无侵袭性疾病生存期(iDFS),次要终点包括OS、无病生存期(DFS)、远处无复发间期和无脑转移间期。
该研究尚在进行,期待更多数据公布。
DB-06研究
再低也有用,进一步拓展HER2超低表达群体
DB-06是一项随机、多中心、开放标签III期临床试验,旨在比较T-DXd与TPC(卡培他滨、紫杉醇或白蛋白结合型紫杉醇)在HR+、HER2-low(IHC 1+或2+/ISH-)或HER2-ultralow(定义为IHC 0伴有膜染色:即IHC >0<1+)晚期或转移性乳腺癌患者中的疗效和安全性。主要终点为BICR评估的HR+、HER2-low患者群体的PFS,次要终点包括OS、总人群PFS等。
2024 ASCO大会中,DB-06首次公布数据7,研究共纳入866例患者(T-DXd组 436例;TPC组430例),其中,HER2-low患者713例,HER2-ultralow患者153例。HER2-low队列中,T-DXd组中位PFS达到13.2个月,TPC组仅为8.1个月,显著降低疾病进展或死亡风险达38%。HER2-ultralow队列中,PFS获益与HER2-low人群一致,T-DXd组中位PFS为13.2个月,TPC组为8.3个月。安全性方面,T-DXd组和TPC组治疗期间不良事件(TEAE)发生率分别为96.1% vs 89.4%,≥3级治疗相关TEAEs发生率分别为40.6% vs 31.4%。
DB-07研究
HER2+乳腺癌的ADC联合治疗模式初步探索
DB-07是一项多中心、开放标签、多队列Ib/II期临床研究,旨在探索T-DXd单药或与其他抗肿瘤药物联合治疗的安全性、耐受性和抗肿瘤活性。主要终点为安全性和耐受性;关键次要终点包括研究者根据RECIST 1.1评估的ORR和PFS。
2024 ASCO大会披露的数据显示8,截至2023年12月22日,研究共入组125例患者(T-DXd单药组 75例;T-DXd+帕妥珠单抗 联合组 50例),其中单药组与联合组分别有64%及60%为初诊IV期患者。在疾病缓解方面,单药组和联合组的确认的ORR分别为76.0%和84.0%,12个月的PFS率分别为80.8%和89.4%。在安全性方面,单药组与联合组≥3级AE发生率分别为52%和62%,最常见的AE为消化道反应及中性粒细胞减少。
联合组 50例),其中单药组与联合组分别有64%及60%为初诊IV期患者。在疾病缓解方面,单药组和联合组的确认的ORR分别为76.0%和84.0%,12个月的PFS率分别为80.8%和89.4%。在安全性方面,单药组与联合组≥3级AE发生率分别为52%和62%,最常见的AE为消化道反应及中性粒细胞减少。
DB-08研究
HER2低表达乳腺癌的ADC联合治疗模式初步探索
DB-08是一项多中心,开放标签,两部分,模块化1b期研究,旨在评估T-DXd与广泛使用的标准疗法联合治疗HR+、HER2低表达转移性乳腺癌的安全性、耐受性和初步抗肿瘤活性。联合治疗方案包括卡培他滨、度伐利尤单抗 +紫杉醇、AKT抑制剂capivasertib、阿那曲唑
+紫杉醇、AKT抑制剂capivasertib、阿那曲唑 与氟维司群
与氟维司群 。主要研究终点是安全性和耐受性;次要终点包括ORR、PFS、DoR和OS。
。主要研究终点是安全性和耐受性;次要终点包括ORR、PFS、DoR和OS。
2023年第46届圣安东尼奥乳腺癌研讨会(SABCS)上公布了DB-08研究中T-DXd联合阿那曲唑与氟维司群队列的初步结果9。数据显示,T-DXd+阿那曲唑组和T-DXd+氟维司群组的AE发生率分别为95.2%和100%,其中,≥3级AE发生率分别为47.6%和55.0%。通过中断用药和减少剂量,AE均可得到控制。疗效方面,T-DXd+阿那曲唑组的ORR为71.4%,T-DXd+氟维司群组为40.0%。T-DXd+阿那曲唑组治疗组的中位PFS和中位DoR分别为13.4个月和9.8个月,T-DXd+氟维司群组暂无法评估。T-DXd+阿那曲唑组6个月和12个月的PFS率分别为80.7%和50.4%,T-DXd+氟维司群组为75.3%和52.7%。
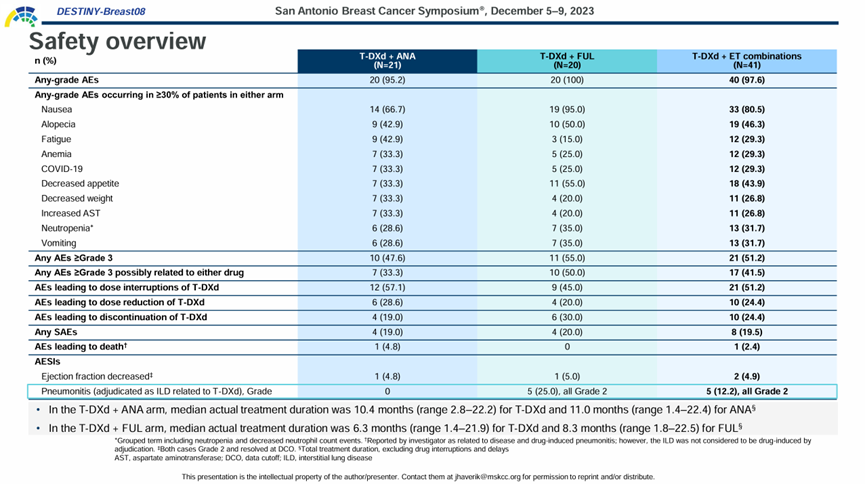
图5. DB-08研究安全性结果
DB-09研究
挑战晚期一线HER2+乳腺癌治疗标准THP方案
DB-09是一项全球性、多中心、随机III期临床试验10,旨在比较T-DXd联合或不联合帕妥珠单抗与标准治疗方案紫杉类+曲妥珠单抗+帕妥珠单抗(THP)作为一线治疗HER2+晚期或转移性乳腺癌患者的疗效和安全性。入组患者按照1:1:1随机分配至A组(T-DXd+安慰剂)、B组(T-DXd+帕妥珠单抗)和C组(THP)。主要终点是BICR评估的PFS。次要终点包括研究者评估的PFS、OS、ORR、DoR、PFS2、健康相关生活质量(QOL)、药代动力学、免疫原性和安全性。
截止目前,DB-09研究尚无公开结果报道。
DB-11研究
全线布局,探索“去蒽”新辅助治疗方案
DB-11研究是是开放标签的III期临床研究11,旨在探讨针对高危HER2+早期乳腺癌患者的新辅助T-DXd单药治疗或T-DXd后序贯THP对比剂量密集型多柔吡星和环磷酰胺 序贯THP方案(ddAC-THP)的疗效与安全性。纳入HR+或HR-的HER2+局部晚期乳腺癌患者,按1:1:1分别分配至A组(T-DXd单药)、B组(T-DXd序贯THP)、C组(ddAC-THP)。主要终点为病理完全缓解(pCR)。
序贯THP方案(ddAC-THP)的疗效与安全性。纳入HR+或HR-的HER2+局部晚期乳腺癌患者,按1:1:1分别分配至A组(T-DXd单药)、B组(T-DXd序贯THP)、C组(ddAC-THP)。主要终点为病理完全缓解(pCR)。
目前,DB-11研究尚在进行。
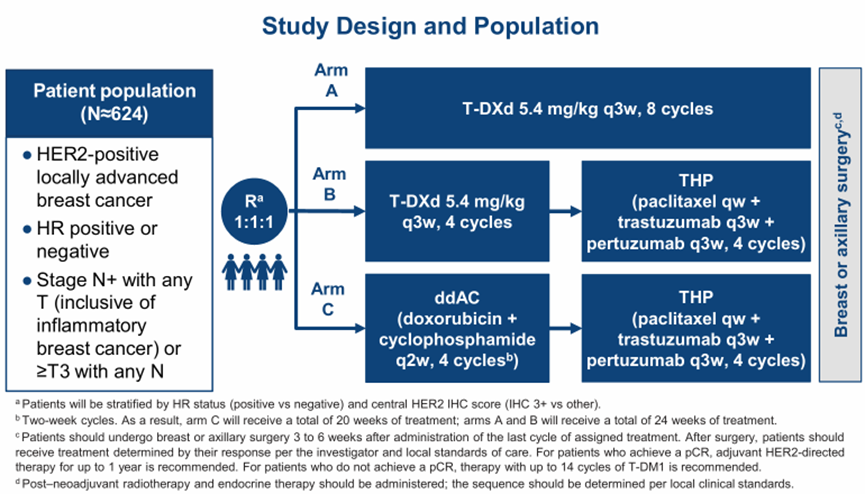
图6. DB-11研究设计
DB-12研究
大样本评估T-DXd在HER2+乳腺癌伴脑转移患者中的疗效
DB-12是一项开放标签、国际多中心的IIIb/IV期研究12,旨在评估T-DXd(5.4mg/kg q3w)在伴或不伴脑转移的HER2+乳腺癌患者中的疗效和安全性。纳入的HER2+乳腺癌患者按照基线处是否伴脑转移进行分组(队列1:不伴脑转移;队列2:伴脑转移)。主要研究终点是队列1的ORR和队列2的PFS。次要终点是OS、DoR、进展时间、后续治疗持续时间、PFS2、安全性等等。
目前,DB-12研究尚在进行。
【刘强教授深度点评】
T-DXd取得了非常大的成功,得益于药物机制方面的改进。T-DXd通过优化四肽连接子技术,链间采用半胱氨酸偶联,有效降低整体ADC药物的疏水性,实现药物抗体比(DAR)达到理论高值8,突破了传统ADC药物2-4的限制。同时,T-DXd具有较好的均一性,既减少了DAR低的ADC分子对靶点的无效占据,又保证了药物在体内分布、代谢等药代动力学特性的稳定。T-DXd的药物设计将靶向药的精准和化疗药的高效进行了优化组合,使其具有更高的药载比、特殊的偶联结构和旁观者杀伤效应,既降低了药物的毒副作用,还增强了杀伤肿瘤的能力,这些都是T-DXd取得众多关键性突破的基础。
T-DXd是一个具有划时代意义的新型ADC药物,DESTINY-Breast系列研究取得了众多突破进展。在HER2+、低表达、超低表达乳腺癌领域,从后线治疗到三线治疗、二线治疗、一线治疗节节推进,显示了令人惊艳的疗效,特别是DB-03研究确立了二线治疗新标准,DB-04研究也是首个在HER2低表达乳腺癌中获得成功的大型III期试验,使HER2阳性乳腺癌“两分法”推进至“三分法”,为更多乳腺癌患者带来更为适宜的治疗选择。值得一提的是,在今年ASCO大会上,DB-06研究对HER2低表达分类进一步细化,引入“HER2-ultralow”概念,成功入选LBA,成为最具开创性、最备受瞩目的研究之一,将为既往未接受过化疗的患者提供了一个新的治疗机会,有望改变目前的临床实践。
DB系列研究全面覆盖于乳腺癌治疗中的多个阶段,随着研究的进行和数据的不断公布,有望进一步丰富乳腺癌的治疗模式,树立新的治疗标准,刷新乳腺癌的治疗格局。期待更多研究数据的公布,为乳腺癌治疗带来夯实的循证医学证据,为我国乳腺癌临床实践带来强有力的治疗新选择,造福更多乳腺癌患者。


