
2024 ESMO Asia | LITESPARK-005试验聚焦东亚地区患者,探索贝组替凡在晚期ccRCC中的疗效与安全性
2024年欧洲肿瘤内科学会亚洲年会(ESMO Asia 2024)于当地时间12月6日至8日在新加坡召开,各领域肿瘤大咖将齐聚新加坡共探肿瘤学领域的最新科学和临床研究,以进一步推动临床肿瘤学的发展。本届大会中的Proffered Paper session环节汇报了一篇关于LITESPARK-005 III期临床试验的亚组分析研究,该研究主要针对东亚地区晚期肾透明细胞癌(ccRCC)患者进行分析,评估其分别接受贝组替凡和依维莫司 治疗的疗效。医脉通编译如下,以飨读者。
治疗的疗效。医脉通编译如下,以飨读者。
LBA2
Belzutifan versus everolimus for previously treated advanced clear cell renal cell carcinoma (ccRCC): Updated follow-up of the East Asian subgroup of the randomized phase III LITESPARK-005 trial
研究背景
LITESPARK-005研究(NCT04195750)是一项III期临床随机试验,在接受抗PD-(L)1和VEGF-TKI治疗或治疗后病情进展的全球晚期ccRCC患者中,与依维莫司相比,贝组替凡改善了患者的无进展生存期(PFS)和客观缓解率(ORR)。在本次大会中,该研究提供了LITESPARK-005试验东亚亚组的最新随访结果。
研究方法
接受1-3个全身系统性治疗方案的晚期ccRCC患者(东亚地区)按1:1比例,被随机分配到贝组替凡组(120mg,口服,每日一次)和依维莫司组(10mg,口服,每日一次)。主要研究终点为评估患者的PFS和总生存期(OS)。关键次要研究终点为评估患者的ORR。其他次要研究终点为评估反应持续时间(DOR)和安全性。
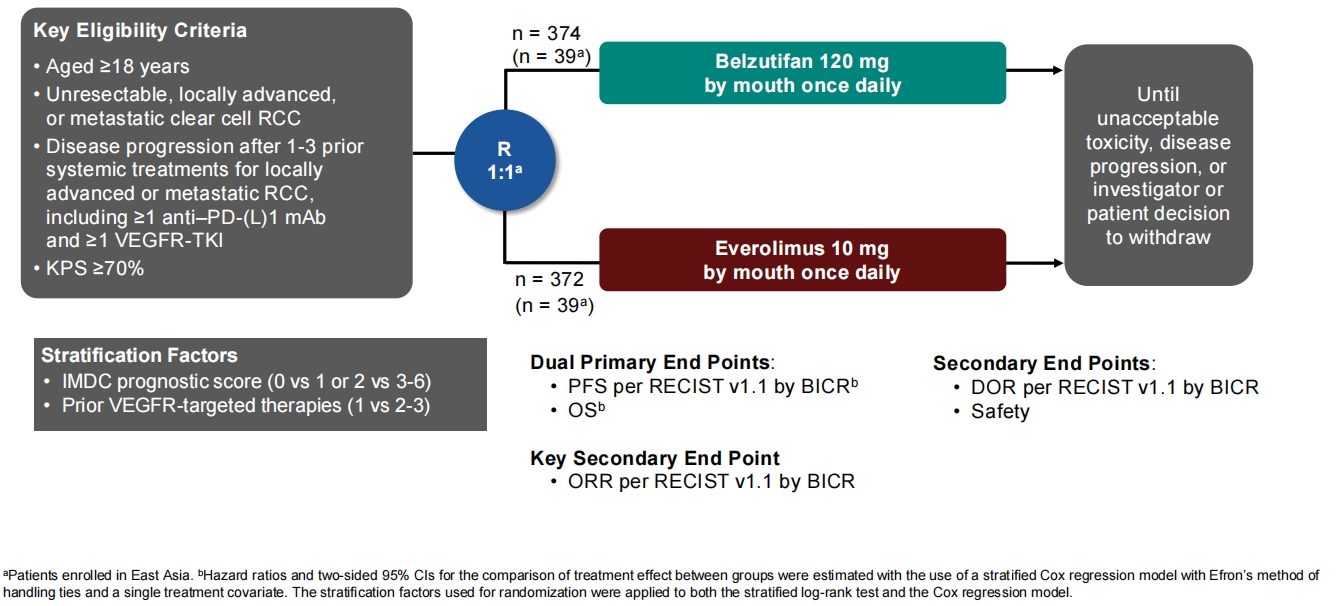
图1 研究设计
研究结果
该亚组分析共计纳入78例患者(每组各39例)。截止至2024年4月15日,中位随访时间为33.4个月(26.9个月-44.2个月)。截至数据截止日期,约30%的患者正在接受贝组替凡治疗,3%的患者正在接受依维莫司治疗(图2),患者基线特征详见表1。
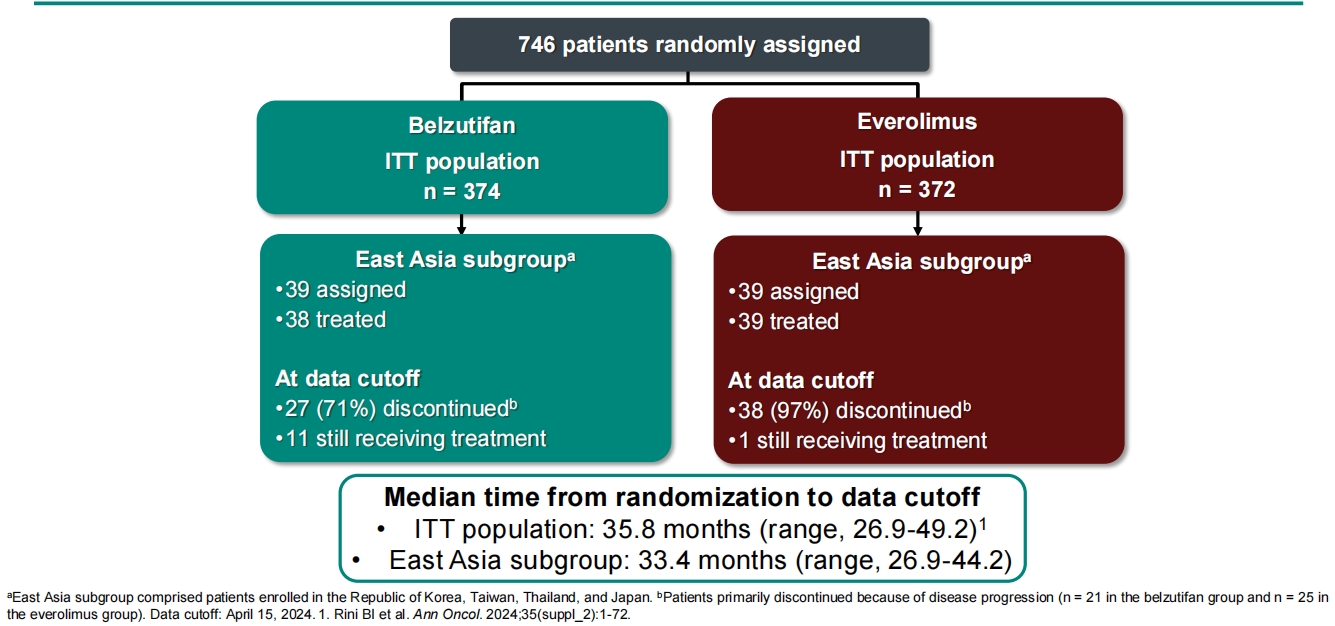
图2 配对图
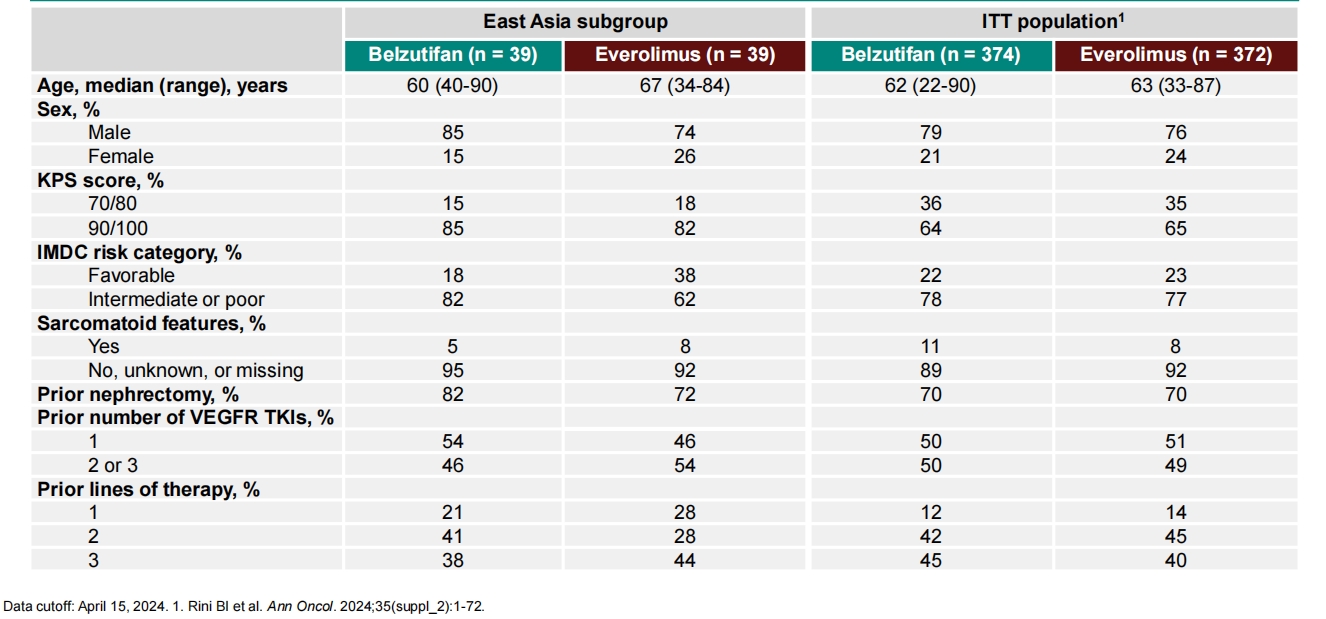
表1 患者基线特征
主要研究终点
贝组替凡组的中位PFS为7.5个月,依维莫司组中位PFS为5.7个月(HR,0.54;95% CI, 0.30-0.98);第24个月贝组替凡组和依维莫司组PFS率分别为30%和4%。
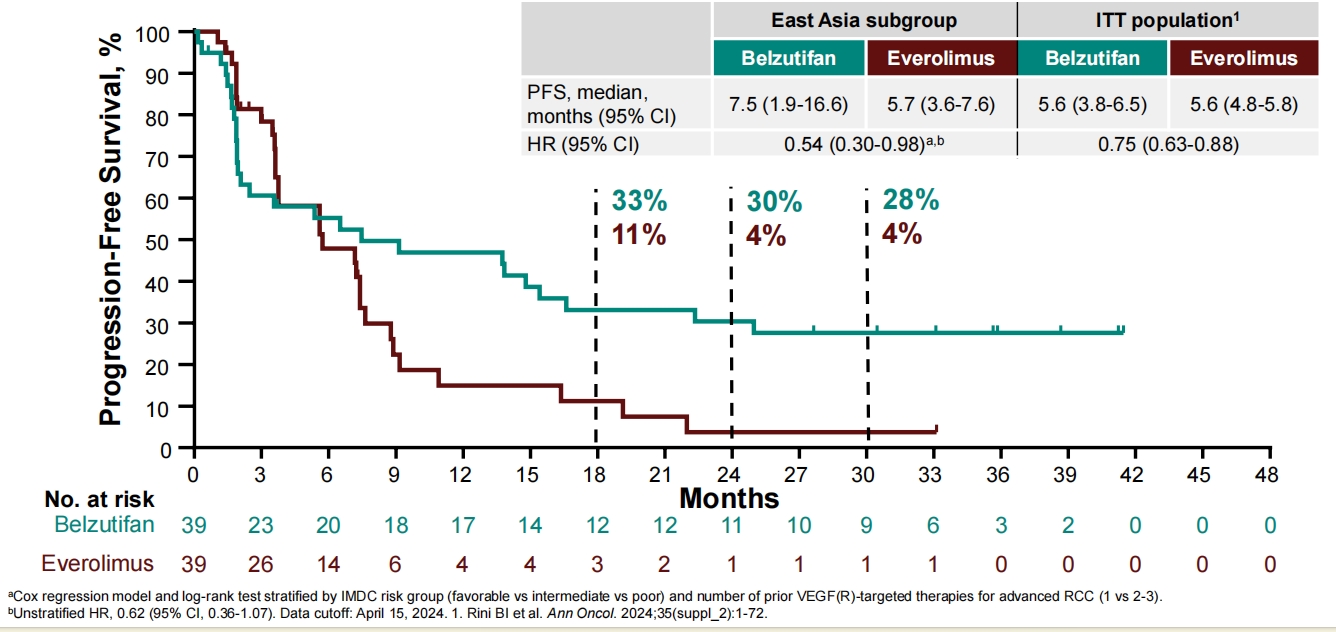
图3 PFS(东亚亚组)
贝组替凡组中位OS为29.7个月,依维莫司组中位OS为30.8个月(HR,0.76;95% CI,0.39-1.46);第24个月,贝组替凡组和依维莫司组患者达到OS的比例分别为59%和56%。
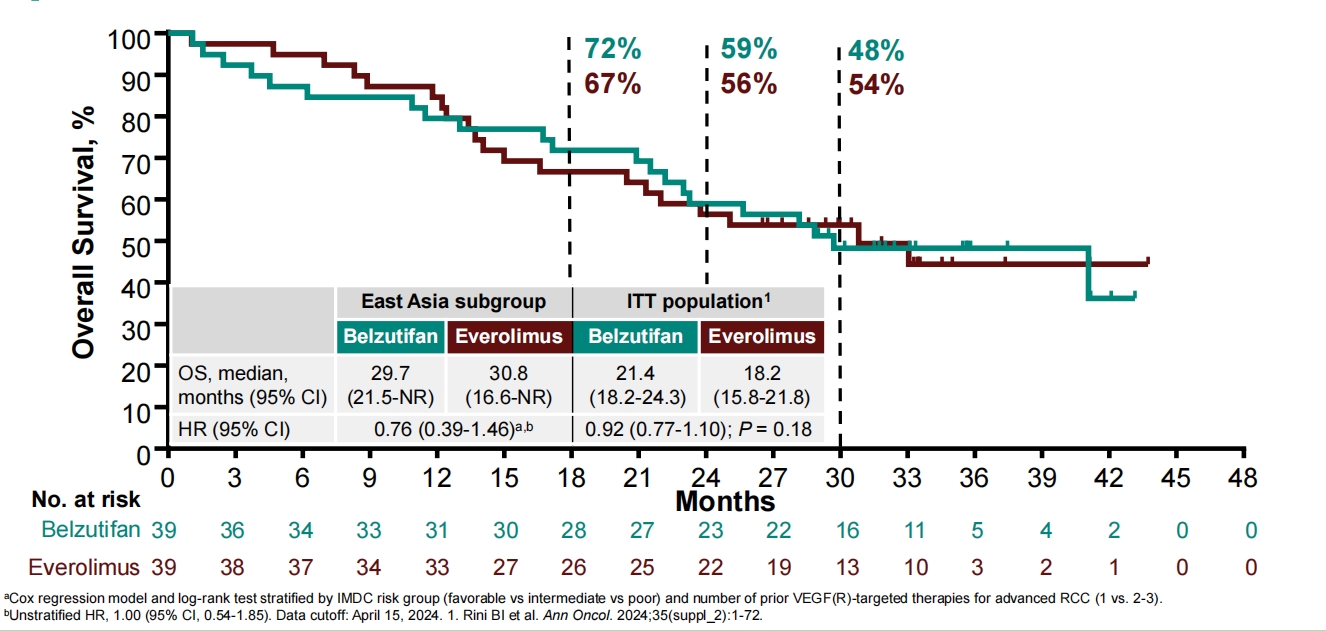
图4 OS(东亚亚组)
关键次要研究终点
ORR与既往研究结果保持一致,贝组替凡组和依维莫司组ORR分别为30.8%和0%。
表2 ORR及最佳总体疗效率(东亚亚组)
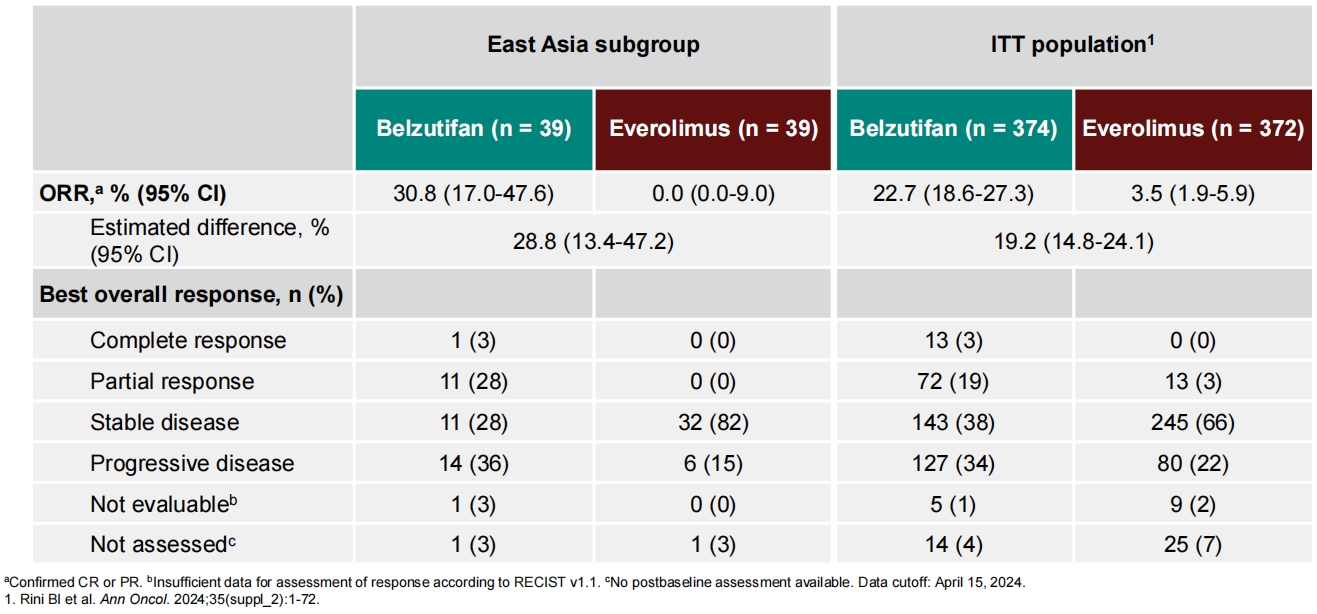
次要研究终点
贝组替凡组未达到中位DOR(图5)。
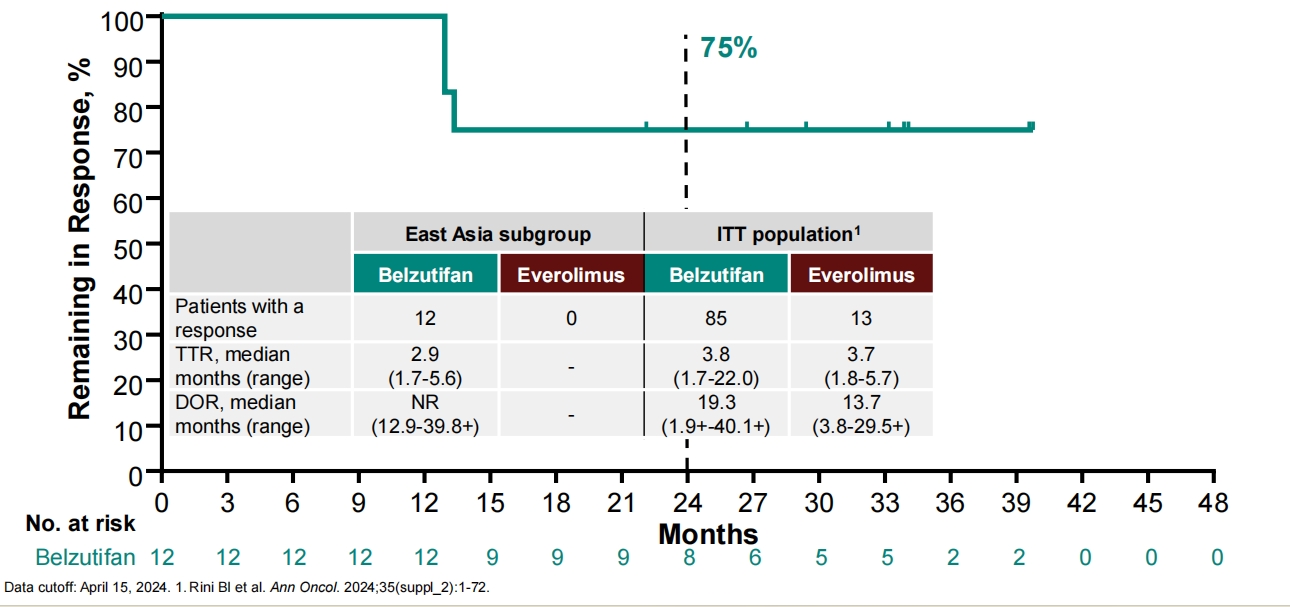
图5 DOR(东亚亚组)
安全性:1例患者因全因不良事件停用贝组替凡,7例患者因全因不良事件停用依维莫司。贝组替凡组53%的患者和依维莫司组33%的患者发生了3-5级治疗相关不良事件。
表3 不良事件(东亚亚组)
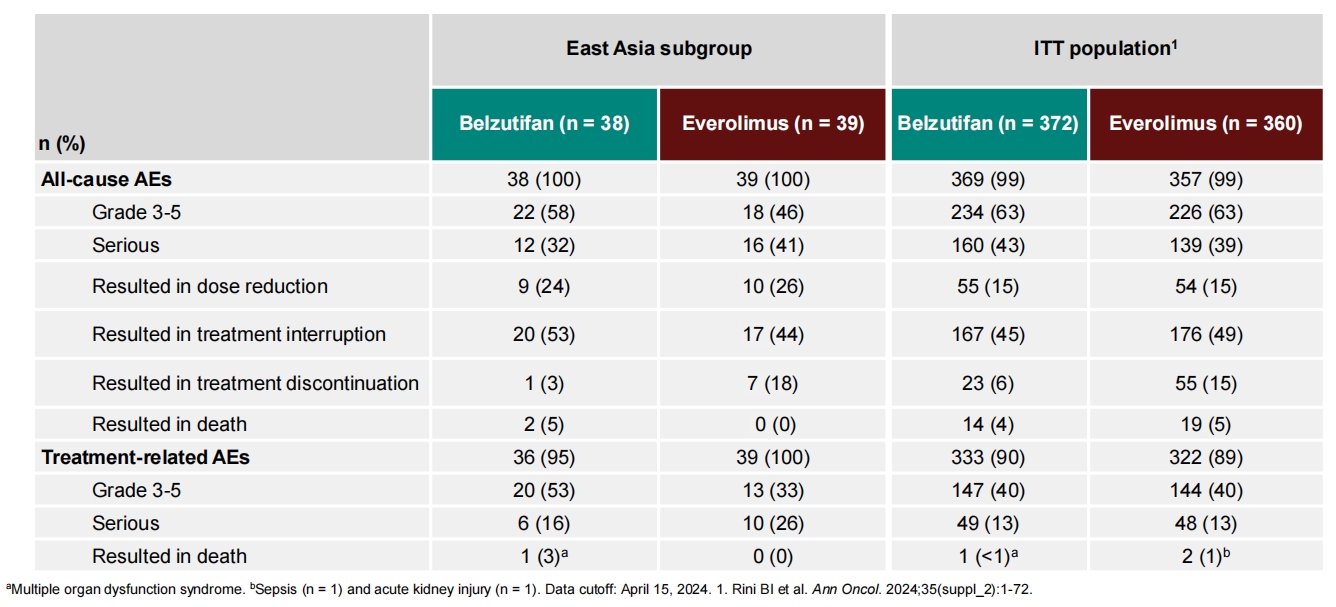
研究结论
LITESPARK-005试验针对东亚地区患者进行了至少为期2年的随访,研究结果显示,接受贝组替凡治疗的晚期ccRCC患者的PFS和ORR结局得到改善。该亚组分析的安全性结局也与之前的全球数据保持一致。该亚组分析结果支持贝组替凡作为东亚地区晚期ccRCC患者在接受抗PD-(L)1和VEGF-TKI治疗后出现病情进展的另一种潜在治疗方案。
参考文献
1.Lee JL,,et al.Belzutifan versus everolimus for previously treated advanced clear cell renal cell carcinoma (ccRCC): Updated follow-up of the East Asian subgroup of the randomized phase III LITESPARK-005 trial.2024 ESMO Asia.Abstract Number:LBA2.
