
2025 EHA速递 | 杜鹃教授: MRD驱动的多发性骨髓瘤诊疗新策略:IsKia研究MRD持续阴性率结果公布
随着多发性骨髓瘤 (MM)治疗的进展,越来越多的MM患者能够取得深度缓解,而是否获得微小残留病(MRD)阴性逐渐成为重要的动态预后因素[1],同时实现骨髓和影像学MRD阴性的患者具有最佳的生存结局[2-3]。此前IsKia研究[4]结果已证实艾沙妥昔单抗
(MM)治疗的进展,越来越多的MM患者能够取得深度缓解,而是否获得微小残留病(MRD)阴性逐渐成为重要的动态预后因素[1],同时实现骨髓和影像学MRD阴性的患者具有最佳的生存结局[2-3]。此前IsKia研究[4]结果已证实艾沙妥昔单抗 (Isatuximab)联合卡非佐米
(Isatuximab)联合卡非佐米 、来那度胺
、来那度胺 和地塞米松
和地塞米松 (Isa-KRd)方案对比KRd方案可显著提升新诊断多发性骨髓瘤(NDMM)患者的MRD阴性率,本次EHA大会进一步展示了此研究1年持续MRD阴性率及减量巩固阶段的结果,再次证明KRd联合CD38单抗方案在实现MRD阴性率方面的疗效[5]。医脉通血液肿瘤科特邀杜鹃教授对该研究进行解读与点评。
(Isa-KRd)方案对比KRd方案可显著提升新诊断多发性骨髓瘤(NDMM)患者的MRD阴性率,本次EHA大会进一步展示了此研究1年持续MRD阴性率及减量巩固阶段的结果,再次证明KRd联合CD38单抗方案在实现MRD阴性率方面的疗效[5]。医脉通血液肿瘤科特邀杜鹃教授对该研究进行解读与点评。
【S208】Analysis of sustained MRD negativity in patients with newly diagnosed multiple myeloma treated with carfilzomib-lenalidomide-dexamethasone with or without Isatuximab (phase III IsKia trial)
卡非佐米-来那度胺-地塞米松联合或不联合艾沙妥昔单抗治疗新诊断多发性骨髓瘤患者中持续微小残留病(MRD)阴性的分析(III期 IsKia研究)
研究背景和目的
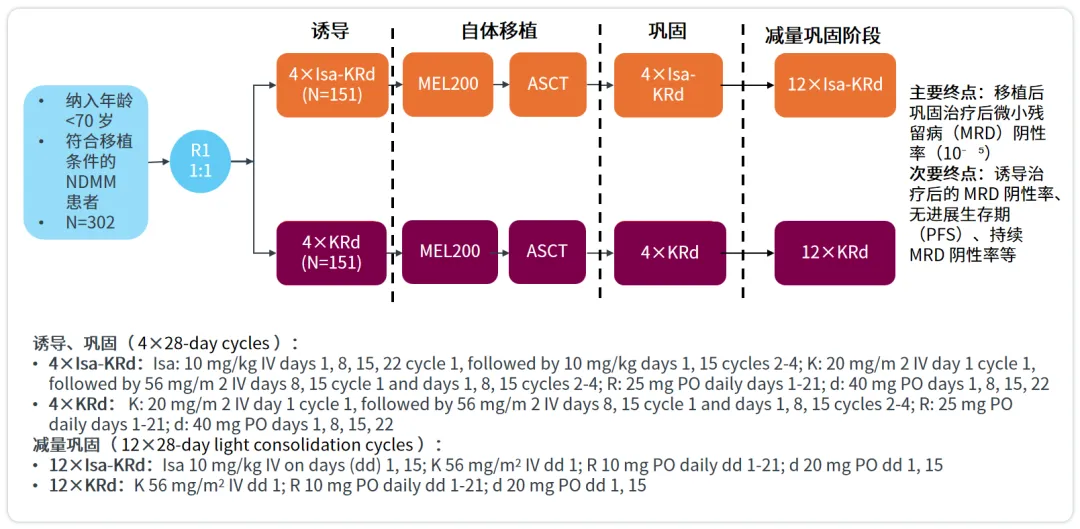
IsKia研究(NCT04483739)是一项针对NDMM患者的III期试验,旨在评估Isa-KRd方案与KRd方案在移植前诱导治疗和移植后巩固治疗中的疗效和安全性。此前的研究结果显示Isa-KRd组在诱导和巩固治疗后的MRD阴性率显著高于KRd组。本次EHA大会公布内容重点是1年持续MRD阴性率及减量巩固阶段的结果。
研究方法
研究纳入了年龄小于70岁且适合移植的NDMM(TE NDMM)患者,数据截至2024年7月22日。达到≥VGPR的患者均通过NGS评估MRD状态。1年持续MRD阴性定义为两次连续MRD阴性评估至少间隔1年。分析遵循意向治疗(ITT)原则,缺失MRD数据或未达到VGPR的患者均视为MRD阳性。
研究结果
共纳入302例患者随机分为两组各151例,基线特征均衡。中位随访35个月后,巩固治疗后Isa-KRd组MRD阴性率(10⁻⁵)为77%,高于KRd组的67%(p=0.049);MRD阴性率(10⁻⁶)两组分别为67%和48%(p<0.001)。减量巩固治疗后,1年持续MRD阴性率(10⁻⁵)分别为66%和59%(p=0.21);MRD阴性率(10⁻⁶)分别为52%和38%(p=0.012)。在携带≥2种高危细胞遗传学异常的患者中,Isa-KRd组1年持续MRD阴性率(10⁻⁶)为62%,显著高于KRd组的20%(p<0.05)。安全性方面,Isa-KRd组与KRd组的3-4级不良事件发生率相近,因毒性终止治疗比例分别为3%和2%,治疗相关死亡分别为2例和0例。
研究结论
NDMM患者中KRd联合艾沙妥昔单抗方案诱导-巩固治疗以及延长的减量巩固治疗显著提升了MRD(10⁻⁶)持续阴性率,且未发生新的安全性问题,同时这一优势在高危患者中也得到了体现。
杜鹃教授点评
过去20年中蛋白酶体抑制剂(PIs)、免疫调节剂(IMiDs)和单克隆抗体等药物的广泛应用显著延长了MM患者的生存期。随着检测技术的进步MRD的疗效评估与监测为患者治疗管理提供了新契机,大量证据表明MRD状态在评估患者治疗反应及预后方面具有重要价值。国际多发性骨髓瘤微小残留病终点审批独立团队(I2TEAMM)发起的荟萃分析以及Sylvester癌症中心发起的EVIDENCE荟萃分析结果显示:MM患者若在治疗第一年达到MRD阴性状态则可作为显著临床获益的预测指标[6-7],因此MRD阴性已成为重要的动态预后因素。
本届EHA大会上除IsKia研究的持续MRD阴性率数据外,多项研究公布和更新了MRD相关结果,如GMMG-CONCEPT研究(Isa-KRd方案)全队列MRD阴性率(10⁻⁵)达73.2%(此前公布的部分队列为67.7%)[8-9]; PERSEUS研究(DVRd VS VRd)本次公布的结果两组MRD阴性率(10⁻⁵)分别为64.8%、29.7%(≥12个月)[10-11]; 此外公布的一项Ⅱ期研究(DKRd VS KRd)8个周期诱导治疗后两组MRD阴性率(10⁻⁵)分别为59%和36%[12];一项基于MRD状态调整巩固及维持治疗策略的Ⅲ期研究采用Isa-KRd方案诱导治疗,四组MRD阴性率(10⁻⁶)分别为84%、86%、40%和32%[13],这几项研究的更新数据均显示经Isa-KRd、DKRd和DVRd方案治疗可获得较高的MRD阴性率,进一步探索MRD阴性在TE NDMM人群中的应用,为后续的治疗策略提供依据。
上述研究证实MRD阴性在MM治疗中的重要性,还可能成为未来治疗策略的重要终点。尽管各研究数值存在差异,但均证实以PIs和IMiDs为基石的药物,联合地塞米松、CD38单抗的治疗方案,在MRD阴性状态指导下追求深度缓解为TE NDMM患者提供了新的治疗策略。不过这些研究存在一定局限性,例如部分研究的MRD持续阴性数据及PFS数据尚未成熟,不同研究队列在患者基线特征、治疗方案选择及MRD检测技术标准上存在差异,因此基于MRD状态的指导策略有效性需通过长期随访进一步评估。

