
开阔研界 | 人工智能引领变革:开启精准预测根治性前列腺切除术预后新纪元
前列腺癌 是男性中最常被诊断出的实体器官恶性肿瘤,美国每年有超过9万例局限性前列腺癌患者接受根治性前列腺切除术(RP)。术后出现转移和前列腺癌特异性死亡率(PCSM)与术中的不良病理特征相关,但仅依靠临床变量和RP不良病理特征,难以有效预测哪类患者可能受益于辅助或早期挽救性放疗联合雄激素剥夺治疗(ADT)。而组织基因组检测因其成本高昂、处理耗时且消耗组织样本,在美国以外地区应用十分有限。
是男性中最常被诊断出的实体器官恶性肿瘤,美国每年有超过9万例局限性前列腺癌患者接受根治性前列腺切除术(RP)。术后出现转移和前列腺癌特异性死亡率(PCSM)与术中的不良病理特征相关,但仅依靠临床变量和RP不良病理特征,难以有效预测哪类患者可能受益于辅助或早期挽救性放疗联合雄激素剥夺治疗(ADT)。而组织基因组检测因其成本高昂、处理耗时且消耗组织样本,在美国以外地区应用十分有限。
计算能力的指数级增长促进了数字组织病理学与人工智能(AI)的应用。此前,基于5项NRG Oncology III期随机对照试验(RCTs)中接受根治性放疗患者的前列腺活检图像,研究者开发并验证了一系列多模态人工智能(MMAI)模型。MMAI模型利用数字病理学和临床数据,可用于提高前列腺癌风险分层的准确性,从而优化治疗决策。The Journal of Urology期刊发表了一篇标题为“An Artificial Intelligence-Digital Pathology Algorithm Predicts Survival After Radical Prostatectomy From the Prostate, Lung, Colorectal, and Ovarian Cancer Trial”的文章,其主要研究内容是评估预先建立且参数锁定的MMAI模型在接受RP的患者中预测其PCSM和总生存期(OS)的能力。医脉通现编译如下,以飨读者。
研究目的
仅依靠临床变量难以确定哪些患者在接受RP后会出现复发。该研究评估了基于前列腺活检样本训练的锁定MMAI模型在预测接受RP且RP标本已数字化的患者PCSM和OS方面的能力。
研究方法
前列腺癌、肺癌 、结直肠癌
、结直肠癌 和卵巢癌筛查RCTs于1993年至2001年期间将受试者随机分配至癌症筛查组或对照组。确定了接受RP且有数字化组织病理学图像及后续生存数据的患者子集。最初基于接受放疗患者的活检切片训练的远处转移(DM)和PCSM的多模态多任务自动编码器(MMAI)被用于预测PCSM和OS。采用 Cox 比例风险模型和 Kaplan-Meier 生存曲线分析。
和卵巢癌筛查RCTs于1993年至2001年期间将受试者随机分配至癌症筛查组或对照组。确定了接受RP且有数字化组织病理学图像及后续生存数据的患者子集。最初基于接受放疗患者的活检切片训练的远处转移(DM)和PCSM的多模态多任务自动编码器(MMAI)被用于预测PCSM和OS。采用 Cox 比例风险模型和 Kaplan-Meier 生存曲线分析。
研究结果
该研究共纳入1032例接受RP的患者,中位随访时间为17年(IQR:14.3~19.3)。患者基线特征详见表1。
表1. 患者基线特征


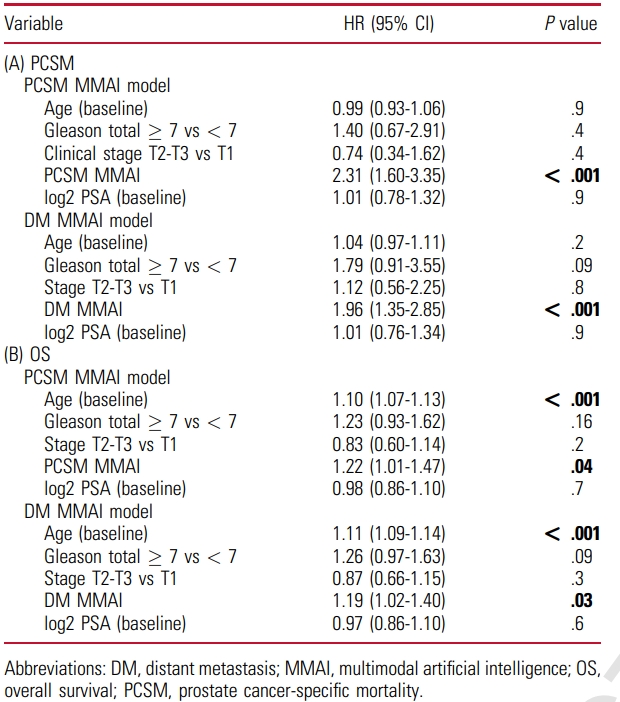
用于预测PCSM和DM风险的MMAI模型均显示出显著的预测能力(PCSM:HR = 2.31,95% CI:1.6~3.35,P < 0.001;DM:HR = 1.96,95% CI:1.35~2.85,P < 0.001)。此外,该模型在预测OS方面亦具有统计学意义,其中针对DM和PCSM的HR分别为1.22(95% CI:1.01~1.47,P=0.04)和1.19(95% CI:1.02~1.40,P=0.03),表2。
表2. PCSM MMAI及DM MMAI预测PCSM(A)与OS(B)的完整多变量模型
研究结论
在PLCO试验接受RP的患者中,DM/PCSM MMAI模型成功预测了PCSM,其提供的预后信息超越单一临床变量。据研究者所知,这是首次验证上述MMAI模型在RP样本中的适用性(该模型最初基于接受放疗患者的活检样本开发,现被应用于以RP作为首要治疗手段的患者群体)。该研究所评估的MMAI模型或可通过未来研究进一步扩展,以识别可能受益于RP术后辅助治疗的患者。随着数字病理学在临床工作流程中的普及,基于AI的预后检测实施门槛有望降低,既能为RP术后患者提供个性化前列腺癌管理方案,又将推动MMAI模型的持续优化。
参考文献:
1.Eric V Li, et al.An Artificial Intelligence-Digital Pathology Algorithm Predicts Survival After Radical Prostatectomy From the Prostate, Lung, Colorectal, and Ovarian Cancer Trial.J Urol . 2025;213(5):600-608.
