
肺凡案例 | 一例小原发灶、大转移灶的“反差”病例启示,揭开肺LCNEC肝转移的诊疗密码
肺大细胞神经内分泌癌(LCNEC)占所有原发性肺癌 的1%–3%,多见于老年男性吸烟者,属于高级别神经内分泌肿瘤。作为一种罕见且高度侵袭性的恶性肿瘤,LCNEC与其他非小细胞肺癌亚型相比,更易发生肝转移,治疗复杂,预后差。晚期患者的肝转移发生率约15%–20%,中位生存期不足8个月。近年来LCNEC发病率呈上升趋势,即使早期患者年死亡率也超过60%。本文分享一例60余岁男性患者,因体检发现肝占位入院,行肝段切除术后病理证实为神经内分泌癌。该病例提示临床医生在遇到多灶性恶性肿瘤时,应高度警惕LCNEC的可能。
的1%–3%,多见于老年男性吸烟者,属于高级别神经内分泌肿瘤。作为一种罕见且高度侵袭性的恶性肿瘤,LCNEC与其他非小细胞肺癌亚型相比,更易发生肝转移,治疗复杂,预后差。晚期患者的肝转移发生率约15%–20%,中位生存期不足8个月。近年来LCNEC发病率呈上升趋势,即使早期患者年死亡率也超过60%。本文分享一例60余岁男性患者,因体检发现肝占位入院,行肝段切除术后病理证实为神经内分泌癌。该病例提示临床医生在遇到多灶性恶性肿瘤时,应高度警惕LCNEC的可能。
患者信息
患者男性,60余岁,有冠状动脉钙化和良性前列腺增生 病史。2024年中期因常规健康筛查偶然发现肝占位性病变,无腹痛、体重下降、呼吸功能障碍等症状。
病史。2024年中期因常规健康筛查偶然发现肝占位性病变,无腹痛、体重下降、呼吸功能障碍等症状。
临床检查
1 影像学检查
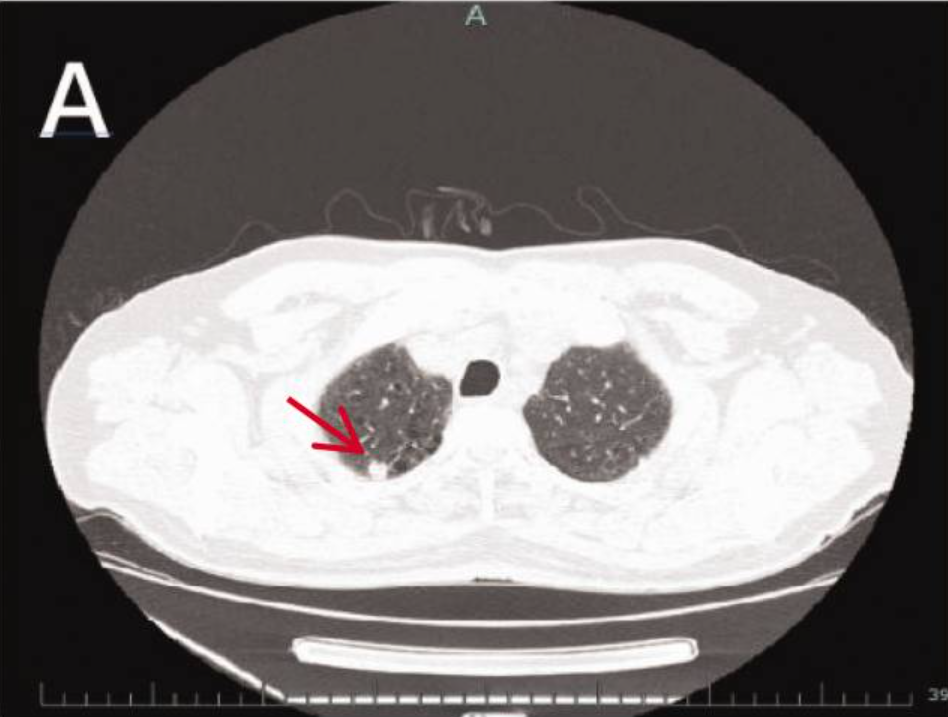
胸部CT:右肺上叶见一孤立性毛刺状结节,大小约9mm。
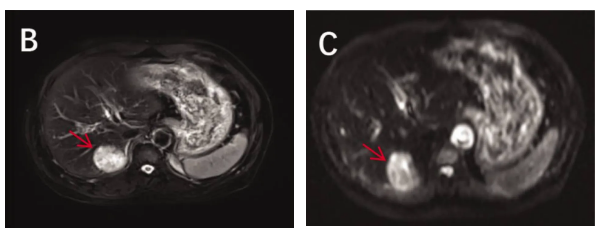
腹部MRI:肝VI-VII段交界区见一边界清晰的圆形病灶(大小46×36×32mm),动脉期呈高强化,门脉期及延迟期强化减退(“廓清征”),初步提示肝细胞癌 。
。
PET-CT:肝病灶、右肺门淋巴结及右肺上叶结节均表现为高代谢活性,符合转移性恶性肿瘤特征;胃肠道可见慢性炎症改变。
2 实验室检查
肿瘤标志物检测 :癌胚抗原(CEA)水平显著升高,达237.23μg/L;其余肿瘤标志物均在正常参考范围内。
:癌胚抗原(CEA)水平显著升高,达237.23μg/L;其余肿瘤标志物均在正常参考范围内。
诊断评估
1 手术及病理检查
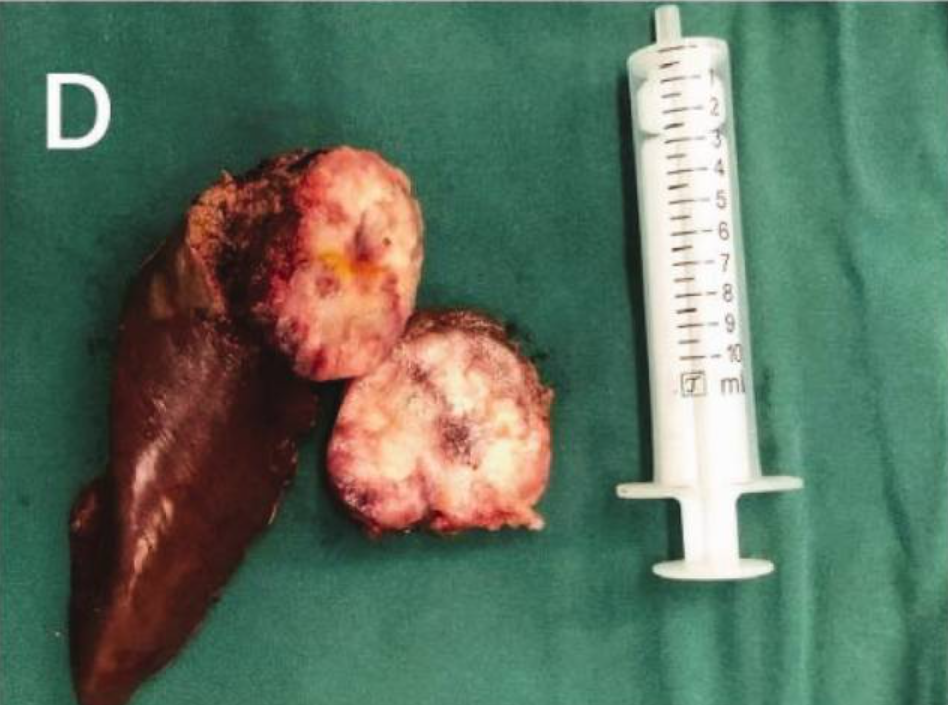
肝段切除术:术中见肝VI段一孤立性病灶,大小约3.0cm,手术切除后切缘阴性。
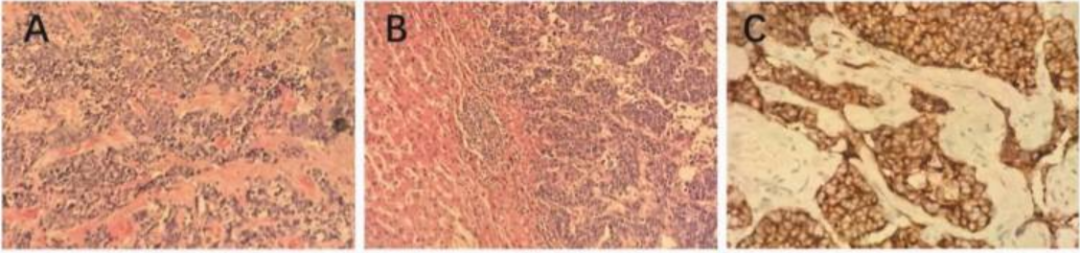
术后病理检查示:肿瘤由大多边形细胞构成,呈巢状排列,胞质丰富,细胞核呈泡状,伴广泛坏死;免疫组化结果显示神经内分泌标志物(CD56+、突触素+、嗜铬粒蛋白A(CgA)+)及甲状腺转录因子1(TTF-1)均强阳性,Ki-67增殖指数达95%,提示为肺来源的转移性神经内分泌癌。
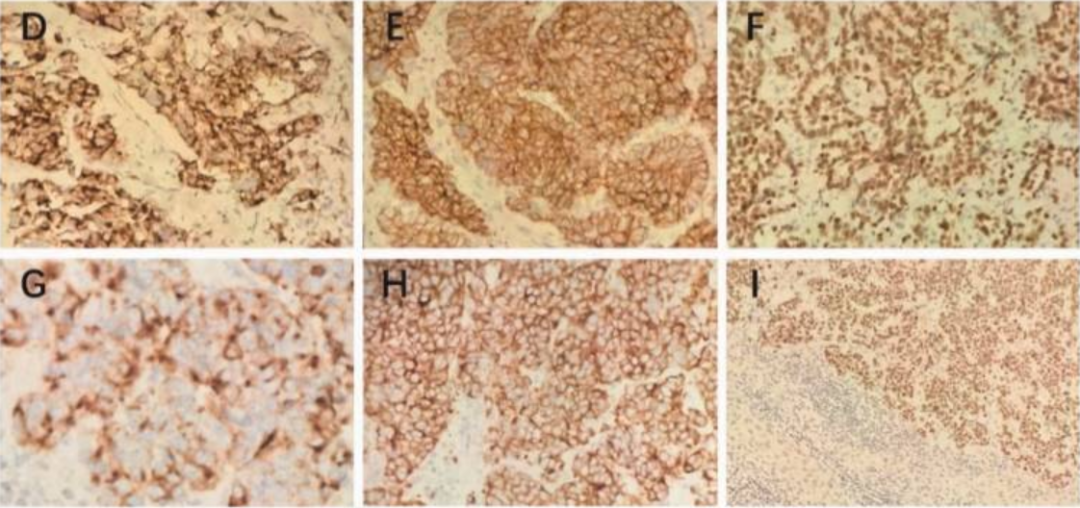
单孔胸腔镜手术(uniportal VATS):患者生命体征稳定后行右肺上叶部分切除术,术后病理示肺病灶与肝转移灶组织学形态一致,确诊为原发性肺大细胞神经内分泌癌(LCNEC),伴脏层胸膜侵犯(图 2d-i)。
2 分子检测
肿瘤组织分子分型提示:PD-L1阳性,存在致病性TP53基因突变。
治疗与结局
1 多学科(MDT)团队评估
由肝胆外科、胸部肿瘤内科及介入放射科组成的MDT团队评估后,优先处理肝转移灶,再治疗肺原发灶。
2 治疗方案
局部治疗:先行腹腔镜 下解剖性肝VI-VII段切除术;术后行肝动脉化疗栓塞术(TACE),予依托泊苷
下解剖性肝VI-VII段切除术;术后行肝动脉化疗栓塞术(TACE),予依托泊苷 150mg+顺铂
150mg+顺铂 90mg;3周后行单孔胸腔镜下右肺上叶部分切除术,实现肿瘤完整切除。
90mg;3周后行单孔胸腔镜下右肺上叶部分切除术,实现肿瘤完整切除。
全身治疗:术后启动一线治疗,方案为斯鲁利单抗 300mg静脉滴注+顺铂35mg/m²+依托泊苷100mg/m²,每21天为1个周期。
300mg静脉滴注+顺铂35mg/m²+依托泊苷100mg/m²,每21天为1个周期。
3 治疗结局
患者术后手术切口愈合良好,无并发症发生;目前临床状态稳定,尚未出现肿瘤复发或转移,拟行第2周期化学免疫治疗。
病例讨论
本病例中,患者因肝占位就诊,影像学提示肝、肺多发病灶。肝转移灶体积远大于原发肺病灶(46 mm vs. 9 mm),体现LCNEC极强的转移和增殖能力。此类快速增长在神经内分泌肿瘤中罕见,提示即使原发灶很小,也需高度警惕转移。
1 影像学诊断与生物标志物
增强CT和PET-CT是检测肝转移的主要手段,CT上肝转移灶通常表现为边缘不规则的低密度病变,PET–CT则显示明显的FDG摄取(最大标准化摄取值SUVmax > 9.0),反映了病灶的高代谢活性。与传统成像方式相比,⁶⁸Ga-PET-CT具有更高的肿瘤定位敏感性,能提升隐匿原发灶检出率及分期准确性,尤其在生长抑素 类似物治疗期间仍可维持诊断效能,建议对疑似神经内分泌肿瘤患者优先选用。此外,超声检查中出现的“驼峰征”(鹿角样钙化)也,有助于将LCNEC肝转移与其他肝脏恶性肿瘤相鉴别。
类似物治疗期间仍可维持诊断效能,建议对疑似神经内分泌肿瘤患者优先选用。此外,超声检查中出现的“驼峰征”(鹿角样钙化)也,有助于将LCNEC肝转移与其他肝脏恶性肿瘤相鉴别。
在生物标志物方面,神经元特异性烯醇化酶(NSE)和嗜铬粒蛋白A(CgA)在60%–80%的LCNEC病例中升高,其水平与肿瘤负荷、转移程度相关。Ki-67增殖指数(>50%)是区分LCNEC与低级别神经内分泌肿瘤的关键指标,同时可预测转移潜能。近期有研究强调PD-L1表达在转移性LCNEC中的作用,约15%–20%的病例显示细胞膜阳性(≥1%),提示其可能适用于免疫治疗。
2 分子分型与预后
通过下一代测序(NGS)进行的分子分型进一步将LCNEC分为SCLC样(RB1/TP53突变)和NSCLC样(KRAS/STK11突变)亚型。两种亚型在转移模式和治疗反应上存在差异,SCLC样对化疗更敏感,但中位生存期更短(8-12个月 vs 12-18个月)。术后辅助化疗可能延缓复发,但其对转移性疾病的疗效仍有限。肝转移进一步将生存期缩短至6–10个月,升高的乳酸脱氢酶(LDH)和中性粒细胞-淋巴细胞比率(NLR)是不良预后的独立预测因子。
3 治疗策略
早期可切除LCNEC的首选治疗方式是手术切除。肺原发灶行肺叶切除术+淋巴结清扫后,I-IIIA期患者5年生存率约30%-40%。晚期LCNEC管理的核心是全身治疗,一线推荐铂类+依托泊苷化疗,缓解率约40%–50%。目前尚未建立标准的LCNEC一线或二线全身治疗方案,尤其是晚期LCNEC的管理策略尚未明确。免疫治疗在PD-L1阳性病例中显示潜力。针对分子亚型的靶向药物处于探索阶段。对于肝转移患者,局部治疗包括手术、TACE、射频消融和放疗。
本病例展示了肺LCNEC的高度侵袭性,其特征为原发性肺部病灶较小但肝转移进展异常迅速。这一现象提示临床医生在面对多灶性恶性肿瘤(尤其吸烟人群)时,需高度警惕LCNEC的可能,即使原发灶较小,也应完善神经内分泌标志物检测及全身影像学评估,以早期识别转移。同时,尽早开展分子分型与PD-L1表达检测,可为后续精准治疗提供依据。
