
纪春岩教授、金洁教授:护航CLL/SLL全程管理,从SEQUOIA研究到真实世界应用,泽布替尼长期安全性再获印证
近年来,随着以布鲁顿酪氨酸激酶抑制剂(BTKi)为代表的靶向药物问世和更新迭代,慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤 (SLL)患者的预后得到明显改善。然而,CLL/SLL是一种不可治愈的疾病,患者往往需要如慢性病一样进行长期管理和治疗1,2。如何选择兼具良好疗效和安全性的治疗策略,做好疾病的全程管理,是实现患者长期生存的关键。为此,医脉通特邀山东大学齐鲁医院纪春岩教授、浙江大学医学院附属第一医院金洁教授围绕CLL/SLL治疗全程管理及新一代BTKi泽布替尼
(SLL)患者的预后得到明显改善。然而,CLL/SLL是一种不可治愈的疾病,患者往往需要如慢性病一样进行长期管理和治疗1,2。如何选择兼具良好疗效和安全性的治疗策略,做好疾病的全程管理,是实现患者长期生存的关键。为此,医脉通特邀山东大学齐鲁医院纪春岩教授、浙江大学医学院附属第一医院金洁教授围绕CLL/SLL治疗全程管理及新一代BTKi泽布替尼 的治疗安全性分享真知灼见。
的治疗安全性分享真知灼见。
良好的药物安全性和依从性有助于CLL/SLL治疗全程管理
靶向治疗时代,BTKi不仅显著改善了CLL/SLL患者的缓解率和预后,也改变了疾病的治疗格局,逐渐成为临床广泛应用的治疗选择3。然而,CLL/SLL仍不可治愈1,患者需要长期、规律地服药以维持良好的缓解3。并且CLL/SLL多为中老年患者,通常身体虚弱且伴多种合并症,治疗耐受性较差,因此治疗期间的全程管理十分重要1。
《布鲁顿酪氨酸激酶(BTK)抑制剂用药安全性管理中国专家循证共识(2024年版)》(以下简称共识)建议,BTKi治疗前需结合患者病情,完善相关检查,排除用药禁忌,评估出血、心房颤动 、高血压
、高血压 等不良事件(AE)的发生风险;治疗中密切监测相关指标和体征,必要时进行对症处理,治疗后则持续观察,以实施全流程、多维度、规范化的安全管理4。并且共识指出,药物依从性和长期安全性对于获得良好的疗效至关重要4,因此选择合适的BTKi亦是患者实现长生存的关键。
等不良事件(AE)的发生风险;治疗中密切监测相关指标和体征,必要时进行对症处理,治疗后则持续观察,以实施全流程、多维度、规范化的安全管理4。并且共识指出,药物依从性和长期安全性对于获得良好的疗效至关重要4,因此选择合适的BTKi亦是患者实现长生存的关键。
值得注意的是,新一代BTKi泽布替尼对BTK激酶结合位点具有高选择性,疗效和毒性特征良好,并且不易与食物、中度/强度CYP3A抑制剂和质子泵抑制剂发生相互作用的特性也提高了给药便利性5,无疑为CLL/SLL治疗全程管理带来了新的希望。
SEQUOIA研究5年随访证实,泽布替尼在CLL/SLL一线治疗中安全性可控
那么,泽布替尼在初治CLL患者中的长期安全性如何?全球、多中心、开放标签、Ⅲ期SEQUOIA研究的队列1中,共纳入479例无del(17p)的初治CLL/SLL患者,随机接受泽布替尼或BR(苯达莫司汀 +利妥昔单抗
+利妥昔单抗 )治疗,其中泽布替尼口服160mg,每日两次,每28天为一个治疗周期,直至疾病进展或发生不可耐受的AE6。
)治疗,其中泽布替尼口服160mg,每日两次,每28天为一个治疗周期,直至疾病进展或发生不可耐受的AE6。
截至2024年4月30日,中位随访时间为61.2个月。泽布替尼组和BR组发生疾病进展的患者分别为30例和98例,其中59例接受BR治疗的患者在疾病进展后转用泽布替尼6。对治疗中/后出现的特别关注的不良事件(AEI)进行分析,发现相较于BR组,泽布替尼组的中性粒细胞减少(17.1% vs 56.8%)、贫血 (9.6% vs 21.1%)、血小板减少(7.1% vs 18.5%)发生率更低,在≥3级AEI中亦观察到相似的表现[中性粒细胞减少(12.5% vs 51.1%)、血小板减少(2.5% vs 8.4%)和贫血(0.8% vs 2.6%)]6。
(9.6% vs 21.1%)、血小板减少(7.1% vs 18.5%)发生率更低,在≥3级AEI中亦观察到相似的表现[中性粒细胞减少(12.5% vs 51.1%)、血小板减少(2.5% vs 8.4%)和贫血(0.8% vs 2.6%)]6。
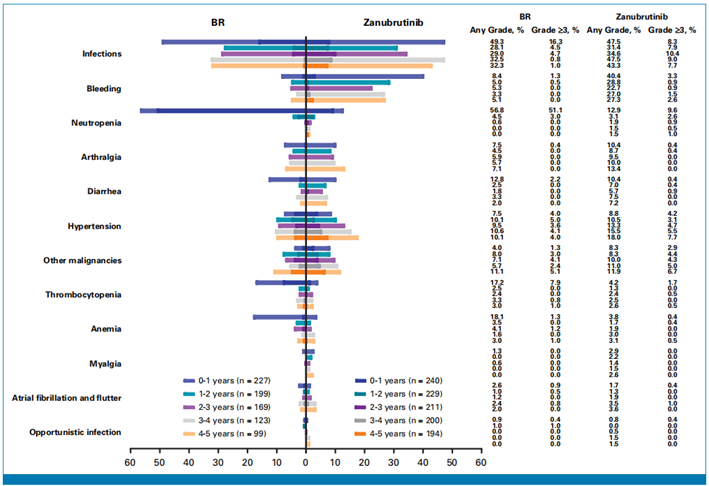
图1.治疗期间的安全性
此外,对于队列2中111例伴有del(17p)/TP53突变的初治高危患者,泽布替尼也表现出相当的安全性结果,其中≥3级AEI分别为感染(33%)、中性粒细胞减少(16%)、高血压(8%)、出血(6%)、心房颤动/心房扑动(5%)和血小板减少(2%)7。
除大型Ⅲ期临床试验的5年随访数据外,泽布替尼的安全性亦在真实世界研究中得到了有力验证,为CLL/SLL患者的长生存之路奠定了坚实的基础。一项真实世界研究纳入2019年1月至2023年7月期间,15317例采用BTKi治疗的初治CLL/SLL患者,其中837例接受泽布替尼治疗,结果显示,泽布替尼一线治疗的新发高血压风险较低,为13.9%8。另一项真实世界研究则评估了2020年1月1日至2023年11月30日期间,接受BTKi一线治疗的600例CLL/SLL患者数据,患者中位年龄为75岁,其中200例患者应用泽布替尼,中位随访13.4个月,研究发现,接受泽布替尼治疗的患者持续治疗可能性较高,并且往往不需要进入下一线治疗,患者第6、12、18和24个月时的持续治疗率分别为88.0%、80.6%、75.9%、75.9%,未进入下一线治疗的概率分别为91.5%、84.6%、77.3%、71.7%9。
当然,泽布替尼便捷的给药方式也为持续治疗提供了支持,该药物服用时间不限餐前/餐后,胶囊可整粒吞服,如有漏服,患者可在当天补服,并在第二天恢复正常用药计划;此外,老年患者和轻中度肝肾损伤患者均无需额外调整剂量,这也为临床全程管理的实施打下了基础10。
纪春岩教授
临床发现,药物治疗相关毒性风险增加,可能与治疗时抑制其他具有BTKi结合半胱氨酸的激酶和超出了BCR信号通路的作用有关;具体而言,腹泻 常被归因于EGFR抑制,感染则与对免疫系统的直接影响有关,包括抑制BTK、TEC和ITK等11。而泽布替尼作为新一代高选择性BTKi,可通过优化丙烯酰胺结构实现与BTK活性位点(Cys481)的不可逆共价结合,显著降低对TEC、ITK、EGFR等激酶的抑制,有效减少脱靶毒性5。
常被归因于EGFR抑制,感染则与对免疫系统的直接影响有关,包括抑制BTK、TEC和ITK等11。而泽布替尼作为新一代高选择性BTKi,可通过优化丙烯酰胺结构实现与BTK活性位点(Cys481)的不可逆共价结合,显著降低对TEC、ITK、EGFR等激酶的抑制,有效减少脱靶毒性5。
SEQUOIA研究的5年随访数据亦证实,泽布替尼在无del(17p)和有del(17p)/TP53突变的初治CLL/SLL患者中均实现了良好的生存,5年PFS率分别达75.8%和72.2%,并且长期安全性可控,出血、血细胞减少和腹泻等AE发生率在第二年逐渐下降,而且随访中近70%患者仍在持续治疗6,7。基于此,《中国肿瘤整合诊治指南(CACA):血液肿瘤(2025)》将泽布替尼作为所有初治CLL/SLL患者[无论有无del(17p)/TP53突变,身体状态良好/欠佳]优先推荐的治疗选择,为临床长期治疗管理提供了指导。
金洁教授
随着BTKi的问世及更新迭代,CLL/SLL患者的预后得以改善,治疗模式也逐渐向慢病化管理转变,但CLL/SLL仍是一种不可治愈的疾病1,在长期临床实践中,BTKi的安全性与疗效同样重要,均有助于保障患者的持续治疗和实现长期生存。
作为新一代高选择性BTKi,泽布替尼一线治疗CLL/SLL的疗效已在SEQUOIA研究中得到充分验证6,真实世界研究则进一步表明,泽布替尼在临床实践中亦有良好的安全性和治疗持续性:接受泽布替尼治疗的初治CLL/SLL患者年医疗资源利用率(HCRU,包括门诊、住院和其他服务)较低,仅为2.613;泽布替尼一线治疗第6、12、18和24个月的持续治疗率均超过75%,未进入下一线治疗的比例均高于71%9。此外,泽布替尼口服给药十分便捷,可在长期治疗过程中提高患者的用药依从性,其CLL/SLL适应症更于2023年正式纳入国家医保目录。作为目前唯一一个初治CLL/SLL适应症纳入国家医保的新一代BTKi,泽布替尼在进一步提升药物可及性的同时,也为广大CLL/SLL患者的全程管理和长期生存提供了有力保障。
专家简历

纪春岩 教授
山东大学教学名师、杰出人才体系特聘教授
泰山学者攀登计划专家
中国抗癌协会整合血液肿瘤委员会执行主任
中国抗癌协会血液肿瘤专业委员会主任委员
中国医院协会血液学机构分会副主任委员
国家卫生计生突出贡献中青年专家
享受国务院政府特殊津贴
中华医学会血液学分会委员
山东省卫生系统杰出学科带头人
山东省抗癌协会血液肿瘤分会主任委员
山东大学血液病 智能诊疗联合实验室主任
智能诊疗联合实验室主任
山东省医学会第八届、第九届血液病学分会主任委员
山东省医学会临床分析细胞学分会主任委员

金洁 教授
医学博士,二级教授,博士生导师
享受国务院特殊政府津贴,全国卫生系统先进工作者
浙江大学医学院附属第一医院终身教授
浙江省全省血液肿瘤精准诊治重点实验室主任
国家卫健委临床重点学科-浙一医院血液学科带头人
浙江省血液病临床医学研究中心主任
浙江大学癌症研究院恶性血液病基础与临床研究负责人
中国女医师协会血液学专委会主任委员
中国抗癌协会血液疾病转化医学前任主任委员
中国医师协会整合血液学会副主任委员
海峡两岸血液学会常务委员
浙江医学会血液学分会前任主任委员浙江省医师学会血液学分会第一、第二届会长


