
儿童急淋白血病门冬酰胺酶相关性胰腺炎的风险因素与预后
门冬酰胺酶 是儿童急性淋巴细胞白血病
是儿童急性淋巴细胞白血病 (ALL)治疗的关键药物,通过消耗血浆中的天冬酰胺——白血病细胞生存必需的氨基酸
(ALL)治疗的关键药物,通过消耗血浆中的天冬酰胺——白血病细胞生存必需的氨基酸 ,发挥抗肿瘤作用。但该药物存在多种不良反应,其中门冬酰胺酶相关性胰腺炎
,发挥抗肿瘤作用。但该药物存在多种不良反应,其中门冬酰胺酶相关性胰腺炎 (AAP)是关键并发症,导致治疗延迟或中断,进而影响患者预后,为ALL治疗和管理带来严重挑战。既往不同研究中 报道的AAP 发生率差异较大(0.8%-18%),AAP发生的风险因素、治疗的预后影响及再次给药策略尚未达成共识。
(AAP)是关键并发症,导致治疗延迟或中断,进而影响患者预后,为ALL治疗和管理带来严重挑战。既往不同研究中 报道的AAP 发生率差异较大(0.8%-18%),AAP发生的风险因素、治疗的预后影响及再次给药策略尚未达成共识。
近日,由上海交通大学医学院附属上海儿童医学中心和南方医科大学南方医院儿科等团队发表于 Blood 题为 Risk factors and outcomes of asparaginase-associated pancreatitis in pediatric patients with ALL 的文章, 该研究为一项大型、多中心的回顾性分析,探讨儿童急性淋巴细胞白血病(ALL)治疗中门冬酰胺酶相关胰腺炎(AAP)的发生风险因素、临床结局及再次使用门冬酰胺酶治疗对患者预后的影响,为临床决策提供重要循证依据。结果显示,年龄(≥10岁)和中高危(IR/HR)ALL状态是 AAP 发生的独立风险因素。未再次使用门冬酰胺酶治疗和诱导治疗第 46 天 MRD≥0.01%是无事件生存(EFS)不佳的独立相关因素。在早发型 AAP和中高危(IR/HR)ALL患者中,再次接受门冬酰胺酶治疗的患者 5 年 EFS 显著高于未进行再治疗的患者,因此,在替代治疗方案有限时,可考再次给予门冬酰胺酶治疗早发AAP的中高危(IR/HR)ALL患儿。

本研究是一项基于中国儿童癌症协作组(CCCG-ALL-2015)方案开展的多中心回顾性队列研究,研究纳入了2015年1月至2019年12月期间,在中国20家主要医院和医疗中心接受治疗的7640例新诊断的ALL患儿(年龄1个月至18岁)。根据临床特征和可测量残留病(MRD)将患者分为低危(LR)、中危(IR)和高危(HR)组。AAP的诊断依据国际Ponte-di-Legno共识标准,采用NCI CTCAE 5.0版进行AAP严重程度分级。通过多变量回归分析和生存模型(Kaplan-Meier、Cox回归)评估了AAP的发生率、风险因素、以及对无事件生存期(EFS)的影响,同时特别关注了门冬酰胺酶再次用药对患者预后的影响。
在7,640例ALL患儿中,298 例患者发生了 AAP,AAP的总体发生率为3.9%(95% CI:3.5%~4.3%), AAP患者的5年无事件生存率(EFS)和5 年 OS显著低于未发生AAP的患者(EFS 71.8% vs. 81.0% P<0.001,OS 84.8% vs 91.3% P<0.001)(见图1)。复发率在两组间无显著差异。另外,亚组分析显示,低危(LR) AAL 患者中,发生AAP患者的 5 年 EFS低于非AAP患者(81.0% vs 88.6%,P=0.05),中高危 AAL 患者中,发生AAP患者的5 年 EFS与非AAP患者差异无统计学意义(68.0% vs 72.1%,P=0.10)(见图2)。
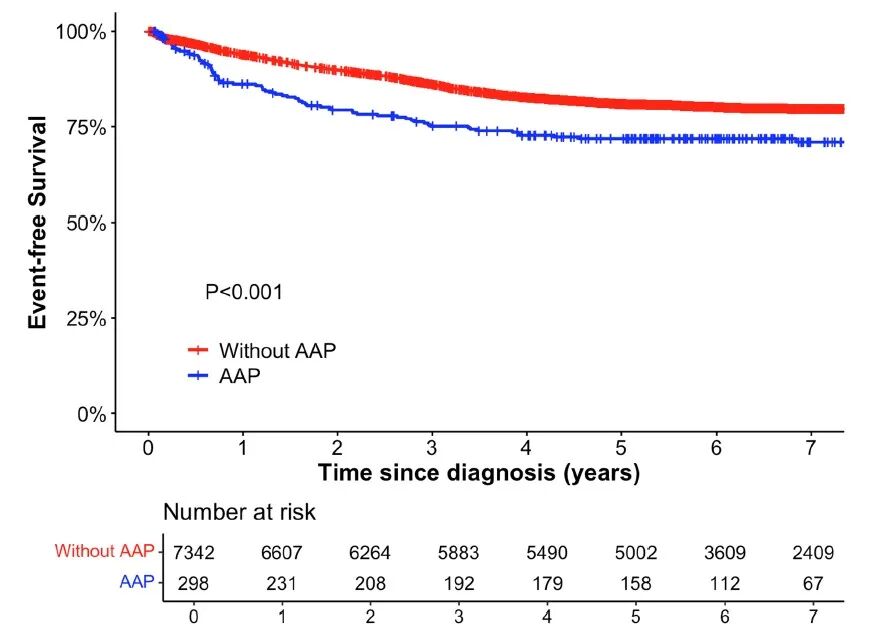
图1 发生/不发生AAP的AAL患者5年EFS对比
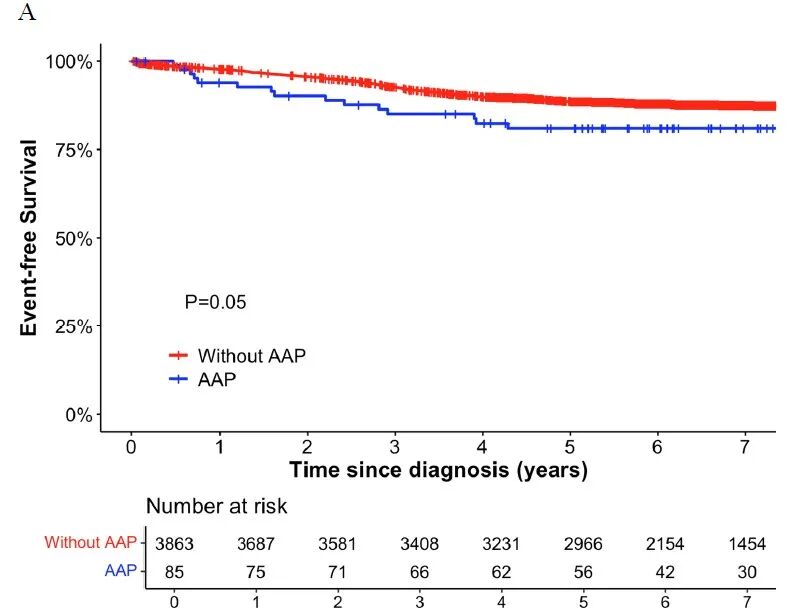
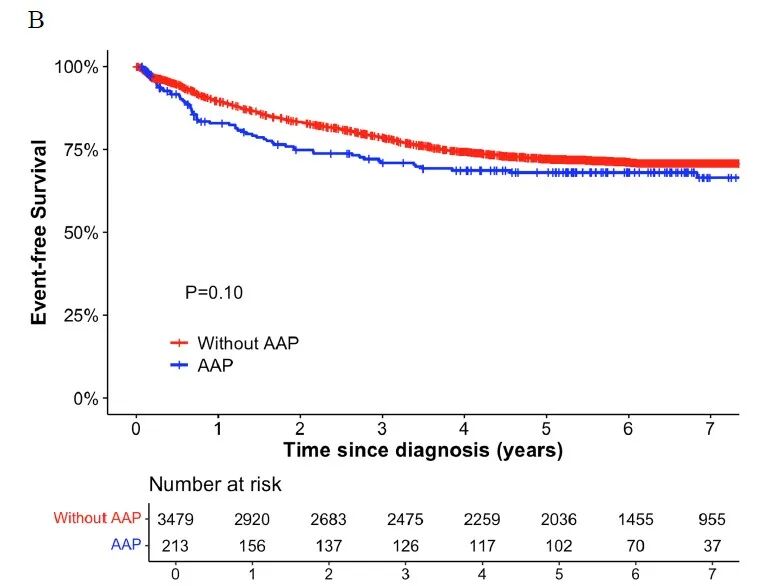
图2(A) 发生/不发生AAP的AAL低危(LR)患者5年EFS对比;(B)发生/不发生AAP的AAL中高危(IR/HR)患者5年EFS对比
AAP 发生的独立风险因素:多因素分析结果表明,年龄≥5岁(尤其是10岁以上)和中高危(IR/HR)ALL状态是AAP发生的独立风险因素(图3)。另外,T-ALL、BCR::ABL1融合亚型也与AAP的发生相关。
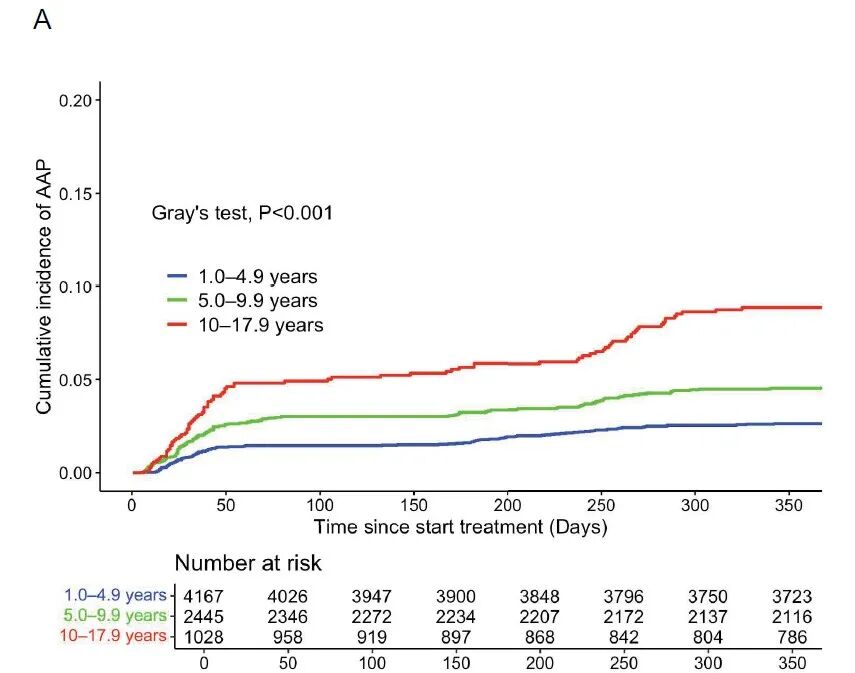
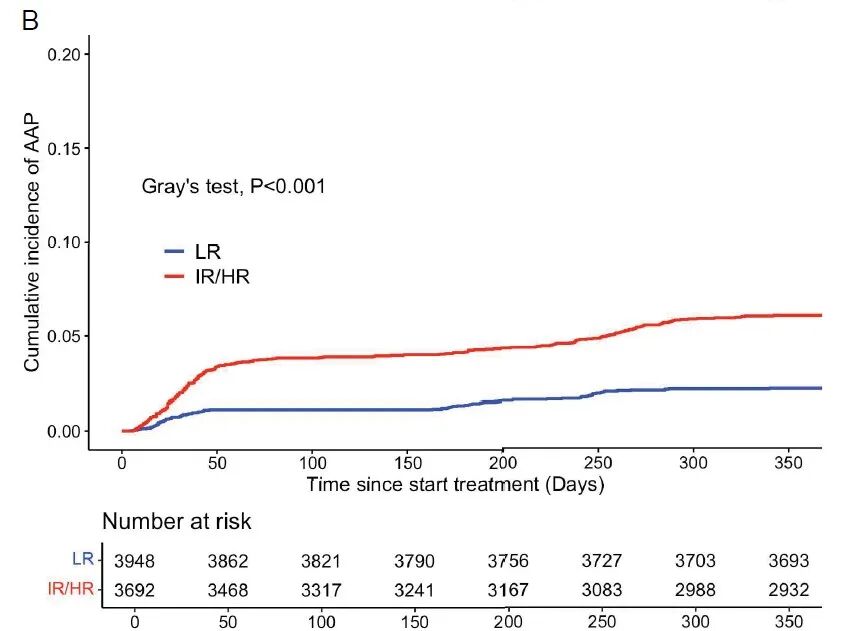
图3:(A)按年龄组分层的AAP发生率;(B) 按疾病严重程度分层的AAP发生率
在298例发生AAP的患者中,接受门冬酰胺酶再次给药患者的5年EFS显著优于未接受者,尤其是在中高危患者(82.4% vs. 60.6%)和早发AAP的患者中(80.1% vs. 60.2%)。未接受再治疗的早期AAP的中高危患者预后相对较差,5年EFS为53.3%。此外,再治疗后二次AAP的发生率在中高危患者中为33.8%,但AAP的严重程度大多未加重,表明门冬酰胺酶再治疗具有一定的安全性。多因素分析进一步确认,未接受再治疗(HR=2.0,95% CI 1.1-3.6,P=0.02)和第46天MRD ≥0.01%(HR=3.7,95% CI 2.1-6.8,P<0.001)是AAP患者EFS不佳的独立风险因素。
本研究证实年龄较大和中高危(IR/HR)ALL状态是 AAP 发生的独立风险因素。但中高危(IR/HR)组ALL患者的 AAP 风险升高可能是由于几乎所有 10 岁以上患儿均为中高危ALL患者,且该组使用的门冬酰胺酶剂量更高(已知高剂量会增加 AAP 风险)。按风险分层分析时,AAP 对低危组 5 年 EFS 的影响似乎比中高危组更显著,可能的原因包括:AAP 直接导致的治疗相关死亡;与 AAP 和复发均相关的高危特征(如年龄≥10 岁、T-ALL、诱导治疗反应不佳)发生率更高;医生为选择替代治疗而决定患者退出研究。
本研究仍有一些局限性:首先,缺乏针对 AAP 管理的方案指定指南,再治疗决策(包括是否再治疗及制剂选择)由医生自主决定;其次,尽管低危组和中高危组的再治疗的患者比例相近(分别为 28.2%(24/85)和 31.8%(68/213)),且研究人群反映了真实的临床实践,但仍可能存在选择偏倚;再次,大多数再治疗患者使用短效门冬酰胺酶(10 例使用大肠杆菌 门冬酰胺酶,10 例使用欧文氏菌门冬酰胺酶),仅 8 例使用培门冬酶
门冬酰胺酶,10 例使用欧文氏菌门冬酰胺酶),仅 8 例使用培门冬酶 ,尽管仅使用大肠杆菌门冬酰胺酶的患者出现了更严重的复发,但样本量较小,无法明确再治疗的最佳制剂;最后,医生决定的研究中断(被视为 EFS 事件)可能受此前门冬酰胺酶停用的影响,而本研究模型未调整这一潜在混杂因素。
,尽管仅使用大肠杆菌门冬酰胺酶的患者出现了更严重的复发,但样本量较小,无法明确再治疗的最佳制剂;最后,医生决定的研究中断(被视为 EFS 事件)可能受此前门冬酰胺酶停用的影响,而本研究模型未调整这一潜在混杂因素。
研究人员指出,尽管存在上述局限性,在缺乏新型有效治疗的情况下,仍应考虑再次使用门冬酰胺酶进行AAP 中高危(IR/HR)患者(尤其是早发AAP患者)的治疗;相反,若存在其他有效的全身化疗方案,低危(LR)患者可能无需再次使用门冬酰胺酶治疗。而且随着双特异性抗体(如 blinatumomab)被纳入 B-ALL 一线治疗方案,停用门冬酰胺酶带来的的临床影响可能会潜在降低,尤其是在化疗不耐受的ALL患者中。因此,尽管本研究强调了早期停用门冬酰胺酶的风险,但这类风险可能通过包含 blinatumomab 等免疫治疗药物的现代治疗方案得到部分缓解。
*本文由深圳市拾玉儿童公益基金会“儿童肿瘤前沿”团队编译或约稿,文中图表均源引自文献原文。本文著作权归文章作者所有,欢迎个人转发分享,未经允许禁止转载,作者拥有所有法定权利,违者必究。如需转载,请留言或联系shiyu@curekids.cn。本文旨在分享儿童肿瘤科研前沿成果,不是治疗方案推荐。如需获得疾病治疗方案指导,请前往正规医院就诊。
原文摘要(Abstract)
Asparaginase-associated pancreatitis (AAP) is a significant complication in acute lymphoblastic leukemia (ALL) therapy, often leading to treatment delays or discontinuation. This study aimed to identify AAP risk factors, assess outcomes after first and second episodes, and evaluate the impact of asparaginase rechallenge. We retrospectively analyzed 7,640 patients (aged 1 month-18 years) treated under the Chinese Children Cancer Group ALL 2015 protocol. Patients were stratified as low-risk (LR), intermediate-risk (IR), or high-risk (HR) based on clinical features and measurable residual disease (MRD). AAP was categorized as early- or late-onset depending on treatment phase. Older age and IR/HR status were independent risk factors for AAP. The cumulative AAP incidence was 2.2% in LR and 5.8% in IR/HR groups. Among 298 patients who developed AAP, 92 were rechallenged with asparaginase; second episodes occurred in 20.8% of LR and 33.8% of IR/HR patients, with no increase in severity. Lack of rechallenge (HR, 2.0; 95% CI, 1.1-3.6) and Day 46 MRD ≥0.01% (HR, 3.7; 95% CI, 2.1-6.8) were independently associated with inferior event-free survival (EFS). Among patients with early-onset AAP, rechallenged patients had superior 5-year EFS compared to those not rechallenged (80.1% vs. 60.2%; P = .003). Similarly, among IR/HR group, rechallenged individuals and better 5-year EFS than those not rechallenged (82.4% vs. 60.6%; P = .004). IR/HR patients with early-onset AAP who were not rechallenged had especially poor outcomes (5-year EFS, 53.3%). These findings support considering asparaginase rechallenge in IR/HR patients with early-onset AAP when alternative therapies are limited. Chinese Clinical Trial Registry: ChiCTR2000032211.
