
细胞焦亡及其与椎间盘退变关系的研究进展
作者:甘肃中医药大学第一临床医学院付振江
腰痛是全球性的公共卫生问题,不仅影响个人生活质量,同时对经济和医疗系统造成沉重负担。椎间盘退变(IDD)是导致腰痛的主要原因之一。椎间盘由外周的纤维环包围着中心的胶状髓核,并与上下端薄层软骨终板相连,其主要功能是承受压力、维护脊柱的稳定性和灵活性。随着年龄的增长,IDD的发病率逐渐增加,并成为慢性腰痛和功能障碍的主要原因。
细胞焦亡是一种新发现的程序性细胞死亡方式,在IDD病理生理过程中扮演重要角色。细胞焦亡依赖于半胱天冬酶(Caspases)并由成孔蛋白(GSDM)介导,主要特征是细胞肿胀、膜孔形成和炎症因子的释放。与凋亡不同,焦亡不仅导致细胞死亡,还引发局部炎症反应,加剧椎间盘组织的损伤和退变。此外,细胞焦亡对免疫反应的激活和调节至关重要。过度激活焦亡不仅破坏免疫系统的稳态并促进自身免疫疾病的发展,如炎性肠病和类风湿性关节炎,而且成为慢性炎症性疾病的主要驱动因素,如骨关节炎。因此,进一步探索IDD的发病机制,采取针对焦亡的治疗策略是当前的研究热点之一。
髓核细胞中含有核苷酸结合寡聚化结构域样受体家族pyrin结构域-3(NLRP3)炎症体介导的焦亡在IDD中被激活。靶向调节NLRP3炎症体介导的焦亡表现出良好的细胞外基质重塑能力及抗炎特性,缓解了IDD进展。笔者旨在综述细胞焦亡的分子机制及焦亡在IDD中的作用,探讨焦亡与炎症反应、凋亡、氧化应激、自噬及IDD相关危险因素之间的相互作用机制。此外,我们还讨论了焦亡在IDD中的靶向治疗应用,为开发更有效的治疗手段提供理论基础。
焦亡的分子机制
根据Caspase的不同,焦亡的机制分为经典途径、非经典途径和其他途径。
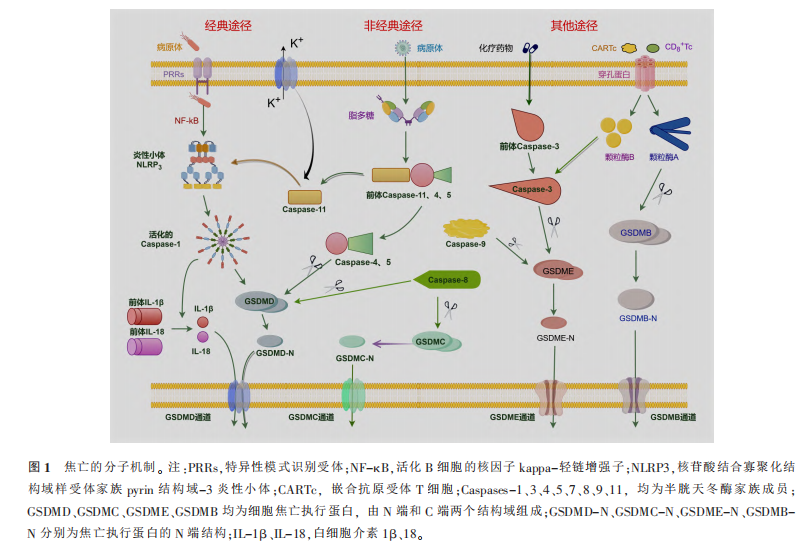
经典途径 主要通过NLRP3炎性小体激活Caspase-1,进而产生多种病理生理反应。当病原体入侵时,细胞的特异性模式识别受体(PRRs)识别病原体并与特定配体结合,形成NLRP3炎性小体,并激活Caspase-1。激活的Caspase-1切割成孔蛋白GSDMD(GSDMD)N端结构域(GSDMD-N)并释放GSDMD-N,导致细胞焦亡。激活的Caspase-1还促使白细胞介素(IL-1β、IL-18)成熟并释放到胞外,从而增强炎症反应。此外,Caspase-11可通过GSDMD-N膜孔引起K+外排,激活NLRP3和Caspase-1,启动经典途径。
非经典途径 依赖于Caspase-4、5(人)、11(鼠)的激活。这些Caspase家族成员能够直接识别病原体的脂多糖并且切割GSDMD,释放GSDMD-N,导致细胞膜穿孔。
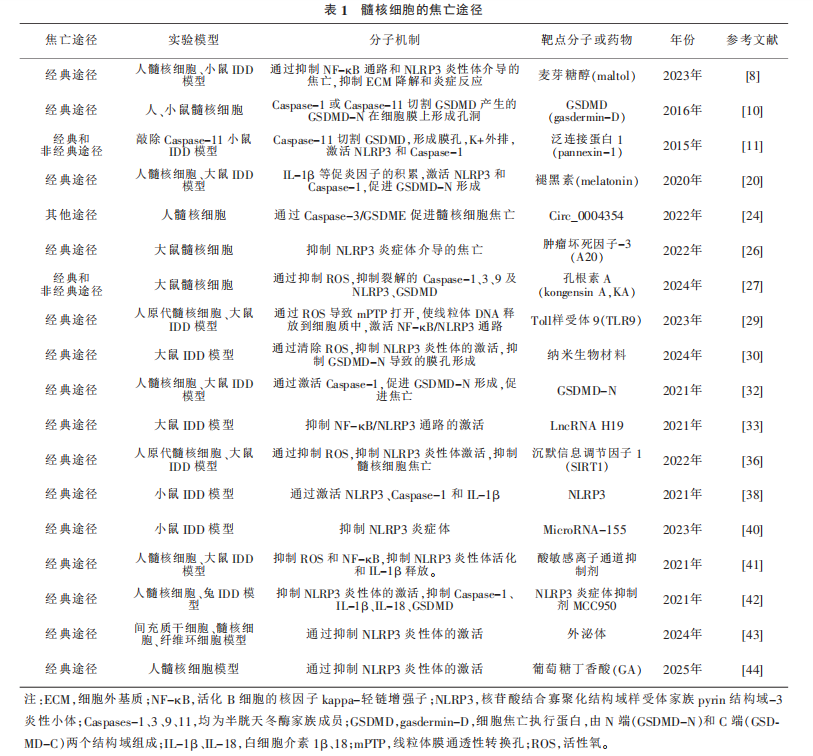
其他途径 由Caspase-3、8、9介导的其他途径。如化疗药物诱导Caspase-3切割GSDME促使细胞发生焦亡;Caspase-8和Caspase-9分别诱导GSDMD和GSDME的裂解,触发细胞焦亡。此外,研究表明颗粒酶也能诱导焦亡。如嵌合抗原受体T细胞(CARTc)通过释放颗粒酶B激活靶细胞中的Caspase-3,激活的Caspase-3裂解GSDME,颗粒酶A直接裂解GSDMB,最终导致质膜穿孔,引发焦亡。这些研究表明,GSDM蛋白家族、Caspase家族在焦亡的分子机制中起着至关重要的作用(图1)。在IDD中,髓核细胞的焦亡主要涉及NLRP3/Caspase-1/GSDMD轴介导的经典途径,焦亡的非经典途径和其他途径在IDD中的研究相对较少(表1)。
焦亡在IDD中的作用
在IDD的病理生理过程中,焦亡与炎症、凋亡、氧化应激、自噬及其他IDD相关危险因素相互作用,共同构成IDD的机制网络,影响着IDD进展(图2)。
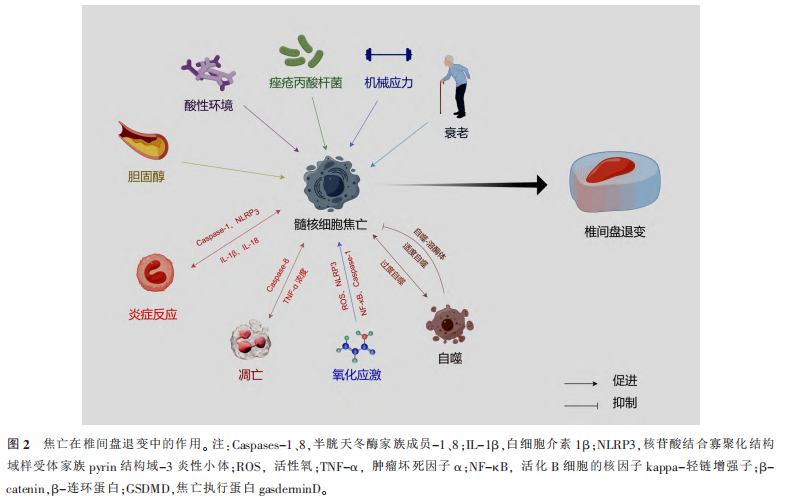
焦亡与炎症在IDD中的作用 细胞焦亡通过促炎因子的释放,引发椎间盘髓核细胞的炎症反应,从而加剧IDD进程。炎症反应进一步促进髓核细胞损伤和焦亡,形成恶性循环,导致椎间盘结构和功能的持续丧失。NLRP3炎性体的激活促使Caspase-1释放,诱导髓核细胞焦亡。焦亡是一种重要的机制,旨在清除细胞内的病原体并调节免疫系统以抵御感染,但过度的焦亡会引起继发性炎症反应,参与多种炎症性疾病的发展。髓核细胞焦亡主要通过NLRP3炎性小体的激活而发生,活化的Caspase-1将GSDMD蛋白的N端结构域切割并释放,导致髓核细胞膜的孔洞形成与裂解,促使IL-1β和IL-18等细胞因子的释放,这不仅直接损伤髓核细胞,又激活周围细胞的炎症反应。IL-1β等促炎因子在退变的髓核细胞中积累,最终激活NLRP3和Caspase-1,促进GSDMD-N形成,诱导细胞焦亡。IL-1β和TNF-α具有强大的促炎活性,并与IDD发展过程密切相关,包括炎症反应、凋亡及焦亡。麦芽糖醇通过抑制NLRP3炎性体介导的焦亡,抑制细胞外基质降解和炎症反应,延缓小鼠椎间盘退变。因此,麦芽糖醇可能是针对焦亡与炎症的潜在缓解IDD药物。
焦亡与凋亡在IDD中的作用 焦亡与凋亡之间存在相互转化的关系,且两者共同参与IDD的病理过程。Caspase-8在凋亡和焦亡中均起着关键作用。当凋亡被抑制时,Caspase-8会激活炎性小体,诱导细胞焦亡。通过上调GSDME水平,可以将TNF-α或化疗药物诱导的细胞凋亡转变为焦亡。此外,Caspase-3和Caspase-7也可通过切割GSDME使细胞由凋亡转化为焦亡。低浓度TNF-α(10ng/mL)处理髓核细胞以焦亡为主,高浓度TNF-α(100ng/mL)处理髓核细胞以凋亡为主。当抑制焦亡时,髓核细胞的凋亡也显著减少。这种转换关系可能与IDD微环境中炎症介质浓度的改变有关。因此,在IDD早期可能以焦亡为主,随着炎症介质浓度的增加,焦亡与凋亡共同参与IDD的过程。孔根素A(KA)通过上调髓核细胞中丝裂原活化蛋白激酶7(Map3k7,也称TAK1)的表达维持线粒体氧化还原平衡,抑制焦亡与凋亡,延缓IDD进展。因此,靶向TAK1可能是IDD的一种潜在治疗方法。
焦亡与氧化应激在IDD中的作用 氧化应激是导致焦亡的重要因素。氧化应激的升高增加细胞内活性氧(ROS)水平,通过激活NLRP3/Caspase-1诱导焦亡。ROS主要在线粒体中产生。ROS升高导致线粒体功能障碍,引起线粒体膜通透性转换孔(mPTP)打开,使线粒体DNA释放到细胞质中,进一步激活NF-κB信号通路引起髓核细胞焦亡。近年来,纳米生物材料在IDD治疗中的研究应用越来越多,主要通过清除细胞内ROS含量,抑制GSDMD-N导致的膜孔形成和膜破裂,降低NLRP3炎性体的激活,抑制焦亡并缓解IDD。此外,槲皮素能够通过逆转线粒体功能障碍并降低线粒体DNA含量而抑制焦亡。因此,氧化应激通过升高ROS水平、损伤线粒体功能以及释放线粒体DNA诱导焦亡,调节氧化应激并恢复线粒体功能可能有助于抑制细胞焦亡而延缓IDD进展。
焦亡与自噬在IDD中的作用 细胞焦亡和自噬在IDD中存在双向作用,焦亡加剧髓核细胞损伤,而自噬通过抑制焦亡维持细胞稳态。当自噬功能过度时,促进髓核细胞的焦亡而加速IDD。
适度的自噬抑制焦亡 自噬对脂多糖诱导的髓核细胞焦亡具有保护作用。主要通过自噬-溶酶体途径降解GSDMD-N以及溶酶体的膜修复功能抑制焦亡导致的质膜穿孔。目前大多数研究表明自噬对IDD起到保护和延缓的作用,而少数研究表明自噬加速IDD。
过度的自噬促进焦亡 过度的自噬可促进细胞成分的降解和自我消化,导致髓核细胞焦亡,从而加速IDD。暂时性压缩(1MPa)可激活自噬,抑制髓核细胞的变性,而持续压缩会促进髓核细胞的死亡。提示自噬在IDD早期对诱导细胞起保护作用,但持续刺激导致过度自噬,最终可能促进髓核细胞焦亡和IDD。由于自噬是一种不同阶段的动态活动,自噬与焦亡之间的关系仍需进一步阐明。沉默信息调节因子1(SIRT1)通过线粒体自噬抑制NLRP3炎性体激活,抑制焦亡,延缓IDD。因此,SIRT1可能是IDD的潜在治疗靶点。
焦亡与其他危险因素在IDD中的作用 机械应力和衰老是影响IDD的最主要危险因素,此外,高胆固醇、酸性环境及痤疮丙酸杆菌等因素均可诱导髓核细胞焦亡而加速IDD的进展。机械应力和衰老是导致IDD的最主要危险因素。机械应力可上调β-连环蛋白(β-catenin),改变细胞间传递机械应力的方式。施加机械应力后可激活Wnt/β-catenin信号通路,诱导髓核细胞焦亡,促进IDD。衰老的过程中伴随着促炎细胞因子的升高,如IL-1β、IL-18和NLRP3炎性小体,且与焦亡的关键步骤密切相关。因此,衰老可能通过焦亡机制参与IDD。高胆固醇、酸性环境及痤疮丙酸杆菌等因素也是IDD的重要诱因。胆固醇过高可导致细胞外基质(ECM)降解和髓核细胞焦亡。高脂肪饮食诱导高胆固醇血症伴IDD的小鼠中,NLRP3炎性体激活,导致髓核细胞焦亡和基质降解。乳酸通过调节细胞间ROS水平激活NF-κB信号通路,促进NLRP3炎性体活化和IL-1β释放,致使髓核细胞焦亡。痤疮丙酸杆菌是一种诱导髓核细胞焦亡的新致病因子。人髓核细胞与痤疮丙酸杆菌共培养导致IL-1β、NLRP3和GSDMD呈时间和剂量依赖性过表达,导致髓核细胞焦亡。
综上,焦亡导致椎间盘髓核细胞功能失调,影响生物力学特性。焦亡释放的炎症介质加剧椎间盘的炎症,尤其NLRP3炎症体的激活,进一步加重IDD。针对NLRP3炎症体的抑制剂在目前IDD研究中取得一定成果,这些抑制剂可显著降低焦亡和椎间盘组织的炎症,减缓IDD进程。因此,靶向焦亡途径成为一种潜在的IDD治疗手段。
总结与展望
细胞焦亡作为一种炎性程序性细胞死亡方式,在IDD中主要通过NLRP3炎性体的激活和Caspase家族介导的经典途径,导致髓核细胞死亡及细胞外基质紊乱,继而引发炎症反应,最终导致椎间盘结构破坏和功能丧失。因此,临床上靶向焦亡途径的IDD治疗主要通过抑制NLRP3炎性体的激活,抑制髓核细胞焦亡,最终延缓IDD进展。如间充质干细胞分泌的外泌体和葡萄糖丁香酸(GA)都是通过抑制NLRP3炎性体的激活,延缓IDD进展。尽管目前对焦亡在IDD中的作用有报道,但焦亡对IDD的具体调控机制未完全明确。如:(1)深入研究焦亡在IDD中的上游信号通路,探索焦亡过程中的关键分子以及相关生物标志物,以促进IDD的早期诊断和预后评估;(2)大量的研究证明IDD的发展与焦亡的经典途径相关,而焦亡的非典型途径和其他途径很少报道,因此可以重点研究焦亡的非经典途径和其他途径对IDD的作用机制;(3)目前,尽管针对焦亡途径的IDD治疗研究有部分进展,但缺乏临床实践的验证。因此,将靶向焦亡药物的研究进一步转化到临床应用是最终的挑战。此外,结合生物信息学、分子生物学和人工智能深度学习等多学科交叉研究,以全面理解细胞焦亡在IDD中的作用机制,为临床治疗IDD提供新的思路。
来源:中国脊柱脊髓杂志2025年第35卷第8期
