
2025 ESMO丨从病理缓解到生存获益:中国研究详解新辅助免疫联合化疗在ESCC中的多重价值
临床困境:局晚期食管鳞癌治疗亟需突破生存瓶颈
我国食管癌 发病率约占全球食管癌的一半以上,其中食管鳞癌(ESCC)高达90%,是我国最常见的食管癌病理类型[3]。目前,对于可切除的局部晚期ESCC,nCT联合手术是临床指南推荐的标准方案之一。然而,这一传统模式面临两大挑战:一方面,nCT可能增加术后并发症发生率、提升手术操作难度[4]。另一方面,大量临床数据表明,即使接受规范治疗,局部晚期食管癌患者的5年总生存率仍不尽如人意,亟待引入新的围术期治疗策略以突破这一生存瓶颈。
发病率约占全球食管癌的一半以上,其中食管鳞癌(ESCC)高达90%,是我国最常见的食管癌病理类型[3]。目前,对于可切除的局部晚期ESCC,nCT联合手术是临床指南推荐的标准方案之一。然而,这一传统模式面临两大挑战:一方面,nCT可能增加术后并发症发生率、提升手术操作难度[4]。另一方面,大量临床数据表明,即使接受规范治疗,局部晚期食管癌患者的5年总生存率仍不尽如人意,亟待引入新的围术期治疗策略以突破这一生存瓶颈。
近年来,以免疫检查点抑制剂为代表的免疫治疗,已在晚期ESCC的一线治疗中展现出卓越疗效,彻底改变了晚期食管癌治疗格局[5]。例如,国际多中心III期临床研究RATIONALE-306和RATIONALE-302证实,替雷利珠单抗 联合化疗一线治疗或单药二线治疗均可显著延长晚期食管癌患者的总生存期(OS),该适应证已获得中美欧日等多个国家药品监督管理局批准。目前,免疫治疗前移至局晚期食管癌的研究成为临床热点。然而,nICT虽能显著提高pCR率,但其能否转化为长期生存获益(尤其是OS),始终是全球学者关注和争论的核心议题。此次江苏省肿瘤医院团队的两项研究,正是针对这一关键临床疑问展开系统解答。
联合化疗一线治疗或单药二线治疗均可显著延长晚期食管癌患者的总生存期(OS),该适应证已获得中美欧日等多个国家药品监督管理局批准。目前,免疫治疗前移至局晚期食管癌的研究成为临床热点。然而,nICT虽能显著提高pCR率,但其能否转化为长期生存获益(尤其是OS),始终是全球学者关注和争论的核心议题。此次江苏省肿瘤医院团队的两项研究,正是针对这一关键临床疑问展开系统解答。
研究设计:真实世界数据结合双重分析路径,全面评估nICT价值
研究人群
两项研究基于同一真实世界队列回顾性分析,研究者从2019-2021年江苏省肿瘤医院收治的5472例食管癌患者中,严格筛选出257例经病理确诊的局部晚期可切除ESCC患者。所有患者均在新辅助治疗后接受手术,其中125例采用nICT方案,132例采用nCT方案。
统计分析
为全面且精准地挖掘nICT的临床价值,研究采用两种独立的统计分析策略:
长期生存情况:采用倾向评分匹配(PSM)平衡nICT与nCT组间的基线特征,运用Kaplan-Meier法和Cox比例风险模型评估生存情况并确定独立预后因素。
免疫病理反应比较和预后预测模型构建:研究对肿瘤退缩情况和免疫相关组织病理学特征进行评估和比较。将257例患者按7:3比例随机分为训练集(n=180)与验证集(n=77),利用LASSO回归和多因素Cox回归进行模型开发与验证。
研究结果:nICT展现多重优势,从病理缓解到生存获益的全面突破
1
患者基线特征
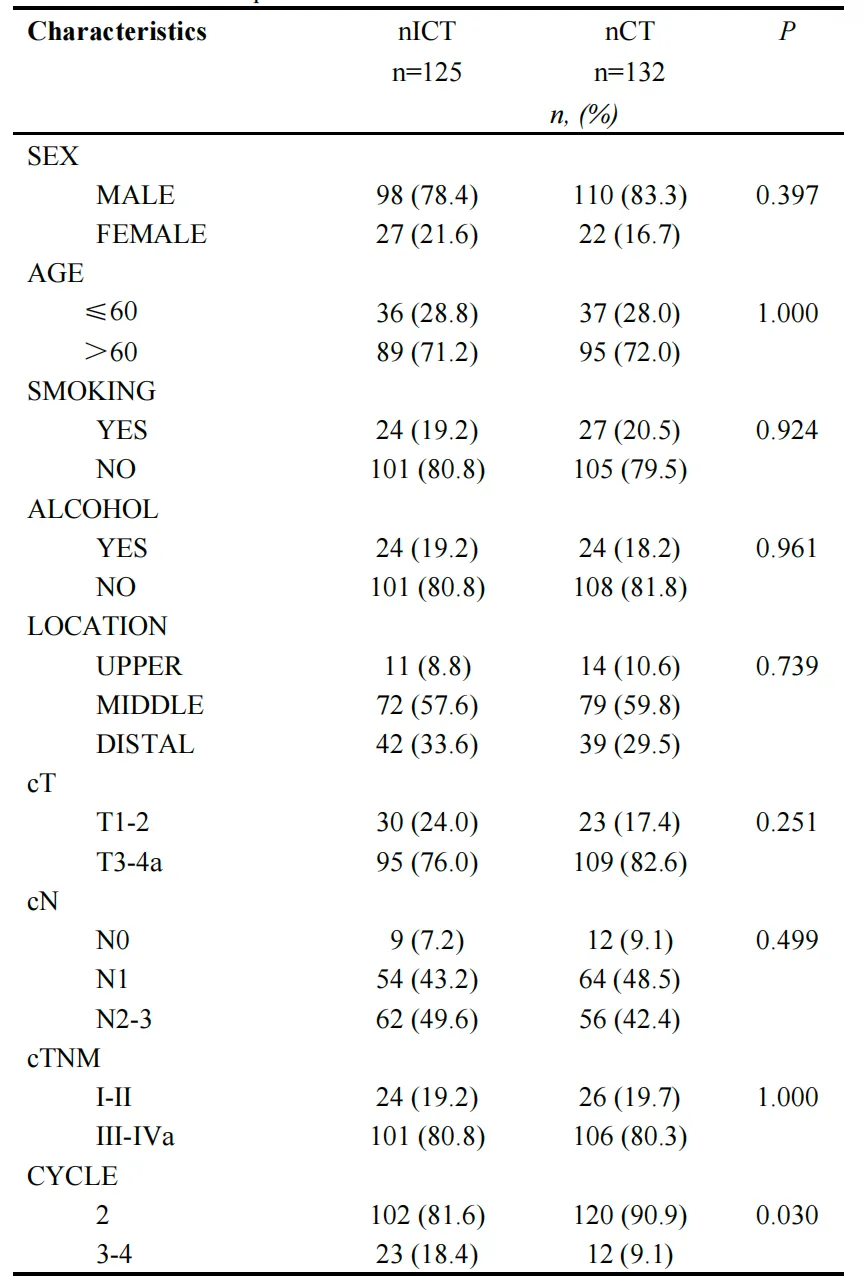
研究初始纳入257例患者(nICT=125, nCT=132)。患者基线特征(表1)显示,在PSM前,两组患者在临床分期(cTNM III-IV期:80.8% vs 80.3%)等多数特征上分布相近,但在新辅助治疗周期分布上存在差异(接受3-4周期治疗者:nICT组18.4% vs nCT组9.1%)。为精准评估疗效,研究对257例患者进行PSM处理,最终成功匹配103对患者,为后续生存与疗效的比较提供了可靠的均衡队列。
表1 患者基线特征
2
生存分析:nICT显著延长无事件生存期
在PSM后的均衡队列中,经过中位45.4个月(IQR, 24.9-49.8)的随访,nICT组的中位EFS未达到,而nCT组的中位EFS为24.3个月。nICT显著降低了事件发生风险达36%(风险比HR=0.64, 95%CI: 0.43-0.95, P=0.029)。两组的中位OS均未达到,且未见统计学显著差异(HR=0.76, 95%CI: 0.47-1.23, P=0.270)(图1)。
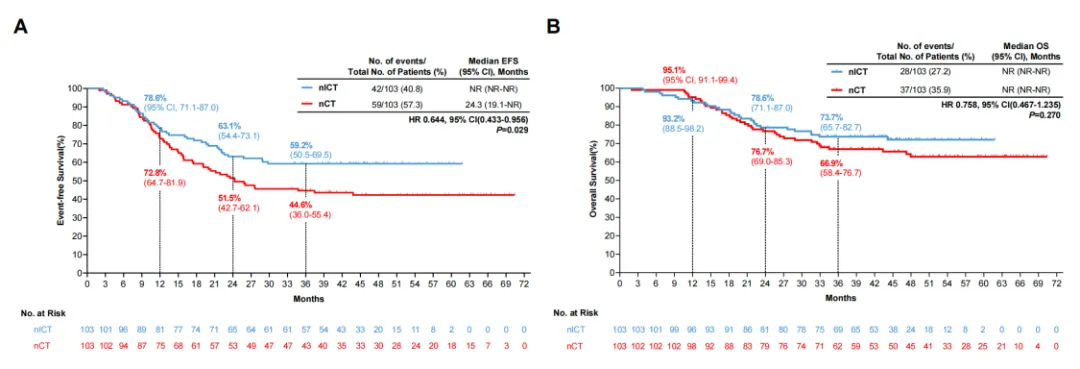
图1 PSM后的(A)EFS和(B)OS生存曲线图
(引自2025 ESMO Poster截图)
对复发和转移模式的进一步分析显示nlCT组相比nCT组表现出更好的疾病控制趋势。nICT组患者的局部区域复发风险(HR=0.52,P=0.018)和远处转移风险(HR=0.53,P=0.013)均显著低于nCT组(图2)。具体而言,nICT组的局部区域复发率(8.8% vs 11.6%)和远处转移率(12.6% vs 17.5%)均低于nCT组。复发后,两组患者接受的挽救性治疗模式相似(图3)。
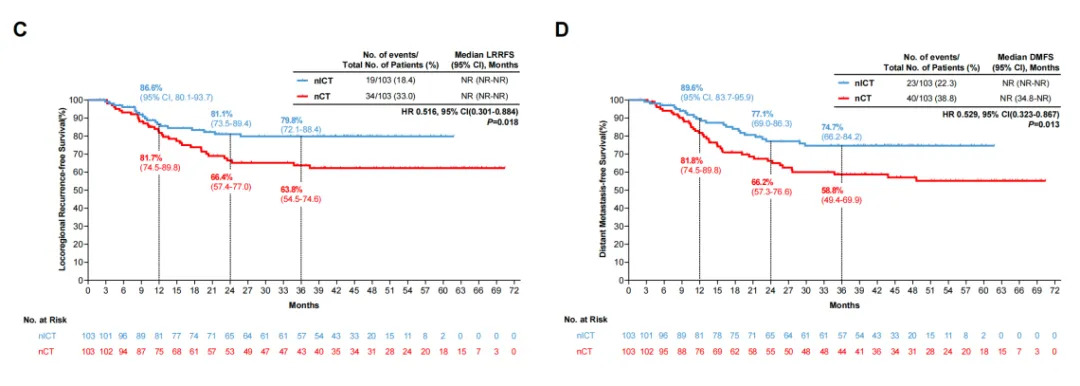
图2 PSM后的(C)LRRFS和(D)DMFS生存曲线图
(引自2025 ESMO Poster截图)
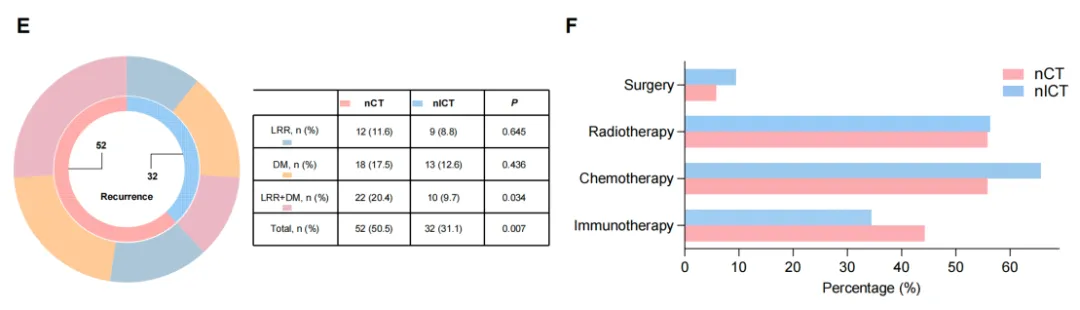
图3(E)失败模式比较;(F)挽救治疗模式
(引自2025 ESMO Poster截图)
3
病理评估:nICT实现更深度的肿瘤缓解
研究显示,nICT组的pCR率,达到23.2%,显著高于nCT组的12.1%。同时,nICT组的MPR率为47.2%,也显著优于nCT组的28.8%。多变量分析进一步证实,nICT是获得更高pCR率(OR=2.36, 95%CI: 1.10-5.32)和MPR率(OR=2.67, 95%CI: 1.43-5.10)的独立有利因素。nICT组患者的RVT%显著低于nCT组(中位数:11.0% vs 37.6%)(图4)。值得注意的是,这种病理缓解优势在局部晚期(cT3-4a)患者中尤为显著,该亚组nICT治疗后的中位RVT%远低于nCT组。
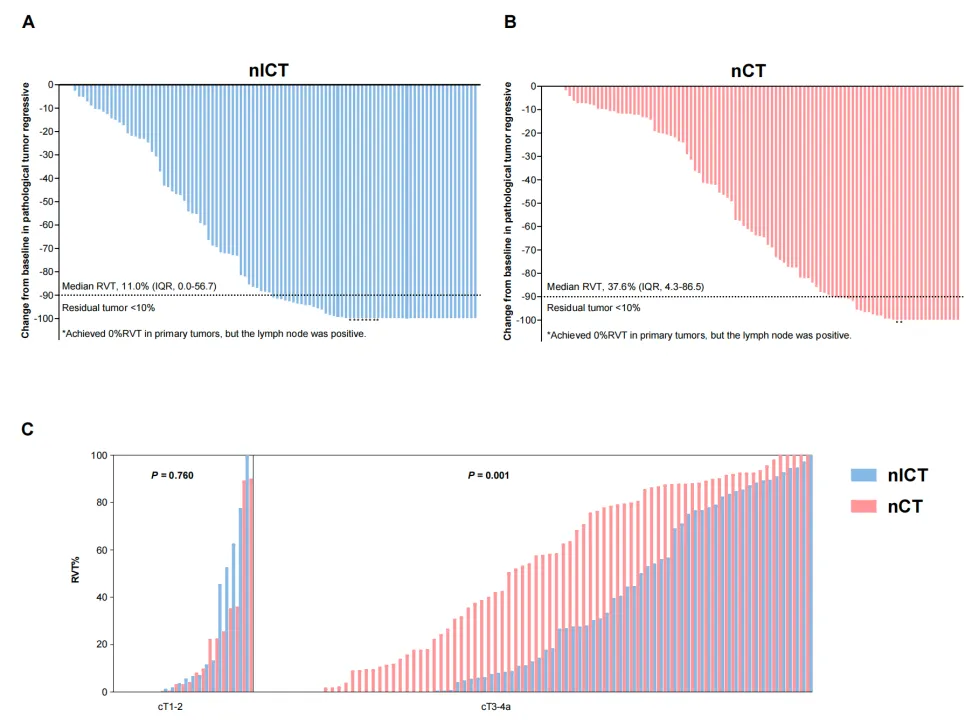
图4 (A) nICT组病理缓解深度;(B) nCT组病理缓解深度;(C) 不同基线分期下的RVT%差异
(引自2025 ESMO Poster截图)
对全部患者数据的样条分析揭示,RVT%与死亡风险存在显著非线性关系(P=0.034)。当RVT%低于25.02%时,其每增加一个标准差,死亡风险显著增加(HR=1.10, 95%CI: 1.03-1.17, P=0.003);高于此阈值时,风险关联不显著(图5)。基于此,研究提出将25.02%作为利用RVT%进行术后风险分层的临界值,为预后评估提供了明确的量化标准。
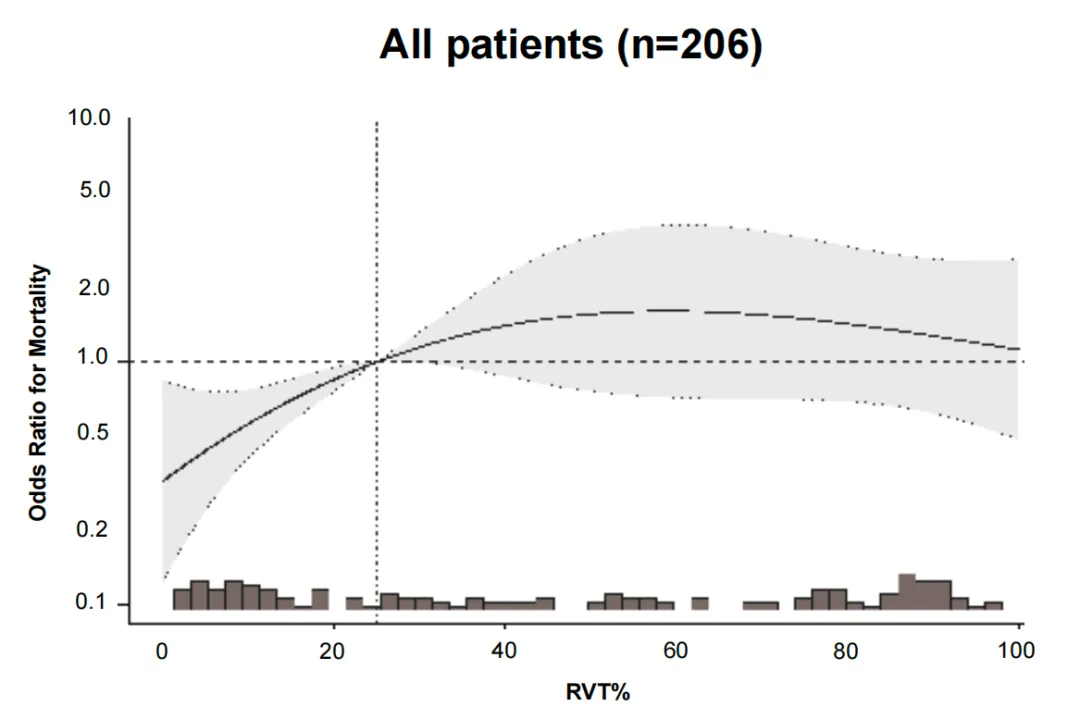
图5 RVT%与死亡风险的关联(非线性P值:0.034)
(引自2025 ESMO Poster截图)
4
机制探索:nICT重塑肿瘤免疫微环境
术后肿瘤样本的病理学分析显示,nICT不仅增强了肿瘤消退,还诱导了独特的免疫微环境重塑(图6)。与nCT组相比,nICT组患者肿瘤组织中三级淋巴结构(TLS)的形成显著更为常见。TLS的存在与更高的MPR率显著相关,提示其可能作为免疫激活与治疗响应的组织学标志。
除TLS外,肿瘤浸润淋巴细胞(TILs)的密度也与病理反应显著相关:在MPR患者中,TIL+++的比例显著更高,且多变量分析进一步证实TIL+++是总生存的独立保护因素(HR = 0.575, P = 0.039)。
此外,多个免疫相关病理特征在MPR与非MPR组间存在显著差异:非MPR组中泡沫细胞浸润、胆固醇裂隙和新生血管的比例更高,而增殖性纤维间质在MPR组中更为常见。这些特征共同描绘了nICT治疗后更为活跃的免疫细胞浸润与组织修复状态,从病理学角度揭示了其促进肿瘤深度缓解的潜在机制。
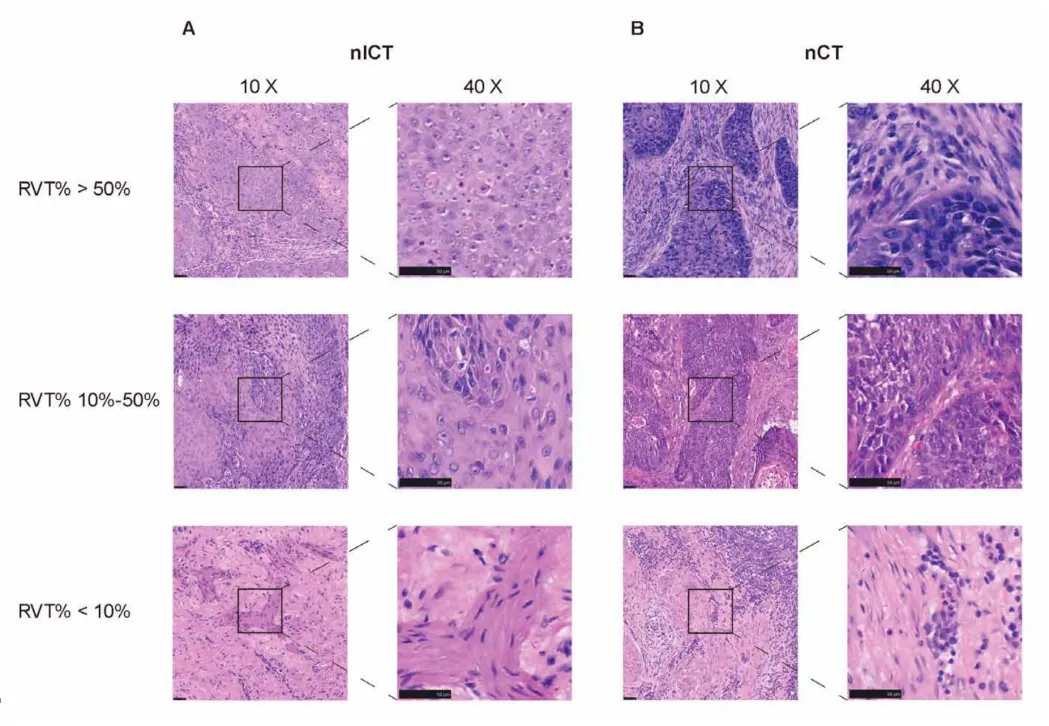
图6 不同RVT%状态的ESCC患者原发灶病理图像
(引自2025 ESMO Poster截图)
5
预后预测:个体化模型实现精准风险分层
研究开发并验证了一项个体化预后预测工具。通过LASSO回归和多因素Cox分析,确定了6个独立的预后因素并整合至预后列线图中,包括:① TILs密度高(TIL+++)、② 无泡沫细胞浸润、③ 未达到MPR、④ 淋巴结阳性、⑤ 无血管侵犯、⑥ 无脂肪组织侵犯。
该模型在训练队列中的区分度C-index高达0.813,在验证队列中亦达到0.780,表明其具有出色的预测准确性。时间依赖性ROC分析显示,模型在训练队列中预测12、24、36个月生存率的AUC值分别为0.759、0.744和0.733;在验证队列中分别为0.713、0.715和0.710,显示出稳健的预测性能。Kaplan-Meier分析明确证实,该模型能有效区分高风险与低风险患者,两组生存曲线差异显著(P
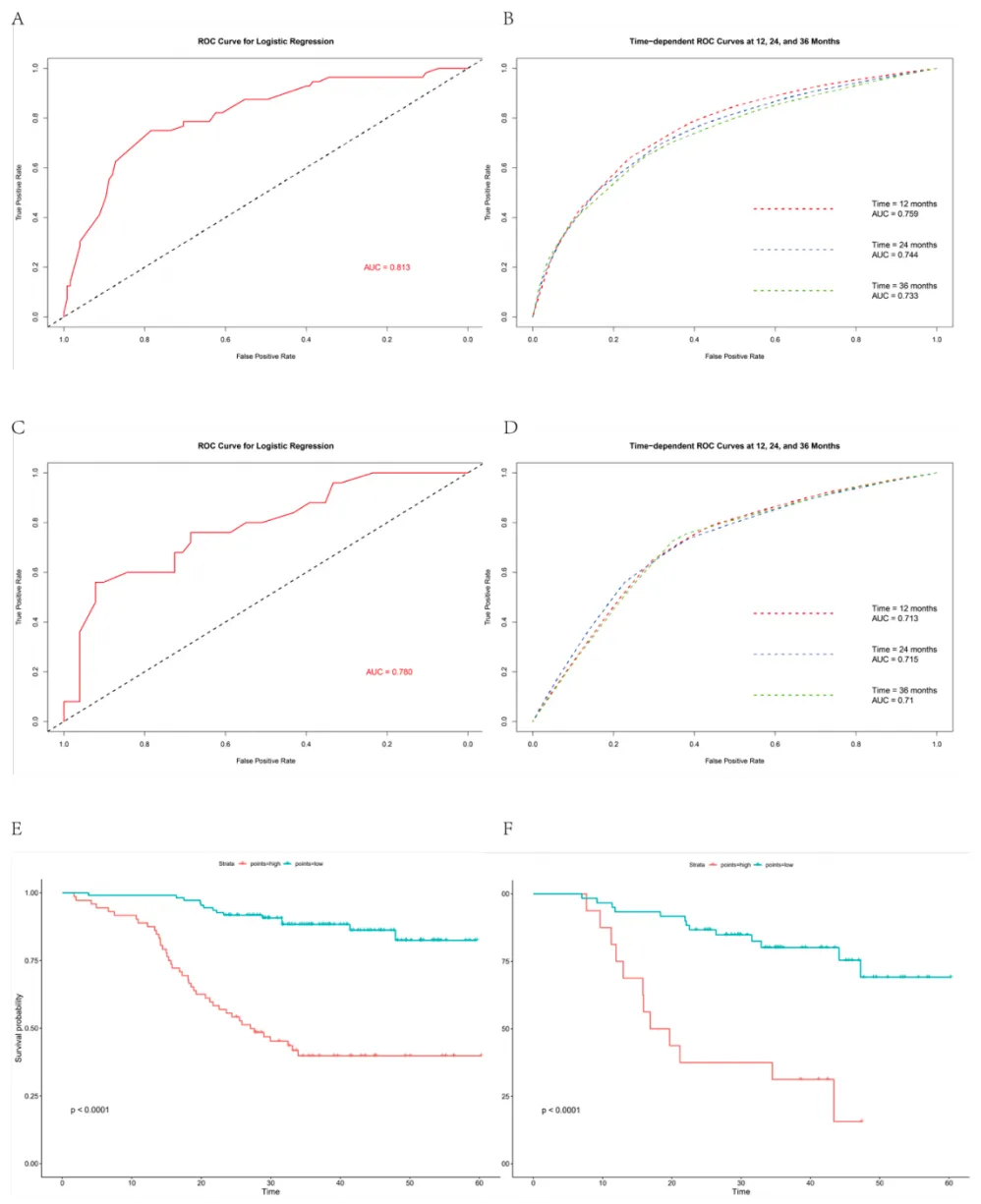
图7 预后列线图模型的区分效能与风险分层
(引自2025 ESMO Poster截图)
总结
本项回顾性研究证实,在可切除ESCC中,与nCT相比,nICT可显著改善EFS,诱导更深度的病理缓解,并降低RVT%,使患者生存获益。研究进一步系统揭示了与长期生存密切相关的三类关键特征:病理特征上,实现深度缓解(RVT%
曹国春 教授
博士,江苏省肿瘤医院内科主任医师,病区主任
中国临床肿瘤学会(CSCO)食管癌专家委员会副主任委员
中国临床肿瘤学会(CSCO)头颈部肿瘤专家委员会副主任委员
北京癌症防治学会食管癌专委会副主任委员
国家肿瘤质量控制中心食管癌质控专家组委员
国家肿瘤质量控制中心鼻咽癌质控专家组委员
中国抗癌协会鼻咽癌专委会委员
中国医师协会头颈部肿瘤专委会委员
中国医师协会食管癌学组委员
中国临床肿瘤学会(CSCO)临床研究专委会委员
江苏省抗癌联盟食管癌专委会副主任委员
江苏省肿瘤质量控制中心食管癌质控专家委员会副主委
江苏省抗癌协会食管癌专委会常委
江苏省抗癌协会头颈肿瘤专委会常委
王晓华 教授
医学博士,江苏省肿瘤医院内科 主任医师,
南京医科大学副教授,硕士生导师
美国UCSD大学,Moors癌症研究中心访问学者
中国临床肿瘤学会(CSCO)血管靶向治疗专委会委员
江苏省抗癌协会肿瘤精准治疗分会常务委员
江苏省医学会化疗与生物治疗委员会青委副主委
国家临床医学研究中心中国呼吸肿瘤协作组江苏分中心副主委
江苏省医学会疼痛学分会青委
江苏省抗癌协会营养学分会青委
江苏省研究型医师协会肺癌与肺结节MDT专委会委员
江苏省康复医学会肿瘤康复医学会委员
江苏省CRDS-NET学会委员
迄今主持课题6项,已发表论文40余篇,其中SCI收录30余篇。
获得江苏省卫健委新技术引进奖二等奖一项。
陈诚 教授
医学博士,副教授,南京医科大学、徐州医科大学、内蒙古医科大学研究生导师
内蒙古医科大学附属肿瘤医院副院长(挂职)
江苏省肿瘤医院医疗质量管理办公室主任
江苏省医学会放射治疗专业委员会青委副主任委员
江苏省医师协会放射肿瘤治疗医师分会委员
江苏省抗癌协会肿瘤精准治疗专业委员会委员
江苏省整合医学研究会肺癌专业委员会委员
中华医学会放射肿瘤治疗学分会青委
中华医学会放射肿瘤治疗学分会放射外科学组委员
中国老年学和老年医学学会精准医疗分会委员
中国人体健康科技促进会立体定向放射外科专业委员会委员
中国老年学和老年医学学会肿瘤康复分会委员
英国Guy's and St Thomas' NHS Foundation Trust 访问学者
赵丽君 医生
江苏省肿瘤医院放疗科主治医师
南京医科大学肿瘤学博士
南京医科大学讲师
江苏省肿瘤精准防治分会委员
获江苏省新技术引进奖二等奖一项
发表SCI及中华系列论文多篇
主持IIT临床研究两项,参与临床研究七项
主要工作方向:肿瘤大分割放疗
李静文
江苏省肿瘤医院,肿瘤科,硕士在读
主要研究方向:食管癌的基础与临床
2020-2021年度 校优秀学生三等奖学金
2022年度 第二届全国医学词汇大赛一等奖
卢麟
医学硕士,南京医科大学放射肿瘤学专业
苏州大学附属第一医院放疗科住院医师
研究方向:食管癌新辅助免疫治疗临床及转化研究
参考文献:
[1] Jingwen Li, et al. 2025 ESMO abstract 2120P.
[2] Xiaohua Wang, et al. 2025 ESMO abstract 2167P.
[3] Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024 May-Jun;74(3):229-263. doi: 10.3322/caac.21834.
[4] GRONNIER C, TRÉCHOT B, DUHAMEL A, et al. Impact of neoadjuvant chemoradiotherapy on postoperative outcomes after esophageal cancer resection: results of a European multicenter study[J]. Ann Surg, ;260(5):764-770.
[5] Topalian SL ,Drake CG ,Pardoll DM . Immune checkpoint blockade: a common denominator approach to cancer the-rapy[J]. Cancer Cell, 2015,27(4):450-461.
编辑:Chiu
审校:Dreams
排版:Uni
执行:Squid
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。







