
SG结构优势独特,HR+/HER2-晚期乳腺癌疗效安全双优
抗体药物偶联物(ADC)凭借其精准的靶向递送机制,在肿瘤治疗中疗效显著。其核心结构由单克隆抗体、连接子以及细胞毒性有效载荷三部分构成[1],通过抗体结合肿瘤抗原,ADC内化降解,释放活性细胞毒性物质诱导肿瘤细胞死亡[2]。这一特性在提升抗肿瘤疗效的同时,也能保障患者的疗效和安全性。
然而,与所有抗肿瘤药物相似,ADC在应用过程中也会出现相关不良反应。随着ADC在HR+/HER2-晚期乳腺癌 的治疗中的应用日益广泛,相关不良反应的管理已成为临床实践中的关键议题。同时,由于HR+/HER2-晚期乳腺癌需要长期接受系统性治疗,若不良反应未及时干预,可能引发治疗延迟甚至中止,影响抗肿瘤效果。因此,科学评估ADC药物的安全性特征并制定全面的管理措施,对优化HR+/HER2-晚期乳腺癌治疗策略、改善患者预后具有重要的意义。
的治疗中的应用日益广泛,相关不良反应的管理已成为临床实践中的关键议题。同时,由于HR+/HER2-晚期乳腺癌需要长期接受系统性治疗,若不良反应未及时干预,可能引发治疗延迟甚至中止,影响抗肿瘤效果。因此,科学评估ADC药物的安全性特征并制定全面的管理措施,对优化HR+/HER2-晚期乳腺癌治疗策略、改善患者预后具有重要的意义。
疗效突破:SG为HR+/HER2-晚期乳腺癌打造超越化疗的生存新路径
戈沙妥珠单抗(SG)是全球首个获批用于治疗HR+/HER2-晚期乳腺癌的Trop-2靶向ADC药物,其在HR+/HER2-晚期乳腺癌患者中的疗效与安全性已获多项临床研究验证。
全球Ⅲ期TROPiCS-02研究对比了SG与医生选择的化疗(TPC)用于曾接受内分泌治疗、CDK4/6抑制剂以及2–4线化疗的HR+/HER2-晚期乳腺癌患者的疗效与安全性。结果显示,SG较TPC可显著改善患者的中位无进展生存期(mPFS:5.5个月 vs 4.0个月,HR=0.66)和总生存期(mOS:14.4个月 vs 11.2个月,HR=0.79)[3]。
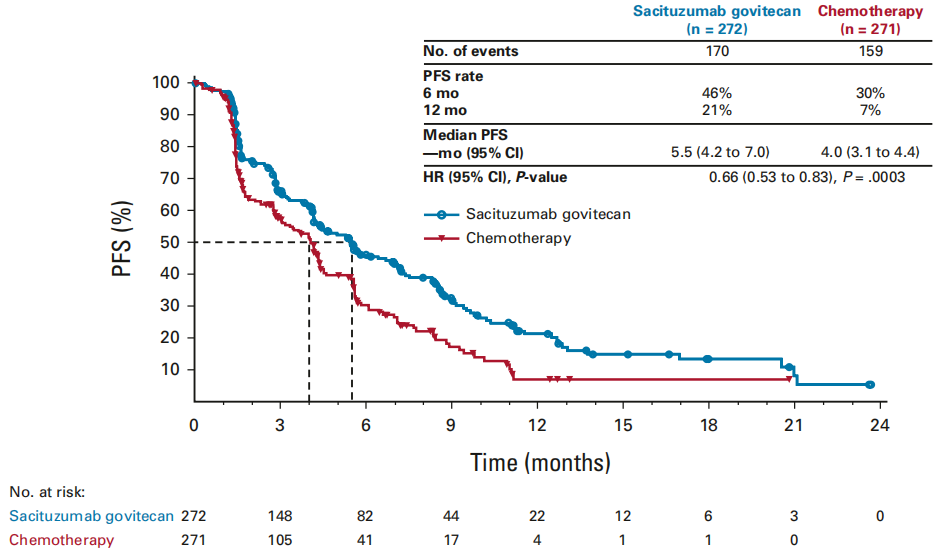
TROPiCS-02研究中患者的PFS生存曲线(BICR)[3]
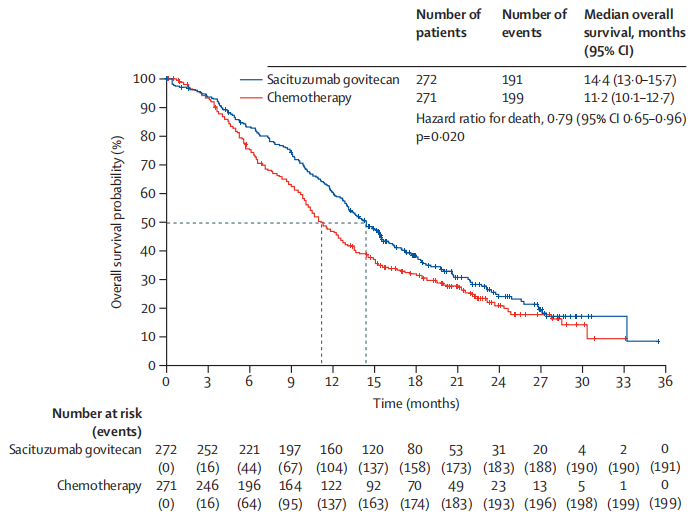
TROPiCS-02研究中患者的OS生存曲线[3]
随后开展的亚洲桥接研究EVER-132-002,进一步验证了SG在亚洲HR+/HER2-晚期乳腺癌患者中的疗效与安全性,尤其是在中国人群中,SG获益更加突出:SG相较化疗可显著改善HR+/HER2-晚期乳腺癌患者的mPFS(5.5个月 vs 4.1个月,HR=0.622)和mOS(20.5个月 vs 15.1个月,HR=0.583)[4]。
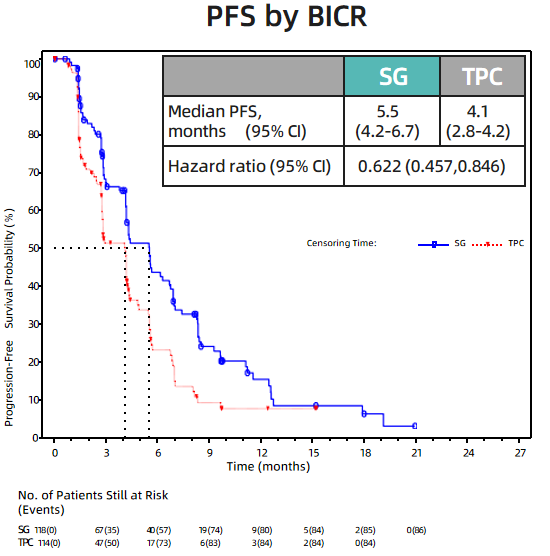
EVER-132-002研究中国亚组人群的PFS生存曲线(BICR)[4]
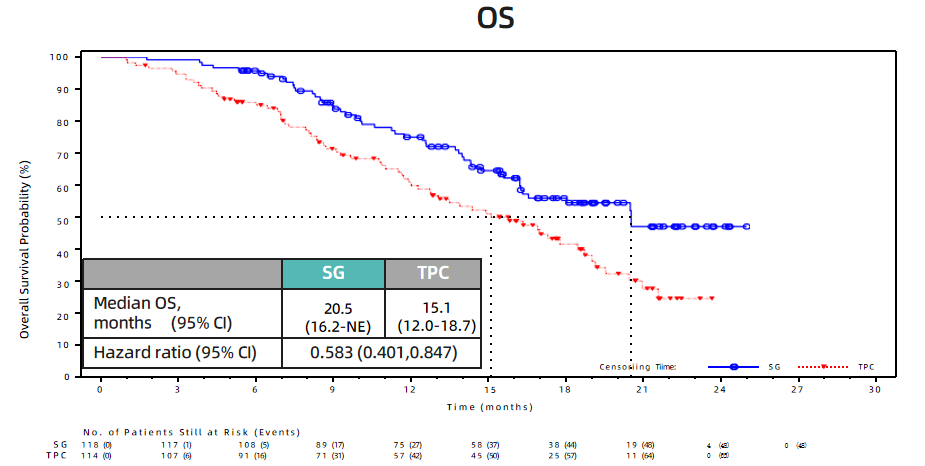
EVER-132-002研究中国亚组人群的OS生存曲线[4]
安全可控:SG的安全性特征与临床管理策略
SG在HR+/HER2-晚期乳腺癌治疗中,不仅疗效获益显著,安全性特征也整体可控。TROPiCS-02研究显示,SG治疗组常见的任何级别血液学不良事件包括中性粒细胞减少(71%)、贫血 (37%);非血液学毒性则以腹泻
(37%);非血液学毒性则以腹泻 (62%)、恶心(59%)和脱发(48%)为主。最常见的≥3级治疗中出现的不良事件为中性粒细胞减少(51%)与腹泻(10%),停药率为6%,整体安全可控[3]。
(62%)、恶心(59%)和脱发(48%)为主。最常见的≥3级治疗中出现的不良事件为中性粒细胞减少(51%)与腹泻(10%),停药率为6%,整体安全可控[3]。
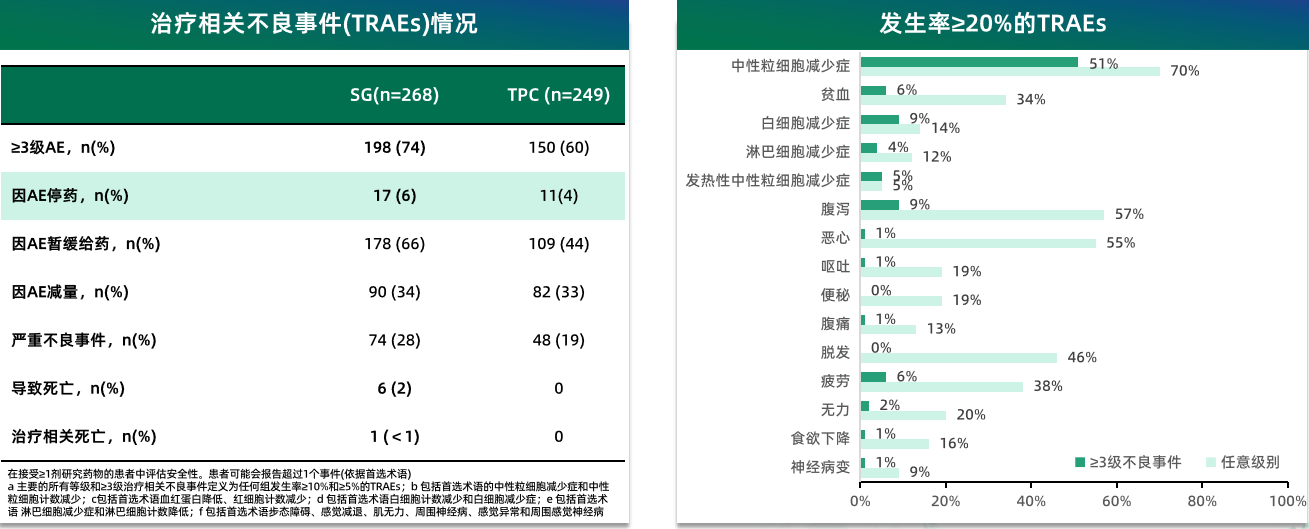
TROPiCS-02研究中治疗期间出现的不良事件汇总及不良反应谱[3]
EVER-132-002研究中[5],SG的安全性特征与TROPiCS-02研究基本一致。这两项研究表明,不论欧美还是亚太地区人种,SG常见的不良反应均以血液学毒性和胃肠道反应为主,包括中性粒细胞减少症、贫血及腹泻等,未出现口腔炎,眼毒性及间质性肺病 等特殊不良反应事件。
等特殊不良反应事件。
针对SG引发的中性粒细胞减少症,当中性粒细胞绝对计数低于1500/mm3或中性粒细胞减少症发热 时,应暂停使用SG治疗,并且在治疗期间定期监测血细胞计数。此外,《注射用戈沙妥珠单抗
时,应暂停使用SG治疗,并且在治疗期间定期监测血细胞计数。此外,《注射用戈沙妥珠单抗 说明书》建议所有发热性中性粒细胞减少症风险较高的患者使用粒细胞集落刺激因子
说明书》建议所有发热性中性粒细胞减少症风险较高的患者使用粒细胞集落刺激因子 (G-CSF)进行一级预防;发热性中性粒细胞减少症患者应立即开始抗感染治疗[6]。
(G-CSF)进行一级预防;发热性中性粒细胞减少症患者应立即开始抗感染治疗[6]。
在非血液学毒性中,腹泻较为常见,发生腹泻的患者应按需给予补液和电解质治疗,并且及时评估感染原因,如无感染,应立即给予洛哌丁胺 。如果发生重度腹泻,应暂停使用SG治疗直至恢复至≤1级,并降低后续治疗剂量[6]。
。如果发生重度腹泻,应暂停使用SG治疗直至恢复至≤1级,并降低后续治疗剂量[6]。
结构独特:SG的抗肿瘤机制优势
SG在临床试验中展现出的卓越疗效和可控的安全性,得益于其独特的结构设计,其核心结构主要包含三部分:人源化抗Trop-2单克隆抗体、可水解的CL2A连接子以及拓扑异构酶I抑制剂SN-38作为有效载荷,药物抗体比约为7.6。其中,SN-38的中等效力特性允许临床可采用相对较高的给药剂量(10mg/kg),以提升肿瘤组织渗透性。此外,连接子在细胞外裂解可介导空间旁观者效应,使载药在肿瘤微环境释放并渗透肿瘤组织,从而克服结合位点屏障与抗原表达异质性;在细胞内裂解则介导异质性旁观者效应,使载药从靶抗原表达阳性细胞释放,作用于邻近靶抗原表达阴性细胞,进一步克服抗原表达异质性。这种双重旁观者效应使得SG在应用前无需检测Trop-2,且抗肿瘤疗效不受肿瘤异质性的影响[7]。
在抗肿瘤过程中,SG的抗体部分与肿瘤细胞表面的Trop-2抗原结合,经内化进入细胞,随后CL2A连接子在细胞内环境中快速水解,释放出SN-38,导致DNA双链断裂和细胞死亡[7]。值得注意的是,CL2A连接子在血液循环中的适度水解减少了ADC在表达Trop-2的正常组织中(例如眼部、口腔黏膜等)的有效载荷累积,从而降低了潜在不良反应发生风险(例如眼毒性、口腔炎)[7]。
小结
综上,SG作为全球首个用于HR+/HER2-晚期乳腺癌治疗的Trop-2靶向 ADC,依托“抗Trop-2抗体-CL2A连接子-SN-38”的独特结构,既克服了肿瘤异质性,又降低了潜在不良反应发生风险。TROPiCS-02与EVER-132-002两项研究也证实SG具有出色的疗效和安全性,可显著延长内分泌耐药后经治HR+/HER2-患者的PFS与OS,具有良好的安全性。其安全性特征以血液学毒性和胃肠道反应为主,可通过规范监测、预防性用药及剂量调整等措施有效管理。综上,SG实现了高效肿瘤杀伤与毒性可控的平衡,为内分泌耐药的经治HR+/HER2-晚期乳腺癌患者提供了新的治疗选择,对优化该类患者的治疗策略、改善长期预后具有重要临床意义。
审批编号:CN-TRO-0359 仅供医疗专业人士参考
有效期至:2026年11月19日
