
2025ASH丨姜尔烈教授团队:亚洲患者数据添力证,吉瑞替尼展现治疗优势,助力FLT3突变AML移植全程管理
FMS样酪氨酸激酶3(FLT3)突变是急性髓系白血病 (AML)患者常见的基因突变之一,严重影响预后。异基因造血干细胞移植(allo-HSCT)是FLT3突变AML重要治疗策略,构建规范化移植管理体系、拓宽移植获益人群、降低移植后复发风险对改善患者预后至关重要。近年来,靶向药物的快速发展为AML治疗开辟了新路径,其与移植的联合应用已成为临床研究热点。其中,吉瑞替尼
(AML)患者常见的基因突变之一,严重影响预后。异基因造血干细胞移植(allo-HSCT)是FLT3突变AML重要治疗策略,构建规范化移植管理体系、拓宽移植获益人群、降低移植后复发风险对改善患者预后至关重要。近年来,靶向药物的快速发展为AML治疗开辟了新路径,其与移植的联合应用已成为临床研究热点。其中,吉瑞替尼 作为高选择性FLT3抑制剂,在移植全程管理中的应用价值备受关注。
作为高选择性FLT3抑制剂,在移植全程管理中的应用价值备受关注。
2025年12月6日~9日,第67届美国血液学会(ASH)年会在奥兰多盛大召开,中国医学科学院血液病 医院(中国医学科学院血液学研究所)姜尔烈
医院(中国医学科学院血液学研究所)姜尔烈 教授团队多项高质量研究成果惊艳亮相,特别是AML移植相关领域的创新探索尤为引人注目。基于此,医脉通特整理相关精彩内容,以飨读者。
教授团队多项高质量研究成果惊艳亮相,特别是AML移植相关领域的创新探索尤为引人注目。基于此,医脉通特整理相关精彩内容,以飨读者。

FLT3突变是AML患者较为常见的突变之一,发生率约30%,包括内部串联重复(ITD)突变和酪氨酸激酶结构域(TKD)突变,其中,FLT3-ITD突变更为常见1,2。FLT3突变影响AML患者预后,与非FLT3-ITD突变患者相比,FLT3-ITD突变患者首次诱导治疗后完全缓解(CR)率+部分缓解(PR)率显著较低(31.6% vs 64.9%,P<0.05,图1),中位总生存期(OS)明显更短(5个月 vs 18个月,P<0.05)3。此外,与FLT3野生型患者相比,FLT3-ITD突变AML患者发生高白细胞血症风险更高,且复发更快、更难治4。
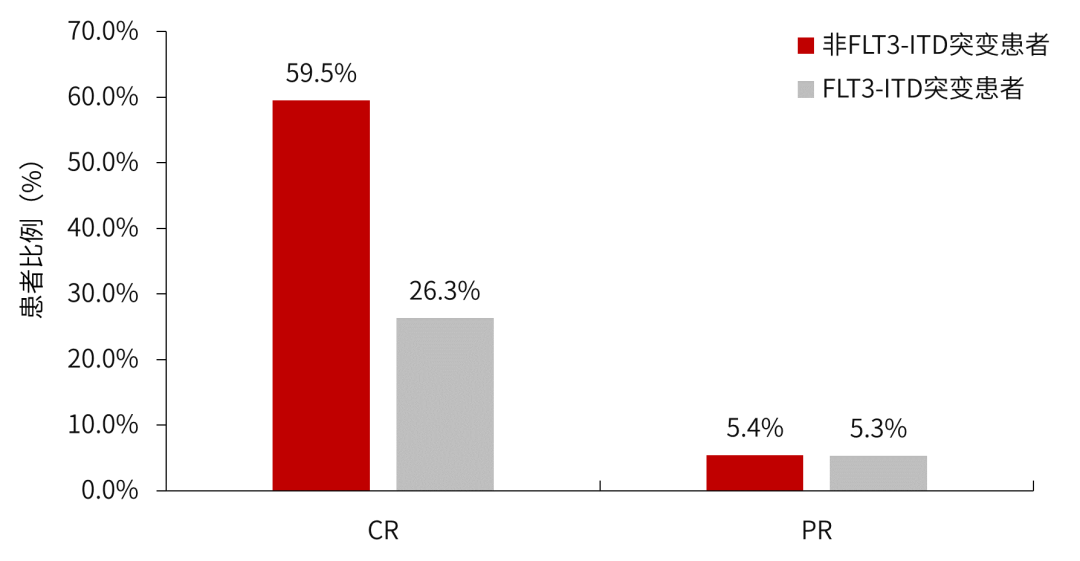
图1.非FLT3-ITD突变和FLT3-ITD突变AML患者首次诱导治疗后缓解率
然而,传统化疗难以克服FLT3突变AML患者的不良预后,与巩固化疗相比,首次完全缓解后接受HSCT的患者生存获益更佳(3年OS率:54% vs 24%,P<0.001;3年无复发生存[RFS]率:46% vs 18%,P<0.001)5。基于此,对于预后中等和预后不良的FLT3突变AML患者,国内外权威指南一致推荐诱导缓解后优选HSCT治疗6-8。
打通移植前壁垒,吉瑞替尼助力更多AML患者获得allo-HSCT机会
近年来,随着对疾病分子生物学研究的深入,FLT3抑制剂等靶向药物不断涌现并广泛应用于AML临床治疗,其中,口服、高选择性的FLT3抑制剂吉瑞替尼单药及联合方案已被证实可提高FLT3突变复发/难治性(R/R)AML患者缓解率并改善生存结局,其在移植全程管理中的应用价值也逐渐受到临床关注。中国医学科学院血液病医院(中国医学科学院血液学研究所)一项回顾性队列研究评估了吉瑞替尼、维奈克拉 、阿扎胞苷
、阿扎胞苷 三药联合方案在FLT3-ITD突变AML患者(包括R/R或持续微小残留病[MRD]阳性)中的疗效与安全性,探索了其作为allo-HSCT桥接治疗的价值,并入选2025ASH壁报,该研究结果显示9:
三药联合方案在FLT3-ITD突变AML患者(包括R/R或持续微小残留病[MRD]阳性)中的疗效与安全性,探索了其作为allo-HSCT桥接治疗的价值,并入选2025ASH壁报,该研究结果显示9:
接受一周期三药联合方案治疗后,81.3%的患者达到CR/完全缓解伴不完全血液学恢复(CRi)并接受allo-HSCT,其余18.7%的患者以活动性疾病状态接受移植。治疗过程中未观察到治疗相关死亡,所有患者均接受清髓性预处理并成功植入,造血重建在移植后+60天内完成,并于移植后+30天~+90天内启动吉瑞替尼维持治疗;
截至本次分析,83.3%的患者存活,存活患者中位随访时间16.6个月,1年OS率和RFS率分别为83.3%和75.0%,1年累积复发率和非复发死亡率(NRM)分别为14.6%和10.4%。
该研究表明,以吉瑞替尼为基础的联合方案可在FLT3-ITD突变R/R AML或持续MRD阳性患者中实现较高的CR/CRi率,并有效提升allo-HSCT的可行性,序贯进行allo-HSCT并联合移植后吉瑞替尼维持治疗,可改善患者的长期预后。
筑牢移植后防线,早期预测复发风险+吉瑞替尼维持治疗助力改善AML患者长期预后
allo-HSCT后复发是导致AML患者治疗失败的重要原因,研究显示,约40%的AML患者在移植后出现疾病复发,1年OS率<25%,2年OS率<20%,且国际血液和骨髓移植中心(CIBMTR)资料显示,复发在移植后死因中占30%~60%10,11,因此,早期识别高复发风险患者并进行有效预防尤为重要。
2025ASH会议上,中国医学科学院血液病医院(中国医学科学院血液学研究所)NICHE-BMT队列研究显示,在经毛细管电泳检测FLT3-ITD阴性的患者中,27.2%的患者在移植后+30天通过高灵敏度二代测序(NGS)检测出FLT3-ITD克隆,并在移植后表现出更高的MRD阳性累积发生率,且值得注意的是,在FLT3-ITD阳性患者中,接受维持治疗的患者2年累积复发率(CIR)显著低于未接受维持治疗的患者(0.0% vs 54.3%,P=0.003)12。该研究证实了在移植后+30天检测到FLT3-ITD克隆可指导AML患者复发风险分层,并为移植后维持治疗提供了理论依据。
目前,移植后维持治疗已成为降低复发风险的重要措施,但既往维持治疗方案存在药物相关不良反应多、移植物抗宿主病 (GVHD)发生风险等挑战,而靶向药物的不断问世促使AML移植后维持治疗疗效得到明显提高11。中国回顾性研究显示,与未接受吉瑞替尼维持治疗的患者(对照组)相比,接受吉瑞替尼维持治疗的患者3年OS率显著提高(79.1% vs 53.0%,P=0.013),RFS明显延长(P=0.026,图2),3年CIR明显降低(25.0% vs 55.0%,P=0.010),且吉瑞替尼未增加患者GVHD发生风险(图3),总体耐受性良好,提示吉瑞替尼或可作为FLT3突变R/R AML患者移植后维持治疗的理想选择13。
(GVHD)发生风险等挑战,而靶向药物的不断问世促使AML移植后维持治疗疗效得到明显提高11。中国回顾性研究显示,与未接受吉瑞替尼维持治疗的患者(对照组)相比,接受吉瑞替尼维持治疗的患者3年OS率显著提高(79.1% vs 53.0%,P=0.013),RFS明显延长(P=0.026,图2),3年CIR明显降低(25.0% vs 55.0%,P=0.010),且吉瑞替尼未增加患者GVHD发生风险(图3),总体耐受性良好,提示吉瑞替尼或可作为FLT3突变R/R AML患者移植后维持治疗的理想选择13。
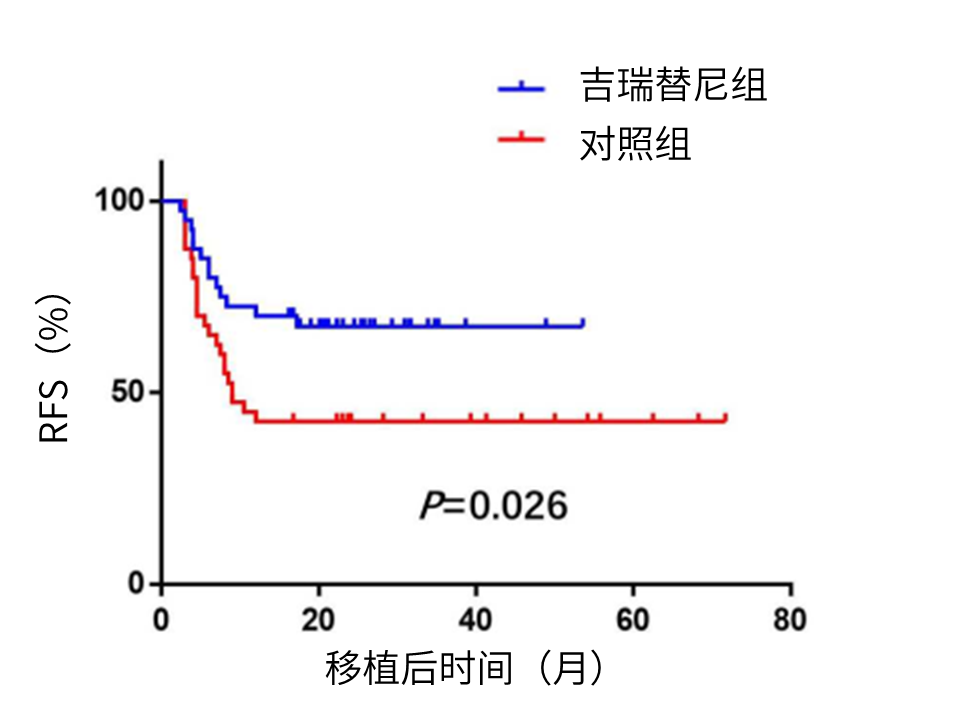
图2.倾向性评分匹配后患者RFS
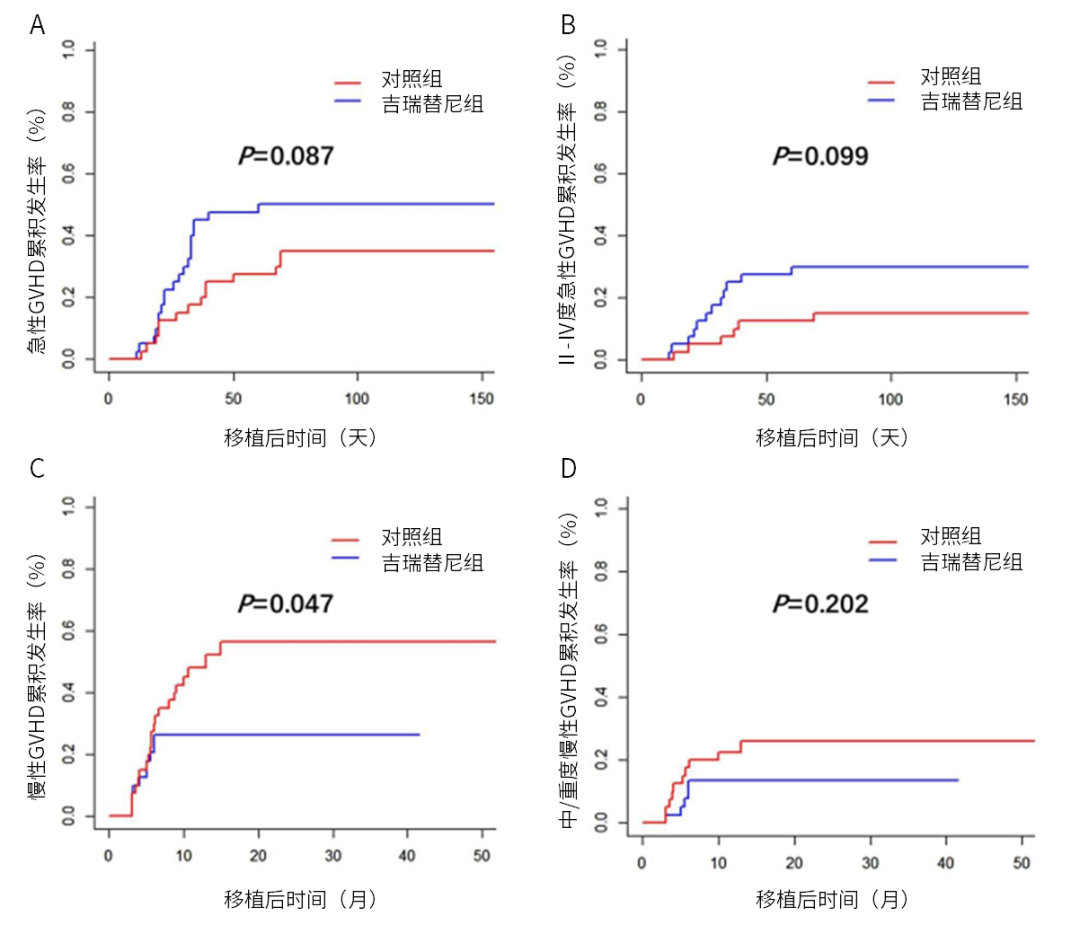
图3.倾向性评分匹配后患者GVHD发生率(A:急性GVHD累积发生率;B:Ⅱ-Ⅳ度急性GVHD累积发生率;C:慢性GVHD累积发生率;D:中/重度慢性GVHD累积发生率)
FLT3突变作为AML患者常见突变,严重影响患者预后。目前,allo-HSCT仍是FLT3突变AML患者重要治疗策略,而构建规范化移植管理体系、拓宽移植获益人群、降低移植后复发风险已成为当前临床研究与实践的重点议题。吉瑞替尼作为上市近5年的二代高选择性FLT3抑制剂,其临床获益已得到充分验证。本届ASH会议公布的最新研究数据,进一步证实了其在AML患者allo-HSCT全程管理中的积极作用。期待未来能开展更多高质量临床研究,深入探索吉瑞替尼的最佳用药时机及联合治疗策略,并加速科研成果向临床实践的转化,为更多FLT3突变AML患者带来治疗福祉。

姜尔烈 教授
中国医学科学院血液病医院(中国医学科学院血液学研究所)副院(所)长
参考文献:
1. Song MK, et al. Int J Mol Sci. 2022;23(20):12708.
2. Perrone S, et al. Cancer Drug Resist. 2023;6(2):223-238.
3. 刘彦,等.中国实验血液学杂志.2018;26( 2):354-358.
4. Bystrom R, et al. Curr Oncol Rep. 2023 Apr;25(4):369-378.
5. Oran B, et al. Biol Blood Marrow Transplant. 2016 Jul;22(7):1218-1226.
6. NCCN Clinical Practice Guidelines in Oncology Acute Myeloid Leukemia. Version 3.2026.
7. 中国临床肿瘤学会指南工作委员会.中国临床肿瘤学会(CSCO)恶性血液病诊疗指南(2025).人民卫生出版社.2025.
8. 中国肿瘤整合诊治指南(CACA)白血病.V2.0_2025.
9. Erlie Jiang, et al. 2025ASH. abs25-9418.
10. 徐岳一 ,等.国际输血
,等.国际输血 及血液学杂志.2023;46(03):206-215.
及血液学杂志.2023;46(03):206-215.
11. 郑欣慧,等.白血病·淋巴瘤.2023;32(08):505-509.
12. Shan Jiang, et al. 2025ASH. abs25-7966.
13. Liang C,et al.Hematology.2025 Dec;30(1):2509353.

