
石远凯教授:迄今为止最大规模探索基因变异图谱GPS研究登顶顶尖学术期刊STTT,夯实EGFR突变NSCLC进展后循证基础


前言

近日,一项由全国16家医院联合开展的前瞻性、多中心真实世界GPS研究(NCT05219162)全文重磅发布于国际知名学术期刊Signal Transduction and Targeted Therapy(影响因子52.7)1,该研究首次前瞻性的进行最大样本量的肿瘤组织与血浆样本配对,对在表皮生长因子受体(EGFR)突变的局部晚期或转移性非小细胞肺癌 (NSCLC)患者在奥希替尼
(NSCLC)患者在奥希替尼 一线治疗进展时的全基因变异图谱(GPS)进行全面且更准确的分析,此外,该研究从基因共变异的角度进行了深入的分析,并进一步创新性评估了下一代测序(NGS)、滴度数字PCR(ddPCR)与荧光原位杂交(FISH)等多种检测方法在MET扩增检测中的表现,这些重要研究成果为未来的临床研究以及临床实践提供了高质量循证医学证据。值此研究成果公布之际,医脉通特邀GPS主要研究者、中国医学科学院肿瘤医院石远凯
一线治疗进展时的全基因变异图谱(GPS)进行全面且更准确的分析,此外,该研究从基因共变异的角度进行了深入的分析,并进一步创新性评估了下一代测序(NGS)、滴度数字PCR(ddPCR)与荧光原位杂交(FISH)等多种检测方法在MET扩增检测中的表现,这些重要研究成果为未来的临床研究以及临床实践提供了高质量循证医学证据。值此研究成果公布之际,医脉通特邀GPS主要研究者、中国医学科学院肿瘤医院石远凯 教授深入解读该研究的核心发现与临床启示,旨在为临床医生在一线奥希替尼进展后的基因谱分析与治疗决策提供实用参考。
教授深入解读该研究的核心发现与临床启示,旨在为临床医生在一线奥希替尼进展后的基因谱分析与治疗决策提供实用参考。

三代EGFR-TKI进展难题待解
GPS研究提供破局高质量证据
奥希替尼作为首个获批的第三代EGFR酪氨酸激酶抑制剂(EGFR-TKI),在FLAURA研究中已证实其相较于吉非替尼 /厄洛替尼
/厄洛替尼 组,在携带EGFR第19外显子缺失(Ex19del)或L858R突变的晚期NSCLC患者中具有显著临床获益,中位无进展生存期(PFS)为18.9个月 vs. 10.2个月(HR=0.46,P<0.001)2,是具有总生存期(OS)显著获益的三代EGFR-TKI,中位OS为38.6个月 vs. 31.8个月(HR=0.80,P=0.0462)3,尤其是在针对中枢神经系统(CNS)转移方面表现突出,中位CNS PFS分别为NR vs. 13.9个月(HR=0.48,P=0.014)4。此外,其他第三代EGFR-TKI亦在临床研究中显示出良好的抗肿瘤活性和CNS活性,例如,FURLONG研究和AENEAS研究显示,伏美替尼
组,在携带EGFR第19外显子缺失(Ex19del)或L858R突变的晚期NSCLC患者中具有显著临床获益,中位无进展生存期(PFS)为18.9个月 vs. 10.2个月(HR=0.46,P<0.001)2,是具有总生存期(OS)显著获益的三代EGFR-TKI,中位OS为38.6个月 vs. 31.8个月(HR=0.80,P=0.0462)3,尤其是在针对中枢神经系统(CNS)转移方面表现突出,中位CNS PFS分别为NR vs. 13.9个月(HR=0.48,P=0.014)4。此外,其他第三代EGFR-TKI亦在临床研究中显示出良好的抗肿瘤活性和CNS活性,例如,FURLONG研究和AENEAS研究显示,伏美替尼 组和阿美替尼
组和阿美替尼 组分别取得了20.8个月5和19.3个月6的中位PFS,CNS PFS分别为20.8个月7和29.0个月8,为EGFR突变NSCLC患者带来了更多治疗选择,但OS获益仍有待进一步验证。然而,几乎所有患者最终都会出现疾病进展,且进展后治疗选择有限。深入了解第三代 EGFR-TKI奥希替尼治疗失败后的基因变异图谱,有助于探索更具有针对性的治疗策略,从而改善晚期NSCLC患者的生存结局与生活质量。
组分别取得了20.8个月5和19.3个月6的中位PFS,CNS PFS分别为20.8个月7和29.0个月8,为EGFR突变NSCLC患者带来了更多治疗选择,但OS获益仍有待进一步验证。然而,几乎所有患者最终都会出现疾病进展,且进展后治疗选择有限。深入了解第三代 EGFR-TKI奥希替尼治疗失败后的基因变异图谱,有助于探索更具有针对性的治疗策略,从而改善晚期NSCLC患者的生存结局与生活质量。
值得注意的是,疾病进展阶段肿瘤组织样本获取较为困难,液体活检逐渐成为识别进展机制的重要替代手段。然而,既往关于奥希替尼进展机制的研究多依赖于回顾性小样本、单一液体活检或缺乏组织验证,难以全面捕捉肿瘤异质性、拷贝数变异(CNV)及组织学转化等关键问题,限制了其替代组织活检的潜力。鉴于肿瘤组织获取受限,探索组织与血浆基因图谱之间的一致性则是至关重要的。
MET扩增是奥希替尼一线治疗失败的重要进展变异。目前 FISH是检测MET扩增的金标准,但其临床应用受到肿瘤高度异质性及组织样本难获取的限制,对FISH的实际临床应用构成了挑战。此外,NGS在临床实践中广泛应用MET扩增的检测,但仍需要进一步明确与FISH 检测MET扩增的一致性。ddPCR是一种高敏感性和高特异性的技术,可使用血浆样本检测MET扩增,但其与组织FISH的诊断一致性仍需进一步证实。
鉴于基因图谱在指导后续治疗中的重要性,GPS研究应运而生。该研究前瞻性采集一线奥希替尼治疗进展时的组织与配对血浆样本,系统解析了奥希替尼进展后的基因图谱,此外采用NGS、ddPCR、FISH等技术,评价了NGS与ddPCR在MET扩增检测方面与组织FISH的一致性,为精准识别进展后基因图谱、优化检测路径及指导后续个体化治疗提供了高质量循证医学证据。
破解三代EGFR-TKI进展
GPS研究全面揭示基因变异图谱
2022年2月25日至2024年4月29日期间,研究共入组182例接受奥希替尼一线治疗失败的EGFR敏感突变(Ex19del/L858R)晚期NSCLC患者,其中,149例具有配对组织和血浆样本的患者被纳入全分析集(FAS)进行最终分析。结果显示,奥希替尼一线治疗失败时的基因组改变可归纳为三大类:EGFR通路相关变异、旁路信号通路激活以及下游通路失调,首次通过大样本量的基因组分析,全面且清晰的清晰地构建了进展后基因变异图谱。为一线奥希替尼治疗进展后的诊疗探索提供了循证参考。
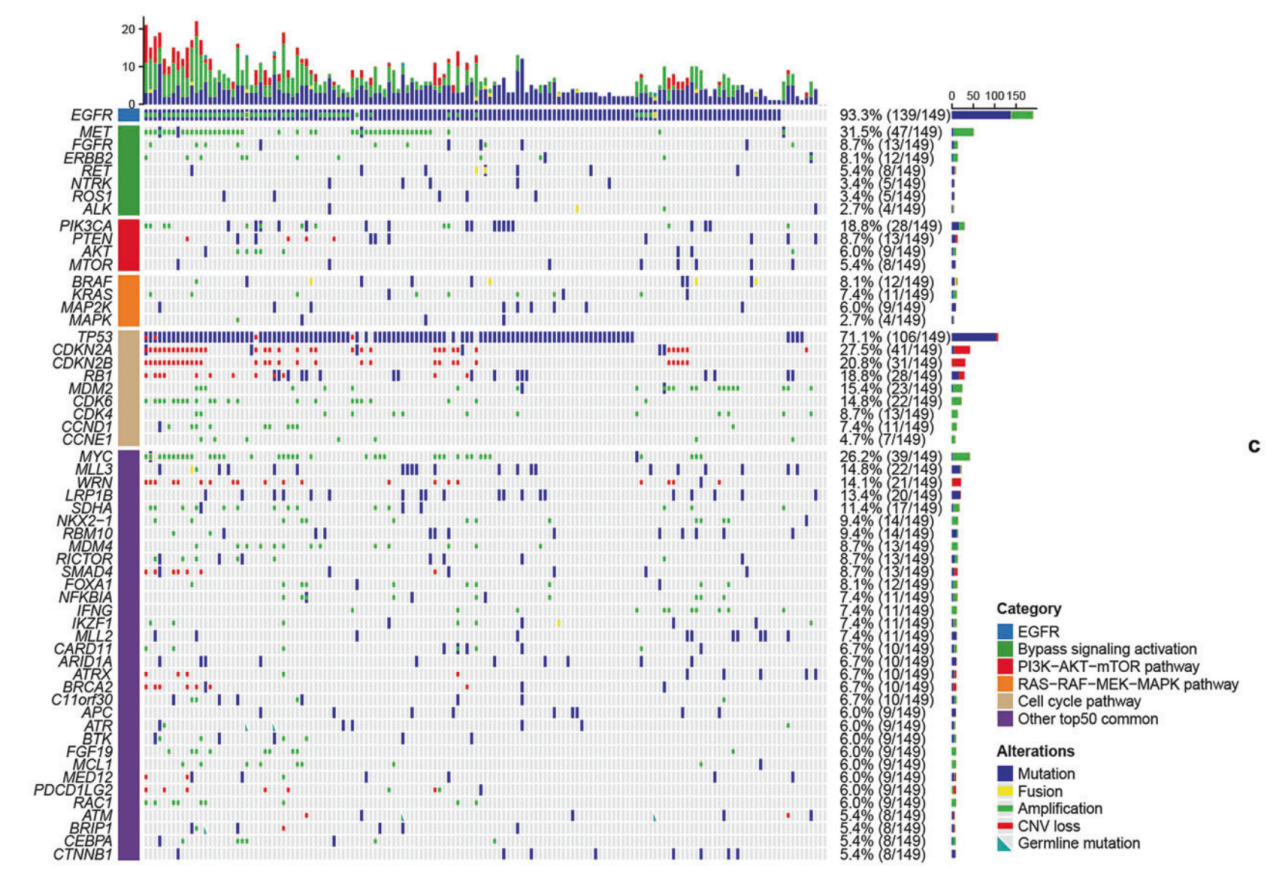
图.奥希替尼一线治疗失败时组织样本中的GPS
在组织标本中,EGFR通路相关变异常见驱动基因突变包括:EGFR Ex19del (40.9%, 61/149),EGFR L858R突变 (36.9%, 55/149),EGFR扩增(32.9%,49/149)、EGFR L718Q/V突变(4.7%,7/149)和EGFR C797S突变(3.4%,5/149)。旁路信号通路激活最主要的变异是MET扩增,发生率为30.9%(46/149),其他旁路变异则包括ERBB2扩增(7.4%,11/149))和FGFR扩增(5.4%,8/149))等。在下游通路失调中,TP53突变在组织中检出率高达69.8%(104/149),此外,CDKN2A/B拷贝数缺失(分别达24.2%,36/149和20.8%,31/149)、PIK3CA突变(11.4%(17/149))等亦被检出。可见,奥希替尼一线治疗失败背后存在多种变异,需根据特定基因组变异制定个体化治疗方案。在血液样本中,观察到与肿瘤组织样本类似的基因变异图谱。以组织NGS检测结果为参考,血浆ctDNA在各类基因变异检测中的一致性结果显示几乎所有基因变异在血浆中均表现出高度特异性(90.7%–100%),该结果进一步提示,组织样本仍是识别基因变异图谱的首选,当组织样本不可及时,血浆样本可作为识别基因变异图谱的有效补充手段。
破解三代EGFR-TKI进展
GPS研究首次揭示基因共突变图谱
为后续个体化诊疗提供重要参考
在组织样本中检测到MET扩增的46例患者中,有44例携带EGFR Ex19del/L858R突变;其中EGFR Ex19del突变占52.2%(24/46),EGFR L858R突变占45.7%(21/46)。在EGFR Ex19del突变患者中,合并其他多发EGFR改变的比例为37.5%(9/24);在EGFR L858R突变患者中,该比例为23.8%(5/21)。在EGFR Ex19del突变患者中,CDK4/CDK6扩增的比例为20.8%(5/24);在EGFR L858R突变患者中,该比例为14.3%(3/21)。该研究结果提示,不同EGFR突变亚型在共变异谱上存在差异,为后续治疗策略的个体化选择提供了有价值的参考,有助于进一步改善患者的临床结局。
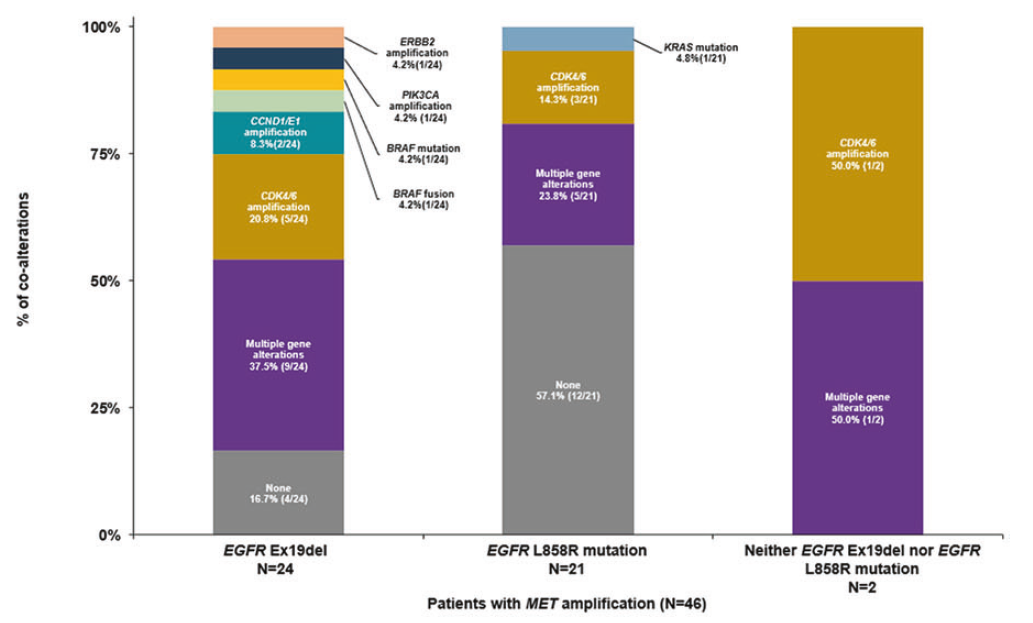
图.奥希替尼一线治疗失败时存在MET扩增患者的EGFR突变状态
破解三代EGFR-TKI进展
GPS研究为MET扩增检测提供新指导
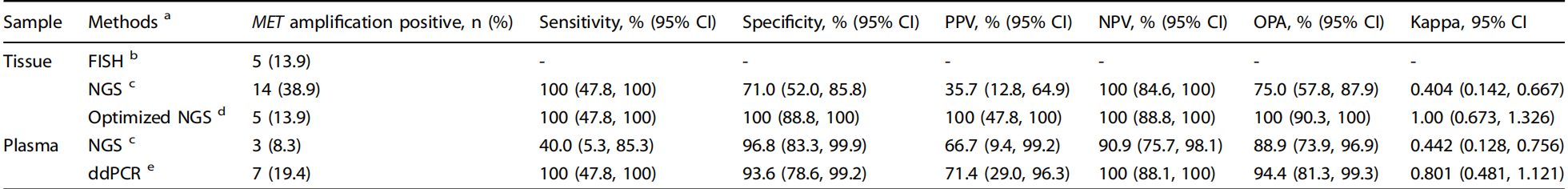
MET扩增是第三代EGFR-TKI进展最重要的机制之一,但既往研究多受限于样本量小及较高的假阴性率,导致不同检测方法的可靠性存在争议。因此,系统评价不同检测方法间的一致性,可能有助于寻找FISH检测的替代方案。GPS首次系统性评估不同MET扩增检测平台的一致性GPS研究在36例患者中同时进行了组织FISH、组织NGS、血浆NGS和血浆ddPCR检测,结果提示,与FISH (GCN≥10相比,优化的组织NGS(GCN≥8.63)敏感性为100%,表明优化的组织NGS有望成为一种可接受的检测方法,此外,血液ddPCR 敏感性为100%,提示对于无法获取组织标本的患者,血浆ddPCR可能成为可选的替代方案,均可用于筛选适合MET靶向治疗的人群。但在GPS研究中样本量较少,未来需要进一步在大型的前瞻性研究中加以验证。
表.奥希替尼一线治疗失败时存在MET扩增患者的比例及跨平台一致性
结语
GPS研究为全球EGFR敏感突变(Ex19del/L858R)晚期NSCLC在奥希替尼一线治疗进展后的精准诊疗提供了重要的循证医学证据,随着检测技术的标准化和靶向治疗策略的不断丰富,奥希替尼一线治疗进展后的治疗策略选择正走向精准,展望未来,基于个体化基因图谱的分型治疗将有望真正转化为生存获益。
专家简介
石远凯 教授
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
审批号:CN-175690
过期日期:2026-03-23
编辑:Eureka
审校:Ari
排版:Sylvia
执行:
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。


