
这种癌的“免疫+”新疗法,让患者保肛生存率飙升,谁懂啊!



局部晚期鳞状细胞肛门癌 (SCAC)的标准治疗方案为同步放化疗,但其复发率高达约40%,且存在治疗相关结肠造口术等严重毒副作用。PD-1抑制剂在初治的复发或转移性SCAC患者中已显示出疗效。这项研究旨在评估PD-1抑制剂ezabenlimab联合改良多西他赛
(SCAC)的标准治疗方案为同步放化疗,但其复发率高达约40%,且存在治疗相关结肠造口术等严重毒副作用。PD-1抑制剂在初治的复发或转移性SCAC患者中已显示出疗效。这项研究旨在评估PD-1抑制剂ezabenlimab联合改良多西他赛 、顺铂
、顺铂 及氟尿嘧啶
及氟尿嘧啶 (mDCF)方案在初治3期SCAC患者中的疗效与安全性。
(mDCF)方案在初治3期SCAC患者中的疗效与安全性。
研究方法

本项开放标签、单臂、II期临床试验在法国10家医疗中心开展。
纳入标准:
年龄≥18岁
经组织学证实为初治局部晚期3期SCAC患者
ECOG PS为0-1分血液学及终末器官功能充足
治疗流程:
诱导治疗:静脉注射mDCF方案(多西他赛40 mg/m²,第1天;顺铂40 mg/m²,第1天;氟尿嘧啶1200 mg/m²,第1-2天),每2周为
 1周期,共4周期;同时静脉注射ezabenlimab 240 mg,每3周为1周期,共3周期。
1周期,共4周期;同时静脉注射ezabenlimab 240 mg,每3周为1周期,共3周期。诱导治疗8周后评估疗效:
无疾病进展者:追加2周期mDCF化疗与1周期ezabenlimab治疗;
达到主要缓解(肿瘤缩小≥30%)、病理完全/近完全缓解(活检中存活细胞<10%)且实现生物学完全缓解(HPV ctDNA检测阴性)者:给予受累淋巴结照射(INRT),后续再进行7周期ezabenlimab维持治疗(240 mg 静脉注射,每3周为1周期);
未达到主要缓解者:接受标准同步放化疗。
主要终点:
40周时改良意向治疗(mITT)人群的临床完全缓解率(cCR)
次要终点:
诱导治疗后的病理完全/近完全缓解率
生物学完全缓解率
20周时生物学完全缓解率
客观缓解率(ORR)
8周疾病控制率(DCR)
总生存期(OS)
无进展生存期(PFS)
无病生存期(DFS)
安全性及健康相关生活质量(HRQOL)
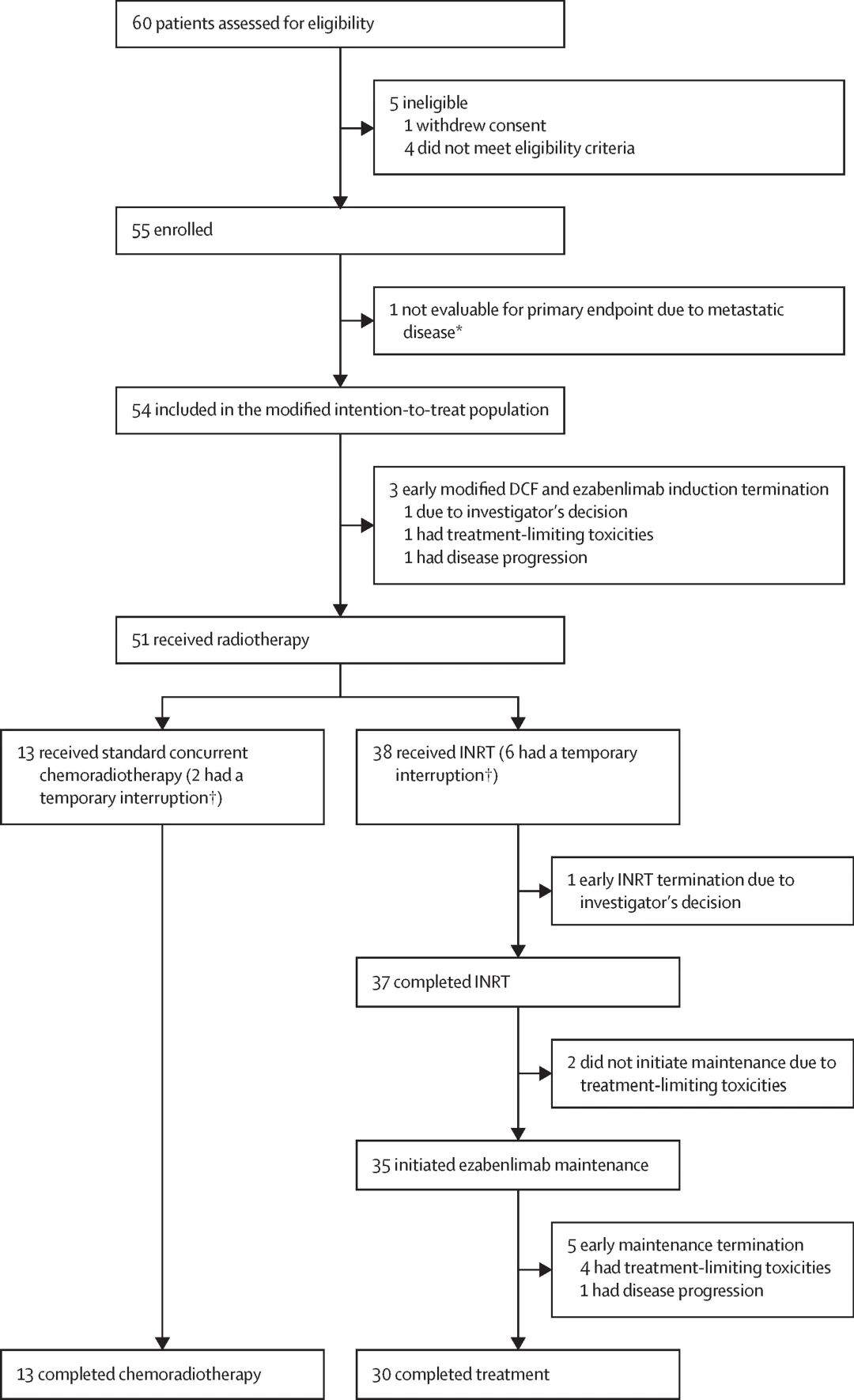
图 研究设计
研究结果

一、入组人群治疗情况
2022年1月4日至2023年11月20日,共入组55例SCAC患者,其中54例接受至少1周期治疗并纳入mITT人群。
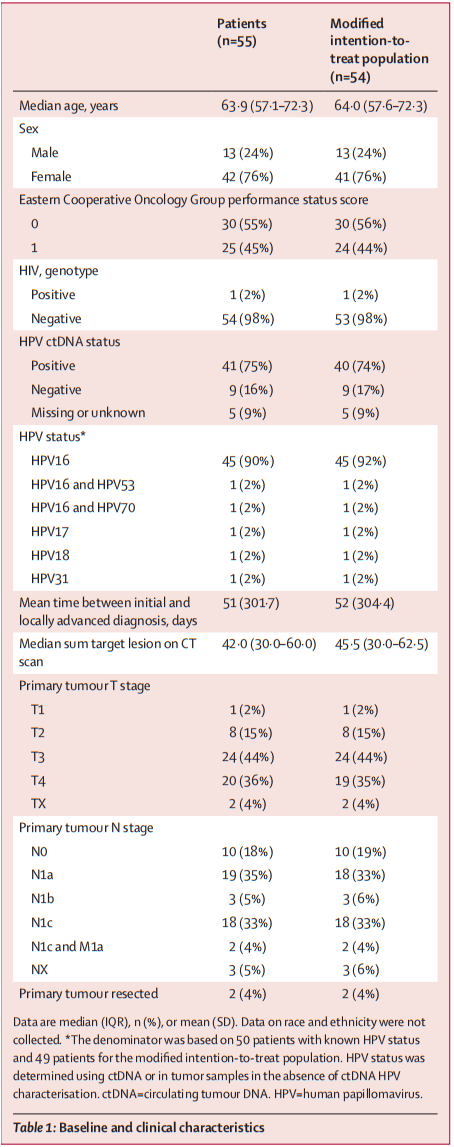
表 患者基线信息
98%(53/54)的患者完成4周期诱导治疗,96%(51/53)追加2周期诱导治疗;mDCF 方案各药物中位剂量强度均超98%。
38例患者接受 INRT,13例患者接受标准同步放化疗。84%(32/38)的INRT组患者、85%(11/13)的同步放化疗组患者完成计划放疗剂量。
二、主要终点目标达成
诱导治疗后,93%的患者达到客观缓解(25%完全缓解、68%部分缓解),84%的可评估患者实现病理完全/近完全缓解,基线ctDNA升高患者中90%达成生物学完全缓解。
40周时mITT 人群cCR达77.8%(90% CI:66.5-86.7),达到主要终点,其中INRT组86.8%、同步放化疗组69.2%。
仅6%(3/54)的患者接受挽救性结肠造口术,2例来自同步放化疗组且未达完全缓解。
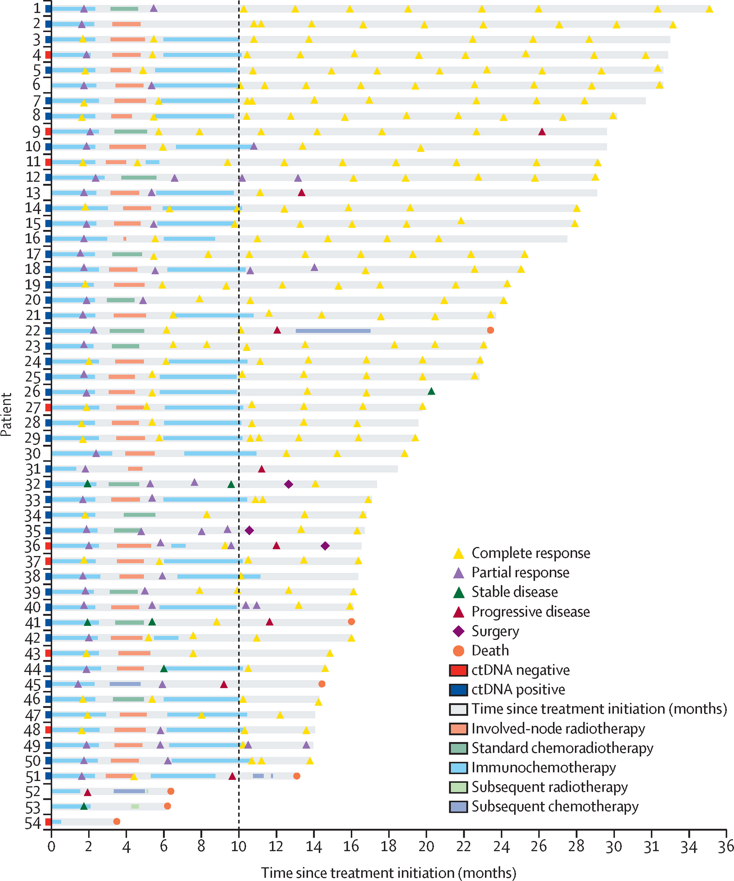
图 疗效分析
三、个体化治疗方案可行
中位随访23.0个月,mITT人群24个月PFS为81.4%、DFS为80.0%、OS为84.3%。
INRT组生存优势显著,24个月PFS(89.4% vs 76.9%)、DFS(89.3% vs 51.3%)、OS(97.4% vs 70.5%)均高于同步放化疗组。
复发率:INRT组11%(4/38),同步放化疗组31%(4/13),复发部位以远处转移和局部区域转移为主。
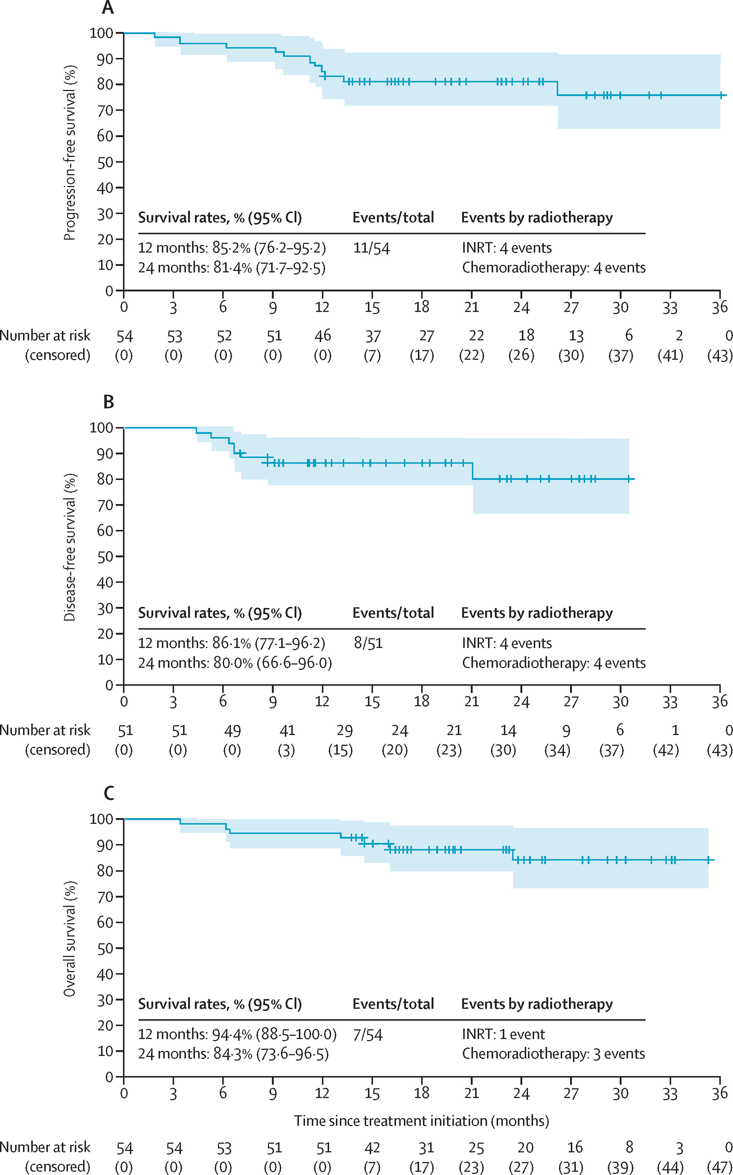
图 生存分析
四、安全性可控
诱导治疗期间100%患者出现不良事件(AE),98%为治疗相关不良事件(TRAE);36%发生严重不良事件(SAE),33%出现≥3级TRAE,5%因AE终止治疗。
各治疗阶段主要≥3级TRAE如下:
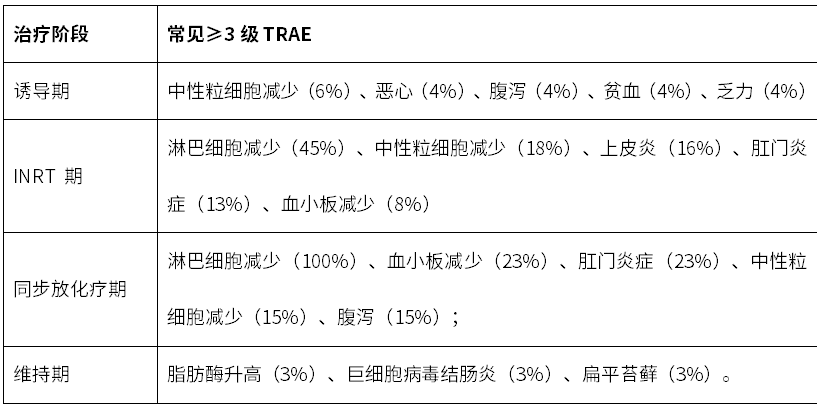
表 安全性分析
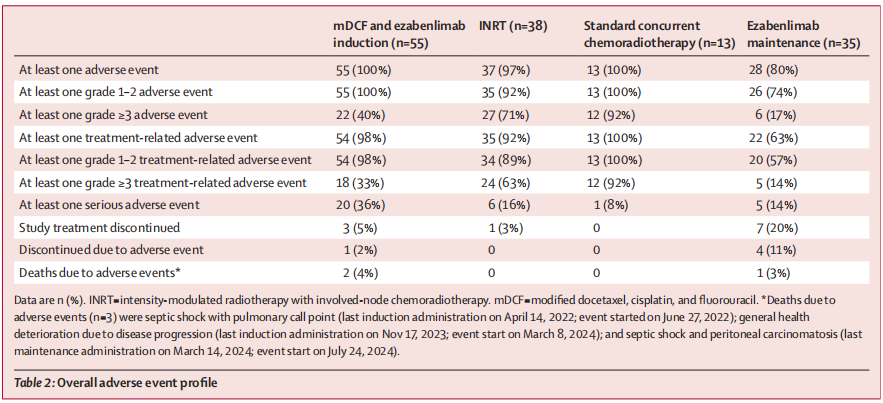
研究结论

本研究为ezabenlimab联合mDCF及INRT治疗3期SCAC提供了关键概念验证数据,支持进一步开展III期临床试验。后续免疫监测分析或可深入揭示该联合策略的免疫调节机制及协同作用,为局部晚期SCAC患者的治疗提供新的优化方向。
撰写:Aurora
审核:Aurora
排版:Aurora
执行:Aurora
 ,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
