
从下游效应靶向到上游调控,上皮源性预警素开启多通路协同新纪元

引 言
近二十年来,靶向免疫球蛋白E(IgE)及白细胞介素(IL)-4、IL-5等下游炎症介质的生物制剂在哮喘 治疗中取得了显著进展,可有效改善临床症状并降低急性发作风险。然而,这些因子主要作用于炎症反应的下游环节,对疾病的发生发展机制干预有限。随着气道上皮源性预警素(alarmins)在哮喘发病机制中的关键作用逐渐被揭示,胸腺基质淋巴细胞生成素(TSLP)、IL-25和IL-33等上游炎症信号分子的调控价值日益凸显,通过从炎症反应的上游靶点入手,实现多通路调控,有望突破当前以下游单一靶点为主的治疗局限性,为气道炎症性疾病的精准管理提供新的理论基础和方向。
治疗中取得了显著进展,可有效改善临床症状并降低急性发作风险。然而,这些因子主要作用于炎症反应的下游环节,对疾病的发生发展机制干预有限。随着气道上皮源性预警素(alarmins)在哮喘发病机制中的关键作用逐渐被揭示,胸腺基质淋巴细胞生成素(TSLP)、IL-25和IL-33等上游炎症信号分子的调控价值日益凸显,通过从炎症反应的上游靶点入手,实现多通路调控,有望突破当前以下游单一靶点为主的治疗局限性,为气道炎症性疾病的精准管理提供新的理论基础和方向。
一、气道炎症异质性强,多因子共激活突显「临床决策困境」
哮喘是一类高度异质性的疾病,其中重度哮喘患者表现出多种下游炎症因子同时升高的特征。国际重度哮喘登记研究(ISAR)的聚类分析表明,超过60%的患者存在两种及以上生物标志物(如IgE、嗜酸性粒细胞、FeNO等)同步升高,反映出炎症通路的复杂交织[1]。这种多通路并行激活的生物学特征,增加了疾病表型和炎症机制的复杂性。
从炎症反应的层级来看,现有生物制剂的作用集中在下游通路。例如,抗IL-5/5R生物制剂主要降低嗜酸性粒细胞水平,但对IgE介导的过敏反应或中性粒细胞炎症效果有限;抗IgE治疗虽能阻断过敏信号传导,却难以抑制嗜酸性粒细胞等炎症细胞的活化[2,3]。这种"单通路干预"模式,在面对多通路复杂炎症网络时,往往显得力不从心。
临床中常见到多种生物标志物升高的患者,即使经过生物制剂治疗,症状控制仍不理想。研究表明,约30%的重度哮喘患者对现有靶向治疗应答不佳,其机制可能与多条炎症通路同时激活或非2型炎症途径的参与有关[4]。因此,仅依赖下游靶点的干预难以覆盖复杂的炎症网络,亟需探索更上游的调控策略。
二、上皮源性预警素:多通路炎症网络的「上游总开关」
气道上皮作为呼吸道的第一道防线,在受到过敏原、病毒、污染物等刺激时,可迅速释放TSLP、IL-33和IL-25等上皮源性细胞因子。这些预警素作为免疫应答的"启动信号",处于炎症网络的顶端,被称为上游炎症"总开关"[5,6]。
➤TSLP:
在受到过敏原、感染和外界环境等刺激时,基底细胞产生的TSLP 可激活树突状细胞,诱导初始 T 细胞向 Th2 细胞分化,进一步释放 IL-4、IL-5、IL-13 等炎症因子。除 Th2 细胞介导的嗜酸性粒细胞炎症外,TSLP 可进一步激活 ILC2s,进一步释放 IL-5、IL-13 等炎症因子,介导嗜酸性粒细胞炎症, 从而推动2型炎症进程。此外,在非2型炎症环境中,TSLP还可通过调节树突状细胞的功能,促进Th17细胞的分化,参与中性粒细胞炎症和组织重塑。
➤IL-33:
主要由簇细胞等分泌,在急性暴露阶段可同步驱动1型(如中性粒细胞活化)和2型免疫反应。研究发现,小鼠在短期屋尘螨过敏原刺激下,肺部出现嗜酸性粒细胞增多、IL-4/IL-5/IL-13水平升高、杯状细胞化生及IgE抗体上升等典型2型特征[7]。
➤IL-25:
能够激活T2先天淋巴细胞产生IL-5和IL-13,促进2型炎症;IL-25还与哮喘相关的血管生成有关,其至少部分通过上调VEGF/VEGF受体表达来促进内皮细胞的增殖[7]。三种预警素协同形成正反馈环路,持续放大炎症信号[7,8,9](图1)。
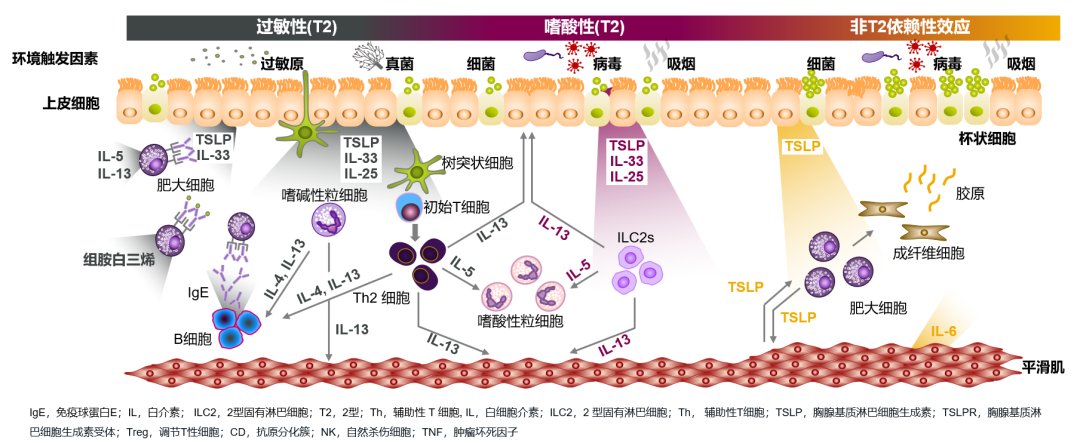
图1 预警素驱动的气道炎症多通路激活示意图[7,8]
三、治疗范式的根本转变:从下游抑制到源头调控
靶向TSLP、IL-33等上皮源性预警素的干预策略,其核心优势在于对炎症反应进行“源头管理”。该策略通过抑制这些位于免疫网络上游的“总开关”,能广泛影响包括Th2反应在内的多条炎症通路,突破了传统下游靶向药物的局限性。从作用位点看,这是在炎症反应的起始阶段进行干预,如同建立防火隔离带,能从源头上避免下游IL-4、IL-5、IL-13等多种效应因子的多重激活与放大,从而更有效地阻止炎症“山火”的蔓延,并有助于降低因单一通路被抑制而引发的免疫漂移(哮喘炎症类型转换)风险。
随着对预警素信号通路认识的不断深化,气道炎症性疾病的治疗正进入新的阶段。相较于仅阻断单一下游效应分子的治疗方式,上游干预能够在炎症反应早期同时影响多条下游通路,在多因子共激活、伴随多种生物标志物同步升高的复杂炎症表型患者中显示出更为突出的潜在优势,为突破当前治疗瓶颈提供了新的可能性。
结 语
重度哮喘作为哮喘谱系中疾病负担重、治疗难度高的亚型,其核心挑战在于炎症机制的高度异质性及多通路并行激活的复杂生物学特征。随着对气道上皮在炎症启动与放大过程中的关键作用逐步认识,以上皮源性预警素为代表的上游调控节点,为调控重度哮喘的复杂炎症网络提供了新的视角。通过作用于炎症反应的起点,上游干预策略有望同时抑制多条下游通路,为多生物标志物升高、反复加重或对既往生物制剂应答不佳的重度哮喘患者带来新的希望。
未来,随着对不同炎症通路主导模式的进一步厘清,以及临床分层和治疗策略的不断完善,上游调控理念有望推动重度哮喘治疗从“单通路阻断”向“炎症网络整体管理”转变,为实现更稳定、持久的疾病控制奠定基础。
审批编号:CN-176070
截止至:2026-12-30
本材料由阿斯利康提供,仅供卫生专业人士参考,不用于推广目的。

