
2025年末盘点丨破浪前行:从国际到本土,B细胞耗竭疗法深耕不辍,引领MS治疗迈向新征程
2025年渐近尾声,纵观多发性硬化(MS)治疗领域的发展,B细胞耗竭疗法始终处于焦点。2025年Immunity上一项研究再次强化了B细胞的核心作用:B细胞是MS的核心驱动因素,是复发缓解型MS(RRMS)复发的重要起始因素,也是治疗MS的关键靶点。
随着诊断标准更新、个体化治疗策略的发展,MS治疗正迈向精准诊治、早期高效的新阶段,其中靶向CD20的B细胞耗竭疗法如奥法妥木单抗等公布多项重磅研究数据,本文将重点聚焦B细胞耗竭疗法,从国际循证证据到中国临床实践,全面呈现MS发展的最新脉络与未来方向。
B细胞耗竭疗法的相关靶点主要有CD20、CD19、CD22、CD38和B细胞活化因子(BAFF),其中,全人源靶向CD20单克隆抗体,是为MS患者“量身定制”的B细胞疗法,具有广泛的应用1。抗CD20单抗通过抗体依赖性细胞毒性(ADCC)、补体依赖性细胞毒性(CDC)、抗体依赖性细胞吞噬作用(ADCP)以及直接诱导细胞凋亡,清除大部分致病B细胞2。其中,奥法妥木单抗在应用第4天中位B细胞数量降至2个细胞/µL,并持续维持≤1个细胞/µL直至第84天,凭借其快速、深度且持续的B细胞耗竭,为实现长期的临床疾病控制奠定了基础3。
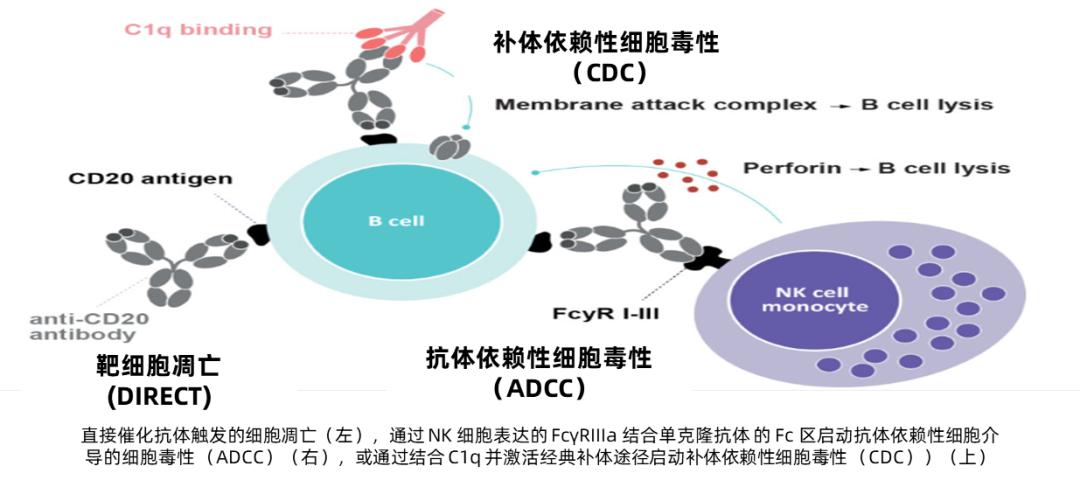
图1.抗CD20单抗的作用机制
早在2023年ECTRIMS大会中Stephen Hauser教授就表示,MS的治疗越早越好,早期高效策略是通往治愈之路的第一步。近一年来,以奥法妥木单抗为代表的抗CD20单抗多项重磅研究数据陆续更新,进一步从疗效、脑容量保护、安全性等核心获益角度,在临床实践中持续验证并强化其治疗优势。
第2年的NEDA-3达标是衡量长期预后最理想的指标,对于预测患者第7年实现最小化疾病进展(EDSS增加<0.5分)的正向预测值达到78.3%4。既往研究显示,奥法妥木单抗持续治疗2年NEDA-3达标率高达88%5,处于DMT治疗的领先水平。且3期关键研究数据的模拟治疗比较研究(STC)结果显示,相较于其他抗CD20单抗,奥法妥木单抗在降低年复发率(ARR)、减少磁共振成像(MRI)病灶、提高NEDA-3方面的疗效更优6。
ECTRIMS 2025最新公布的7年随访研究数据显示,随着奥法妥木单抗的持续应用,患者的NEDA-3达标率整体呈现上升趋势,随访第7年时,NEDA-3达标率高达95%(图2)7。
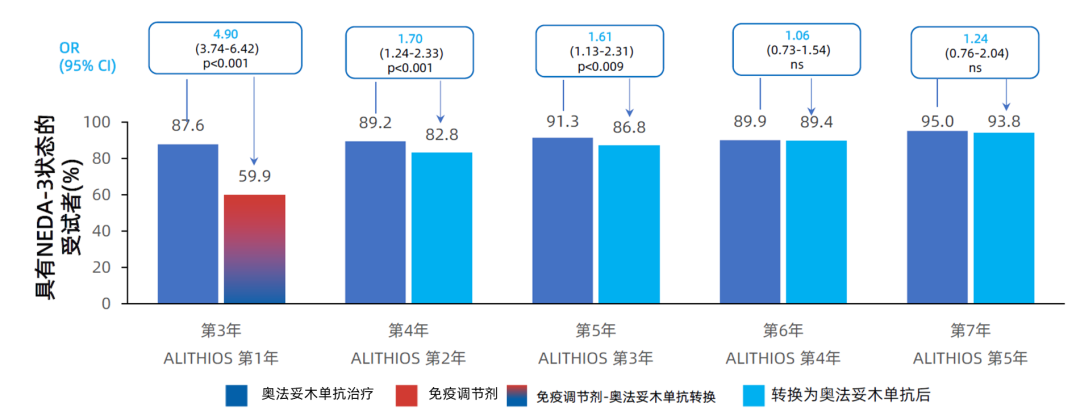
图2. 7年内的NEDA-3状态
在真实世界中,奥法妥木单抗的疗效也不断得到验证。2025年意大利一项真实世界研究评估了奥法妥木单抗对RRMS患者的有效性和安全性。研究结果显示,使用奥法妥木单抗治疗后随访24个月,患者的ARR从0.9显著下降至0.02(P<0.001),且EDSS评分均保持稳定。研究结果表明,使用奥法妥木单抗治疗可以快速控制疾病,延缓疾病进展8。2025德国真实世界研究评估了S1P受体调节剂转换为不同CD20单抗的疗效,其结果显示,转换为奥法妥木单抗较同类药物在临床复发、残疾进展、活动病灶表现更优9。
除此之外,ECTRIMS 2025大会也更新了多项奥法妥木单抗的真实世界研究数据,进一步验证了其在临床实际应用中的疗效:西班牙真实世界研究显示接受奥法妥木单抗治疗1年后,患者ARR显著下降至0.01,钆增强病灶数量由0.7降至0.0410。另有一项意大利真实世界研究显示,患者ARR由0.85显著降至0.03;末次随访时,96.31%的患者无复发,89.66%的患者无新发MRI活动11。
疗效之外,DMT药物的安全性也是MS重点关注的方面,尤其是严重感染等风险可能还会对患者的安全造成威胁,是长期管理时难以避免的挑战。
1)不良事件发生率低。ECTRIMS 2025的7年随访安全性数据显示,奥法妥木单抗治疗严重不良事件(SAE)发生率较低,且超90%的不良事件(AE)为轻度/中度12。来自意大利和欧洲的研究显示,相比其他治疗方案,使用奥法妥木单抗治疗MS发生上呼吸道/尿路感染、头痛及过敏、输液相关反应等常见不良事件发生率均更低13,14。
2)IgG水平保持稳定。奥法妥木单抗长期治疗结果显示,96.8%的患者平均IgG水平在长达7年的时间内保持稳定并高于正常范围下限(LLN:5.65g/L),IgM也仍高于其LLN(0.4g/L),且并未观察到IgG水平与严重感染风险之间存在的临床意义关联(图3)7。
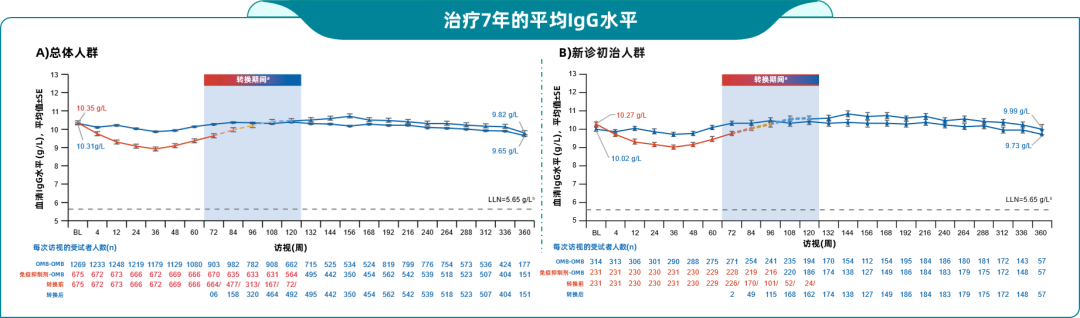
图3.治疗7年的平均IgM水平
3)输注相关反应发生率低。奥法妥木单抗通过皮下给药直接作用于MS致病核心场所——淋巴结内并清除其中的B细胞,还可减少严重输注相关反应15-17。欧洲自发研究报告调查显示,奥法妥木单抗输注相关反应发生率较低,仅为0.9%14。
脑萎缩对MS患者造成严重影响:脑萎缩预示MS残疾进展的风险增加23%、转化为继发进展型MS(SPMS)的风险增加16%,是早期RRMS患者认知能力下降的主要磁共振成像(MRI)预测因子18。
2025年柳叶刀子刊发布一篇关于DMT药物对于MS脑容量损失疗效的Meta分析,结果显示,与安慰剂相比,部分DMT如奥法妥木单抗等可显著减少MS患者的脑容量损失(均值比ROM 0.58;95%CI 0.40-0.83),奥法妥木单抗对脑容量损失的治疗优势显著,且在预防MRI病灶活动及降低残疾累积中也显著获益,其疗效处于DMT治疗选择的领先地位19。
无独有偶,ECTRIMS 2025公布的一项研究显示,相较于安慰剂组,使用奥法妥木单抗治疗1年(-0.32% vs. -2.40%,P<0.001)和2年(-0.53% vs. -3.16%;P<0.001)时均显著降低丘脑体积损失,对全脑、其他皮质下区域、脑干、脑室及小脑进行的同类分析显示,使用奥法妥木单抗治疗在所有观测脑区均产生显著疗效(图4)12。
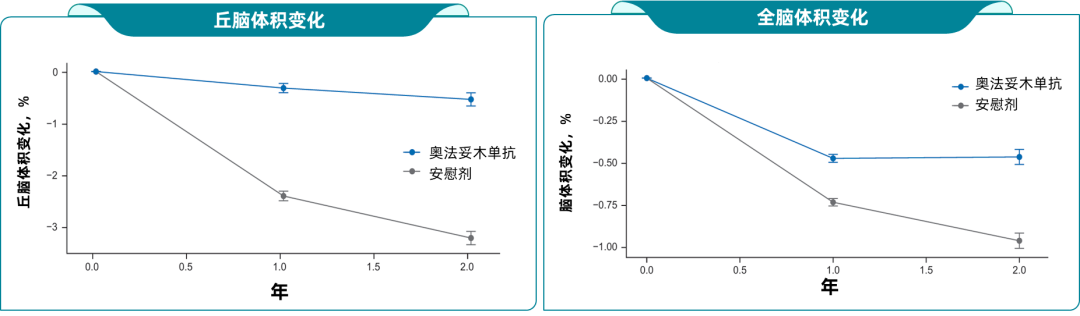
图4.奥法妥木单抗治疗2年较安慰剂持续显著减少丘脑、全脑等多个脑区的体积损失
中国人群MS的发病率为0.235/10万人年,近年来呈现逐渐增高的趋势20,当国际研究不断突破时,中国研究者们也同步带来了响亮的“中国之声”。
奥法妥木单抗是目前唯一*具有中国MS人群数据的高效B细胞耗竭疗法。华山医院团队开展的中国真实世界研究显示,RRMS患者奥法妥木单抗治疗一年NEDA-3达标率高达90%,治疗两年NEDA-3达标率83.7%,且研究随访期间所有应用奥法妥木单抗治疗的RRMS患者均未复发,ARR为021。2025年天津总医院团队进行的研究同样显示,奥法妥木单抗治疗期间患者的ARR为0,且EDSS评分保持稳定,认知评分得到显著改善(表1)22。
表1.患者临床结果

重庆医科大学附属第一医院团队牵头开展的一项真实世界研究,将97例患者分为奥法妥木单抗初始一线治疗组(n=38)和口服DMT转换治疗组(n=59)23。该研究显示:
初治组治疗12个月时,EDSS评分由2.50(2.00-4.00)降至2.00(1.00–3.00),得到显著改善(P<0.001);末次随访时,ARR从0.27±0.47降至0.05±0.23(P<0.001)。
口服DMT转换治疗组12个月时的EDSS评分由2.00(2.00-3.38)降至1.00(1.00-2.00),得到显著改善(P<0.001),ARR从0.45±0.54降至0.08±0.28(P=0.039);且未发现T1钆增强病变或新发/扩大的T2病变显著增加。
随访期间未报告严重不良事件(表2)。
表2.随访期间的临床及MRI特征
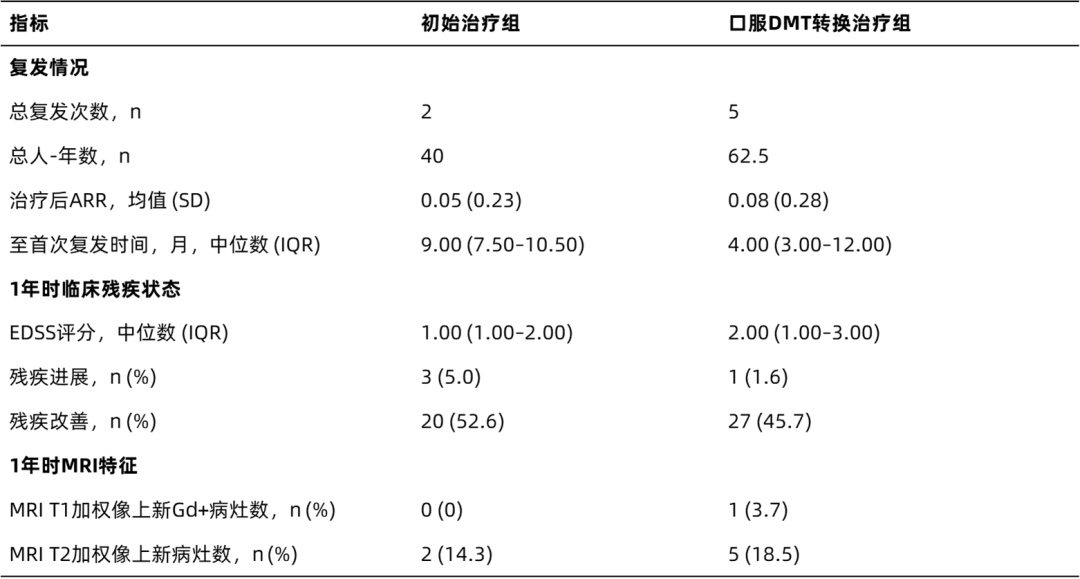
这项研究表明,不管初治患者或从口服DMT转换为奥法妥木单抗治疗,均可显著降低MS患者的疾病活动度与疾病进展风险,同时耐受性和安全性良好22。
MS治疗已经进入B细胞耗竭疗法的新时代,MS的创新治疗路径仍在持续拓展,在抗CD20单抗之外,靶向CD19的CAR-T细胞疗法等新兴策略也初露锋芒,但因潜在毒性如细胞因子释放综合征等,目前在MS的治疗中仍处于早期探索阶段。
作为B细胞耗竭疗法的高效DMT药物,抗CD20单抗奥法妥木单抗具有全人源单抗、小剂量等效、皮下给药三大创新优势。回顾奥法妥木单抗从国际证据到中国实践的系列成果,不仅推动了MS治疗领域的重要突破,更标志着该领域正迈向更精准、更具前瞻性的全新阶段。“MS可治愈”的临床目标正变得触手可及。未来,B细胞耗竭疗法有望为MS治疗带来更多突破,为患者带来更长远的临床获益。
*数据截止至2025年12月
参考文献
审批码KES0058355-120127,有效期为2025-12-16至2026-12-15,资料过期,视同作废

