
Cell Rep Med:肠道准备可促进肠道内病原体定植和易位并加重炎症
来源:IBD Daily
结肠镜检查 作为肠道疾病的常规检查手段之一,要求患者在检查前进行肠道准备,即喝下泻药冲洗肠道并清理肠道内容物。目前广泛认为,结肠镜检查前的肠道准备对人体无危害,但有研究发现,在肠道准备后的数日内肠道微生物群出现短暂改变。而对于包括克罗恩病
作为肠道疾病的常规检查手段之一,要求患者在检查前进行肠道准备,即喝下泻药冲洗肠道并清理肠道内容物。目前广泛认为,结肠镜检查前的肠道准备对人体无危害,但有研究发现,在肠道准备后的数日内肠道微生物群出现短暂改变。而对于包括克罗恩病 和溃疡性结肠炎
和溃疡性结肠炎 在内的炎症性肠病
在内的炎症性肠病 (IBD) 患者,其肠道内的条件致病菌可在特定情况下表现为病原体并加重肠道炎症。先前的一项研究报道,肠道准备可能在结肠镜检查后IBD的病情加重和感染风险增加的过程中起到重要作用。由于IBD患者因疾病监测而需要更为频繁地接受结肠镜检查,因此阐明肠道准备对条件致病菌的生长和炎症发展的影响意义重大。
(IBD) 患者,其肠道内的条件致病菌可在特定情况下表现为病原体并加重肠道炎症。先前的一项研究报道,肠道准备可能在结肠镜检查后IBD的病情加重和感染风险增加的过程中起到重要作用。由于IBD患者因疾病监测而需要更为频繁地接受结肠镜检查,因此阐明肠道准备对条件致病菌的生长和炎症发展的影响意义重大。
本研究旨在探讨结肠镜检查前的肠道准备对肠道微生物群与肠道微环境的作用,并阐明在IBD背景下肠道准备对疾病发展的影响。
研究通过短期的高剂量聚乙二醇 口服处理,模拟人类肠道准备过程。同时,研究以小鼠模型为核心,结合体外肠上皮细胞模型及人源粪菌定植模型,动态观察肠道准备后肠腔理化环境、黏液层结构与屏障功能的变化,并进一步通过鼠伤寒
口服处理,模拟人类肠道准备过程。同时,研究以小鼠模型为核心,结合体外肠上皮细胞模型及人源粪菌定植模型,动态观察肠道准备后肠腔理化环境、黏液层结构与屏障功能的变化,并进一步通过鼠伤寒 沙门菌感染模型和DSS诱导的结肠炎模型评估其对病原体定植、易位及炎症严重程度的影响。
沙门菌感染模型和DSS诱导的结肠炎模型评估其对病原体定植、易位及炎症严重程度的影响。
➤肠道准备可改变小鼠肠道内渗透压平衡、黏液层结构和短链脂肪酸水平
研究首先利用C57BL/6J小鼠构建肠道准备模型。与给予清水的对照组相比,聚乙二醇口服灌胃的肠道准备组小鼠盲肠渗透压显著升高 (438 mOsm/kg vs 724 mOsm/kg, p=0.00017),同时盲肠重量增加,小鼠排泄的水分增多。在组织病理层面,肠道准备组小鼠远端结肠的黏液层平均厚度和覆盖率降低,同时肠腔内容物和肠道菌群均减少。研究进一步探究肠黏膜组织的改变,结果显示,两组小鼠中均未观察到免疫细胞浸润,而肠道准备组小鼠盲肠黏膜厚度显著低于对照组,但结肠黏膜厚度无明显差异。在肠道微生物群层面,肠道准备组远端结肠和小肠中厌氧菌负荷降低,而盲肠中需氧菌负荷大幅升高。为检测微生物丰度的改变对其代谢产物的影响,研究测定了盲肠内容物中的短链脂肪酸水平,结果显示,肠道准备组小鼠短链脂肪酸水平显著低于对照组。此外,研究并未发现肠道准备可影响肠道通透性。总之,上述结果表明,肠道准备可影响肠道微环境,且对肠道微生物的代谢过程具有不利影响。
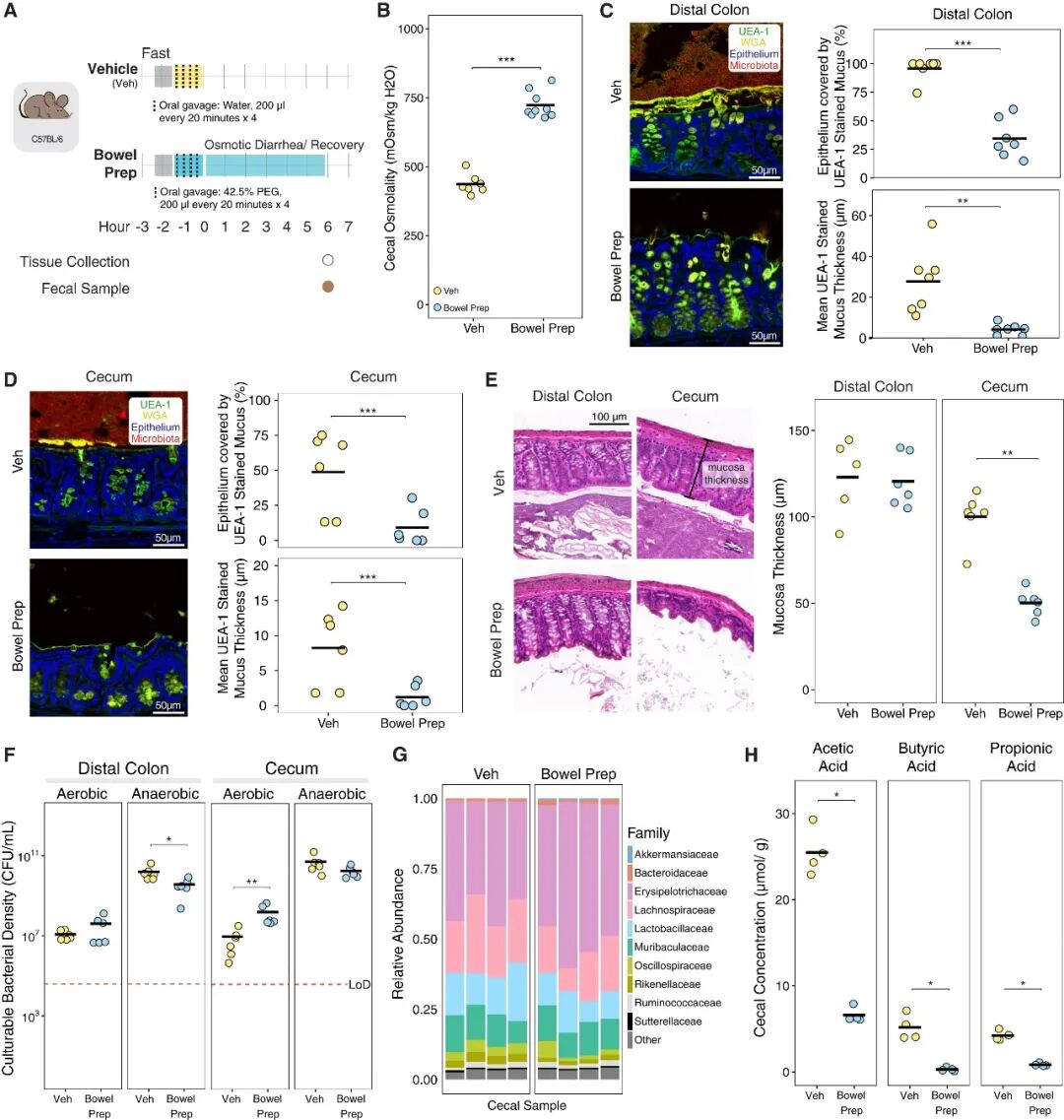
图1. 肠道准备可改变小鼠肠道内渗透压平衡、黏液层结构和短链脂肪酸水平。(A) 小鼠肠道准备模型构建示意图。(B) 肠道准备组与对照组小鼠的盲肠渗透压比较。(C-D) 肠道准备组与对照组小鼠的远端结肠 (C) 和盲肠 (D) 黏液层共聚焦显微图像、上皮表面黏液覆盖率和黏液层厚度。(E) 肠道准备组与对照组小鼠的远端结肠和盲肠H&E染色图像与黏膜厚度。(F) 肠道准备组与对照组小鼠的远端结肠和盲肠中需氧菌、厌氧菌负荷的比较。(G) 肠道准备组与对照组小鼠盲肠内容物的16S rRNA测序结果。(H) 肠道准备组与对照组小鼠盲肠中乙酸、丁酸、丙酸等三种短链脂肪酸水平的比较。
➤肠道准备促进鼠伤寒沙门菌的定植和易位并导致肠道的病理改变
由于前述实验表明肠道准备可降低肠道黏液层厚度和覆盖率并升高肠道渗透压,故研究人员假设肠道准备后小鼠肠道对病原体定植的抵抗能力降低,且耐受高渗环境的病原体,如鼠伤寒沙门菌,将获得竞争优势。在肠道准备后的盲肠渗透压下,研究发现鼠伤寒沙门菌的生长情况与正常肠道渗透压下无显著差异。以106 CFU的标准感染剂量对肠道准备组与对照组小鼠分别灌胃鼠伤寒沙门菌后,对照组小鼠粪便中未检测到鼠伤寒沙门菌,而肠道准备组中鼠伤寒沙门菌成功定植并增殖。感染后3天,肠道准备组小鼠的肠系膜淋巴结、脾脏和肝脏中均检测到鼠伤寒沙门菌的定植,而对照组中未检测到。在组织病理水平,肠道准备组的盲肠组织病理评分显著高于对照组,而远端结肠无显著差异,提示盲肠可能为感染的主要部位。此外,研究发现,鼠伤寒沙门菌在肠道准备后的实现定植所需的最低感染剂量为1000 CFU,且易位水平随感染剂量增加而显著上升。综上,肠道准备显著降低了鼠伤寒沙门菌在肠道内成功定植所需的最低剂量,并有利于其向肠外器官的易位。
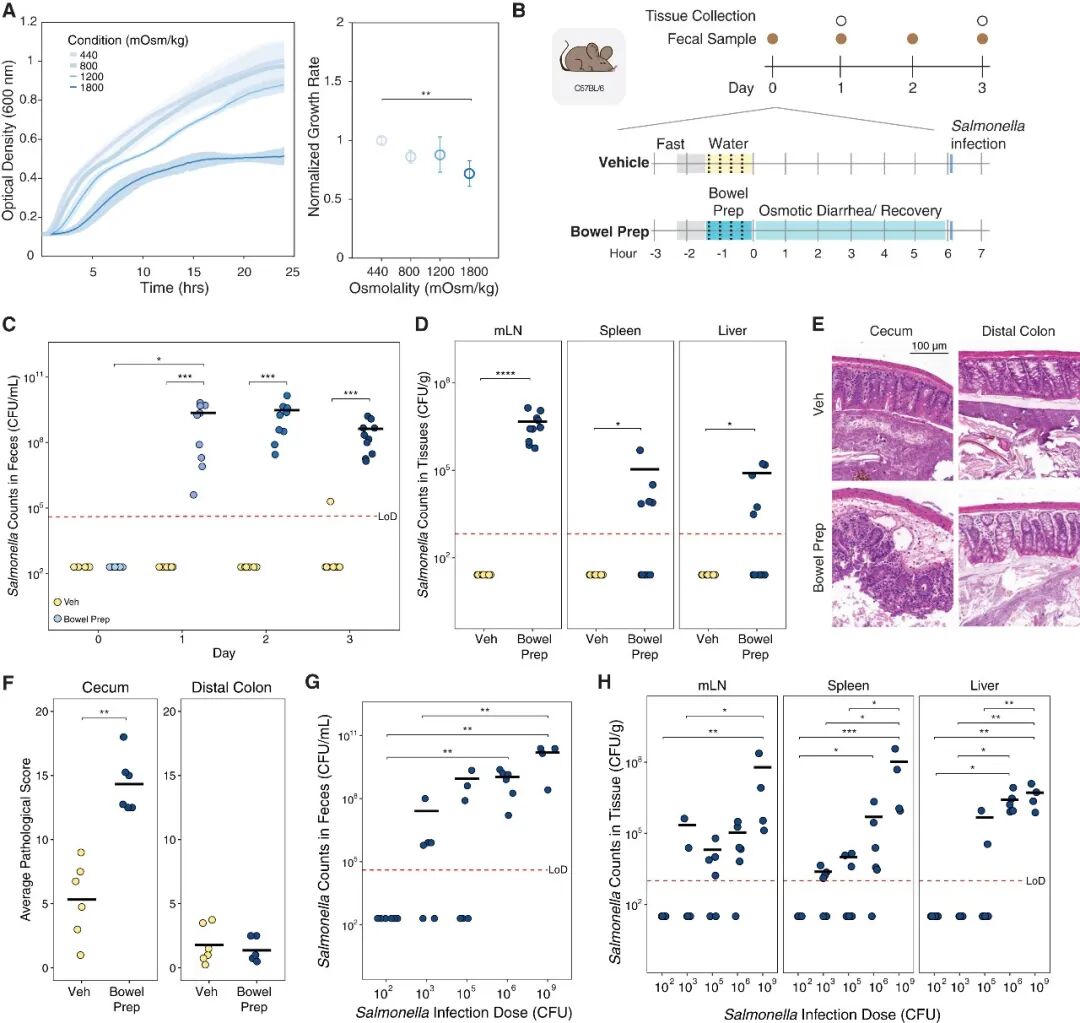
图2. 肠道准备促进鼠伤寒沙门菌的定植和易位并导致肠道的病理改变。(A) 鼠伤寒沙门菌在正常肠道渗透压和肠道准备后相对高渗条件下的生长速率比较。(B) 鼠伤寒沙门菌感染模型构建示意图。(C) 感染后肠道准备组与对照组小鼠粪便中鼠伤寒沙门菌数量的比较。(D) 感染3天后肠道准备组与对照组小鼠肠系膜淋巴结、脾脏和肝脏中鼠伤寒沙门菌数量的比较。(E-F) 感染后肠道准备组与对照组小鼠的远端结肠、盲肠的H&E染色图像 (E) 和组织病理评分比较 (F)。(G-H) 不同接种剂量下肠道准备组小鼠的粪便 (G) 和肠外器官 (H) 中鼠伤寒沙门菌数量的比较。
➤肠道对鼠伤寒沙门菌定植的抵抗能力在肠道准备后随时间逐渐恢复
为进一步阐明促进鼠伤寒沙门菌定植和易位的机制,研究系统表征了肠道准备后不同时间点的小鼠盲肠环境。其中,盲肠渗透压在肠道准备后24h即恢复至基线水平,黏液层覆盖率和厚度以及短链脂肪酸水平在48h后恢复至基线水平,而肠道微生物群的变化则在72h内逐渐恢复。因此,在肠道准备后的6h、24h和48h分别接种鼠伤寒沙门菌,结果显示,小鼠粪便中的鼠伤寒沙门菌数量随接种时间推移而降低,且肠外器官中呈现相似趋势。总之,肠道准备导致的相关改变在48h内逐渐恢复,其中肠道微生物群相关因素在抵抗病原体定植中发挥重要作用。
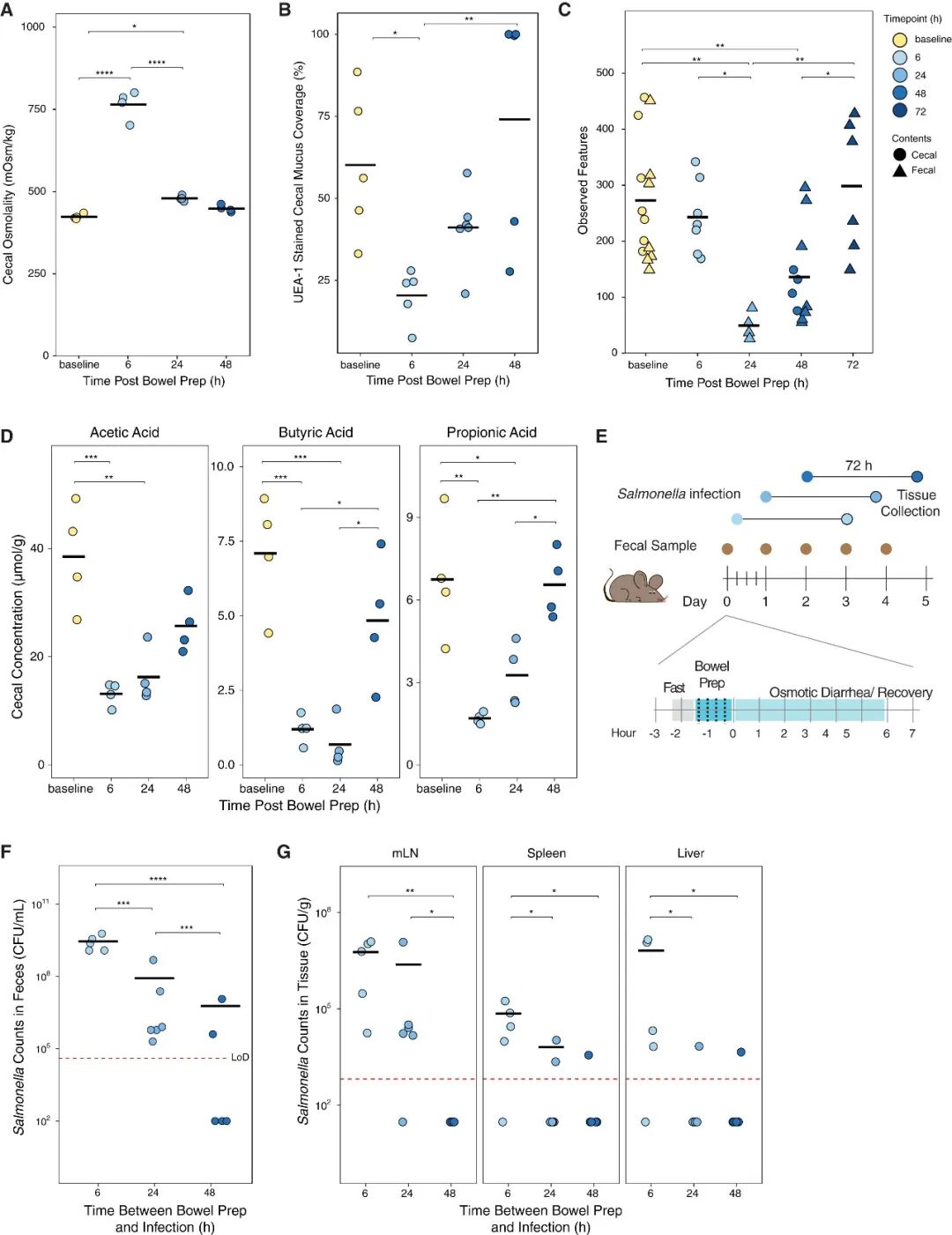
图3. 肠道对鼠伤寒沙门菌定植的抵抗能力在肠道准备后随时间逐渐恢复。(A-D) 肠道准备后不同时间点小鼠盲肠渗透压 (A)、盲肠上皮黏液覆盖率 (B)、盲肠及粪便微生物群的α多样性 (C) 以及盲肠中三种短链脂肪酸水平 (D)。(E) 不同时间点接种鼠伤寒沙门菌的肠道准备小鼠模型构建示意图。(F-G) 接种72h后肠道准备组小鼠的粪便 (F) 和肠外器官 (G) 中鼠伤寒沙门菌的数量。
➤鞭毛运动不影响肠道准备后鼠伤寒沙门菌的定植与易位
正常情况下,鞭毛的运动对鼠伤寒沙门菌等细菌性病原体穿透肠道黏液层并感染上皮细胞至关重要。而在肠道准备后,盲肠黏液层厚度和黏液覆盖范围均显著降低,故研究进一步探究鞭毛运动在肠道准备后鼠伤寒沙门菌定植中的作用。研究将野生型鼠伤寒沙门菌和运动性缺失的ΔflhD突变株分别感染小鼠,结果显示,感染ΔflhD突变株的肠道准备组小鼠中仍存在鼠伤寒沙门菌的定植,且粪便中的菌量与感染野生型菌株的肠道准备组小鼠无显著差异。并且,感染ΔflhD突变株的肠道准备组小鼠中同样可观察到鼠伤寒沙门菌易位至肠外器官。此外,感染ΔflhD突变株与感染野生型菌株的小鼠组织病理学评分无显著差异。因此,研究证明,肠道准备后鼠伤寒沙门菌的定植与易位不受鞭毛运动的影响。
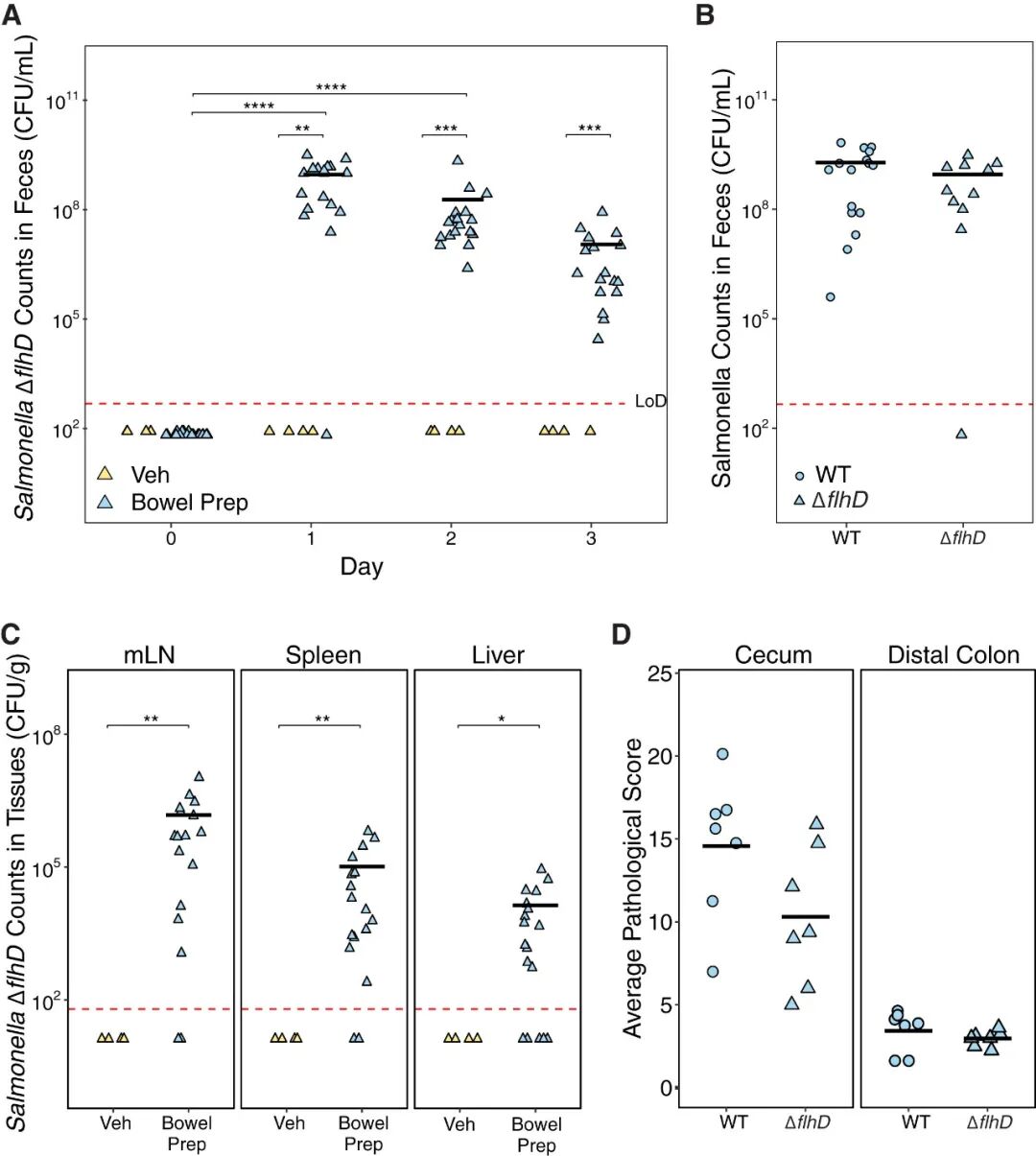
图4. 鞭毛运动不影响肠道准备后鼠伤寒沙门菌的定植与易位。(A) 感染ΔflhD突变株后肠道准备组与对照组小鼠粪便中鼠伤寒沙门菌数量变化。(B) 感染ΔflhD突变株与感染野生型菌株的肠道准备组小鼠粪便中鼠伤寒沙门菌数量比较。(C) 感染ΔflhD突变株后肠道准备组与对照组小鼠肠外器官中鼠伤寒沙门菌数量比较。(D) 感染ΔflhD突变株与感染野生型菌株的肠道准备组小鼠盲肠、远端结肠组织病理评分比较。
➤肠道准备可诱导盲肠组织中的小幅度一致性的转录反应
为探究肠道准备导致肠道对病原体易感性升高的机制,研究分析了小鼠盲肠组织在肠道准备前后的转录组特征。主成分分析显示,肠道准备组与基线组 (肠道准备前) 的基因表达谱无显著差异。在基因层面,两组间仅发现25个差异表达基因,而与黏液层形成、肠道屏障构建和免疫调节相关的关键基因在肠道准备前后表达量无显著变化。通路富集结果显示,正向富集通路主要为蛋白合成和免疫激活相关通路,而负向富集通路集中在细胞器分解过程。因此,尽管肠道准备后单个基因表达量的变化较小,但在通路层面,功能相关的基因表达量的改变一致。
➤聚乙二醇暴露促进体外模型中鼠伤寒沙门菌的侵袭
由于肠道准备对基因表达的影响较小,研究进一步探究了肠道准备是否能够直接改变肠上皮细胞对细菌侵袭的易感性。研究构建了人肠上皮细胞模型,使用聚乙二醇处理模拟肠道准备过程,并在不同渗透压培养条件下评估肠道准备后渗透压改变的影响。结果表明,与对照组相比,短期的聚乙二醇暴露显著提高了上皮细胞对鼠伤寒沙门菌侵袭的易感性。流失细胞术与均显示,聚乙二醇暴露后感染细胞的比例显著升高。此外,不同处理条件下,单个感染细胞内的细菌数量无显著差异,提示肠道准备主要促进细菌感染并进入细胞,而非增强其在胞内的增殖。总之,体外实验进一步证明,模拟肠道准备的聚乙二醇处理后,肠上皮对鼠伤寒沙门菌侵袭的易感性升高。
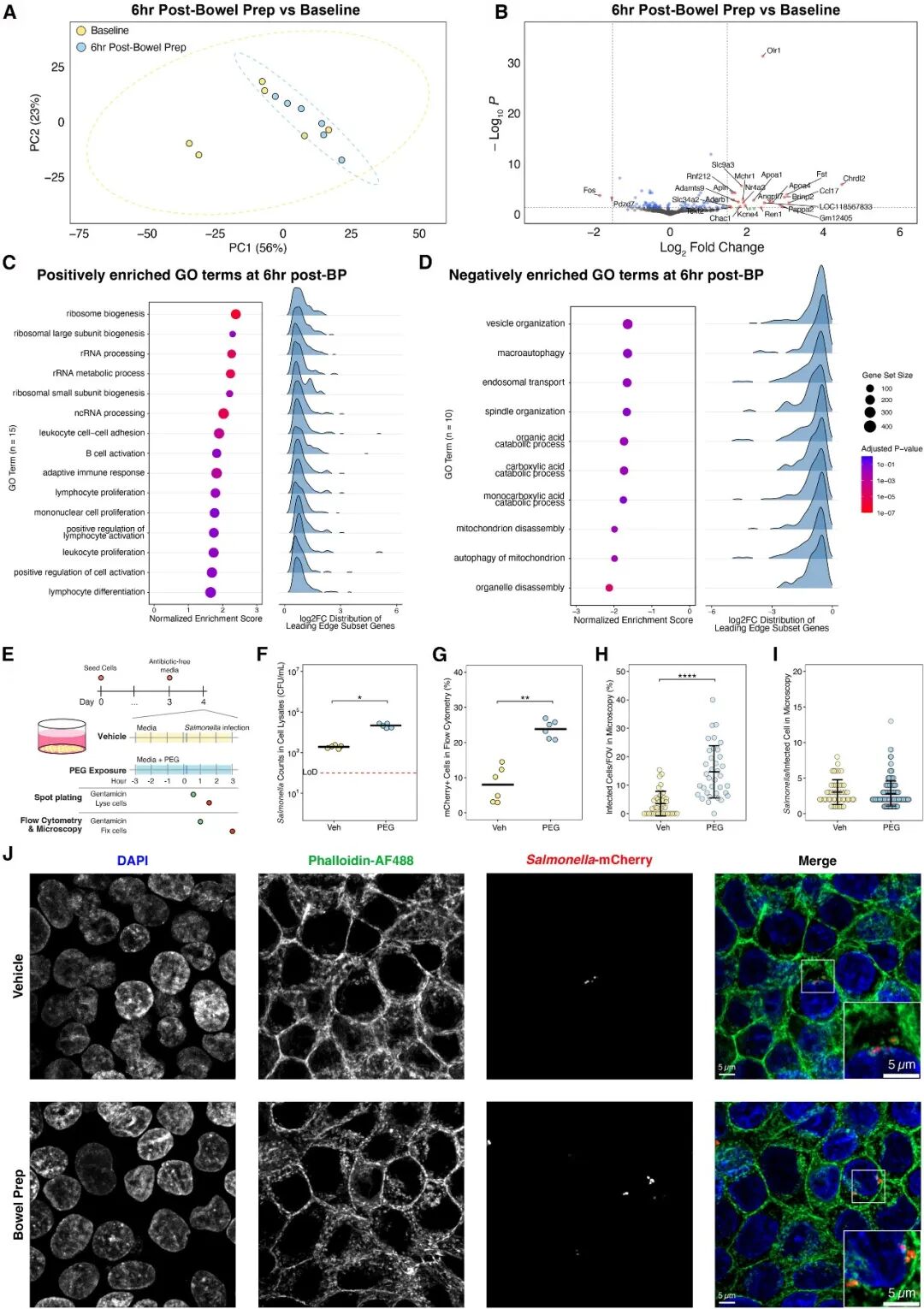
图5. 肠道准备在小鼠体内仅引起盲肠组织基因表达的小幅度变化,而体外聚乙二醇暴露可促进鼠伤寒沙门菌的侵袭。(A) 肠道准备前后小鼠盲肠基因表达的主成分分析图。(B) 肠道准备前后小鼠盲肠组织中的差异表达基因。(C-D) 肠道准备前后小鼠盲肠差异表达基因富集分析结果。(E) 体外聚乙二醇暴露模型构建示意图。(F) 感染后聚乙二醇暴露组与对照组细胞裂解液中鼠伤寒沙门菌数量。(G) 流式细胞术检测聚乙二醇暴露组与对照组感染细胞的比例。(H-J) 共聚焦显微成像下聚乙二醇暴露组与对照组的感染细胞比例 (H)、数量 (I) 和代表性图像 (J)。
➤肠道准备可加重结肠炎并增强IBD相关致病共生菌的易位
先前研究表明,在肠道准备所导致的高渗透压水平下,严格厌氧菌的生长显著受到抑制,而肠杆菌科耐高渗能力最强。由于前述结果显示鼠伤寒沙门菌耐高渗能力强且在肠道准备后可定植并易位,因此研究进一步探究肠杆菌等其他IBD相关致病共生菌在肠道准备后能否获得相似的定植和易位优势。研究首先将肠杆菌科的多种IBD相关致病共生菌培养于高渗环境,结果表明其可在高渗环境中存活并增殖。同时,研究发现,持续的高渗条件下,溃疡性结肠炎患者肠道微生物群组成改变,其中肠杆菌科相对丰度显著升高。此外,在人源IBD微生物群定植的急性结肠炎小鼠模型中,肠道准备显著加重炎症程度,并促进肠道细菌向肠系膜淋巴结和肝脏的易位,且易位菌群以IBD相关致病共生菌为主。
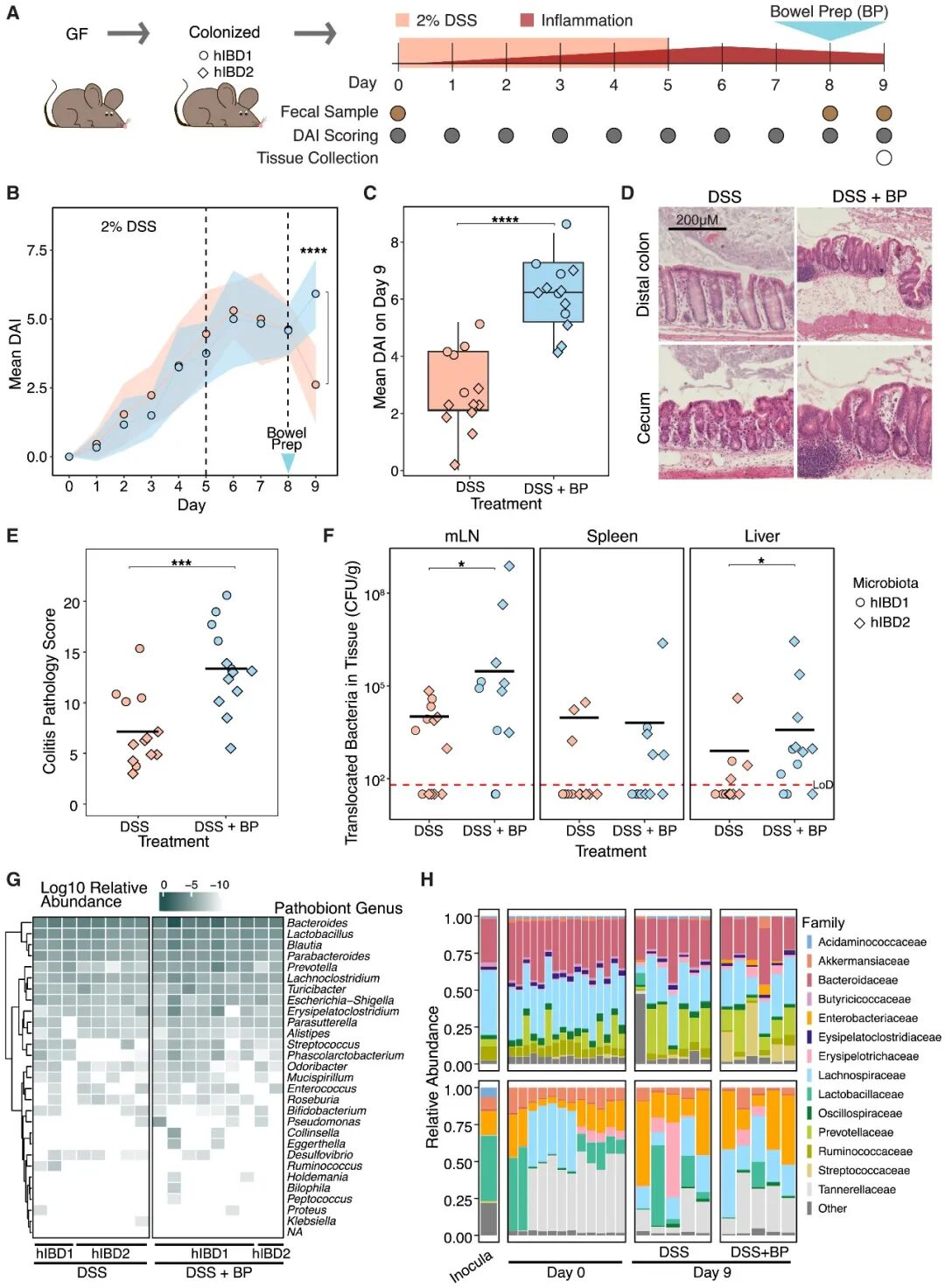
图6. 肠道准备可加重结肠炎并增强IBD相关致病共生菌的易位。(A) 人源IBD微生物群定植的急性结肠炎小鼠模型构建示意图。(B) 微生物定植组与对照组小鼠结肠炎疾病活动指数每日变化。(C-F) 微生物定植组与对照组小鼠第9日疾病活动指数 (C)、远端结肠和盲肠H&E染色图像 (D)、远端结肠的组织病理评分 (E) 以及肠外器官中肠道微生物数量 (F)。(G) 易位至肠系膜淋巴结的肠道微生物群16S rRNA测序结果。(H) 定植不同来源肠道微生物群的小鼠在DSS处理前后以及肠道准备前后粪便微生物群16S rRNA测序结果。
综上所述,本研究通过小鼠模型和细胞模型共同发现,肠道准备可在短时间内改变肠道微环境,增加肠道对鼠伤寒沙门菌的易感性,并加重结肠炎症。此外,肠道准备还可促进肠道细菌由肠腔向临近淋巴结、肝脏和脾脏等肠外器官的易位。尽管本研究提示肠道准备可能存在目前尚未充分认知的临床影响,但需强调的是,本研究的结果并不意味着肠道准备的普遍风险,而是提示未来的科学研究需进一步关注高风险人群中肠道准备的潜在影响。
致谢
中南大学湘雅医学院 郭洋
西湖大学附属杭州市第一人民医院 傅甜
中南大学湘雅三医院 陈杰
中南大学湘雅三医院 王晓艳
对本篇文章解读做出的贡献


