
B-HOT自动化分子诊断系统为肾移植排斥诊断提供客观量化新工具
一、瓶颈:传统组织学诊断陷主观之困,精准医疗呼唤客观新依据
长期以来,Banff 组织学评分体系广泛用于肾移植 排斥诊断,但在实际应用中存在明显局限:1.主观性与变异性突出。诊断高度依赖病理医师的显微镜观察和判读,不同医师甚至同一医师在不同时间对同一活检样本的结论可能存在显著差异;2.难以反映疾病动态变化进程。排斥反应是连续的生物学过程,而组织学评分将其划分为有限等级,细微的病情变化易被忽略;3.早期与轻微病变敏感度不足。对轻度或非典型病变的识别能力有限,易发生漏诊或延迟诊断;4.操作复杂且专业门槛高。随着Banff标准的持续更新,体系日趋复杂,准确应用不仅需要病理医师具备高度专业知识和丰富经验,且操作流程繁琐、耗时较长。总体而言,Banff组织学诊断在主观性强、敏感性有限、操作复杂、耗时长等方面存在多重挑战1,已难以满足精准医疗的临床需求。
排斥诊断,但在实际应用中存在明显局限:1.主观性与变异性突出。诊断高度依赖病理医师的显微镜观察和判读,不同医师甚至同一医师在不同时间对同一活检样本的结论可能存在显著差异;2.难以反映疾病动态变化进程。排斥反应是连续的生物学过程,而组织学评分将其划分为有限等级,细微的病情变化易被忽略;3.早期与轻微病变敏感度不足。对轻度或非典型病变的识别能力有限,易发生漏诊或延迟诊断;4.操作复杂且专业门槛高。随着Banff标准的持续更新,体系日趋复杂,准确应用不仅需要病理医师具备高度专业知识和丰富经验,且操作流程繁琐、耗时较长。总体而言,Banff组织学诊断在主观性强、敏感性有限、操作复杂、耗时长等方面存在多重挑战1,已难以满足精准医疗的临床需求。
二、破局:从分子诊断的探索到破局——聚焦B-HOT面板的革新与验证
为克服单纯依赖组织形态学的诊断局限,学界开始聚焦分子诊断。目前主流分子诊断类别包括:活检组织转录组/基因表达诊断(MMDx、Banff人类器官移植(B-HOT)基因面板 )1,2;外周血基因表达检测(kSORT、AlloMap-Kidney等)3,4;供体来源游离 DNA(dd-cfDNA)5;尿液/尿外泌体 mRNA检测6。然而,因外周血基因表达的验证稳定性欠佳,dd-cfDNA特异性不足,尿液/尿外泌体 mRNA标准化难度大,在明确排斥类型时,活检组织转录组/基因表达仍是当前最优选择7-9。
MMDx利用移植物活检样本,结合基因芯片技术与机器学习算法,将复杂的转录组特征转换成“分子诊断结果”2,10。当组织诊断处于“灰色地带”时,MMDx可提供补充信息,助力优化诊断方案与治疗决策11。但其成本高,可及性不足,难以实现大规模临床推广11。因而,开发一种准确率高、成本可控、通用性强的分子诊断工具,成为当前移植医学领域的重要课题。
近日,Zielinski D等在《美国移植杂志》(Am J Transplant)发表了一项重要的研究成果——《基于Banff人类器官移植基因面板的肾移植物排斥分子诊断:一项多中心国际研究》的重要研究成果1。该项研究的核心突破在于,成功地将Banff工作组在2019年制定的B-HOT基因面板转化为一个低成本、高通量、可自动生成报告的临床实用诊断工具,为解决肾移植排斥诊断的核心痛点提供了创新性解决方案。此突破性进展的基石在于一项严谨的多中心大样本研究设计。该研究共纳入950例肾移植活检样本,覆盖欧洲、北美10个移植中心。样本被划分为开发队列(n=664,法国)和两个外部验证队列(n=286),其中开发队列进一步拆分为训练集(n=537)和测试集(n=127),外部验证队列包括美国中心(n=243)和加拿大中心(n=43)的样本。所有样本均为福尔马林固定石蜡包埋(FFPE)组织样本,为研究结果的可靠性奠定了坚实基础。
三、核心:严谨模型构建与验证,实现临床一键转化
该研究采用多中心国际队列设计,系统性地开发并验证了基于B-HOT基因面板的肾移植排斥分子诊断模型。研究通过NanoString nCounter平台对B-HOT面板中的770个基因进行表达谱检测,并实施了严格的质控和基于内参基因的标准化处理。
在模型构建阶段,研究团队运用LASSO回归结合重复k折交叉验证方法,从758个内源性基因中筛选出52个抗体介导排斥(AMR)相关基因和15个T细胞介导排斥(TCMR)相关基因;并基于这些基因训练了四种不同的机器学习基础模型(包括标准逻辑回归、正则化逻辑回归、线性判别分析及线性支持向量机),且通过重复k折交叉验证对各模型参数进行优化,显著提升了模型的稳健性。最终通过集成学习策略,构建了AMR和TCMR的连续概率预测模型。
模型性能经过多维度严格验证,包括内部测试集验证、两个外部多中心队列验证(美国、加拿大)验证,以及针对组织学与分子诊断结果不一致的活检样本,结合临床数据与组织学信息的复核。验证指标涵盖精确率-召回率曲线下面积(PR-AUC)、受试者工作特征曲线下面积(ROC-AUC)、对数损失(Log loss)和 Brier 分数(0为完全准确,1为完全错误),全面保障了模型的诊断效能。
此外,研究还开发了全自动诊断报告系统(HistoMx),为临床提供可重复、标准化的分子诊断工具。
四、验证:模型性能卓越,精准破解组织学诊断“灰色地带”
该模型在内部测试集与外部验证队列中均表现优异。如表1所示,对于AMR的诊断,其PR-AUC在三个独立验证队列中分别达到0.811、0.891和0.832;针对TCMR的诊断,PR-AUC也高达0.736、0.810和0.782。这些数据充分表明,该模型不仅准确率高,而且具备极强的泛化能力,能够适配不同地区、不同中心的患者群体。
表1. 排斥模型在内部与外部验证队列中的性能表现
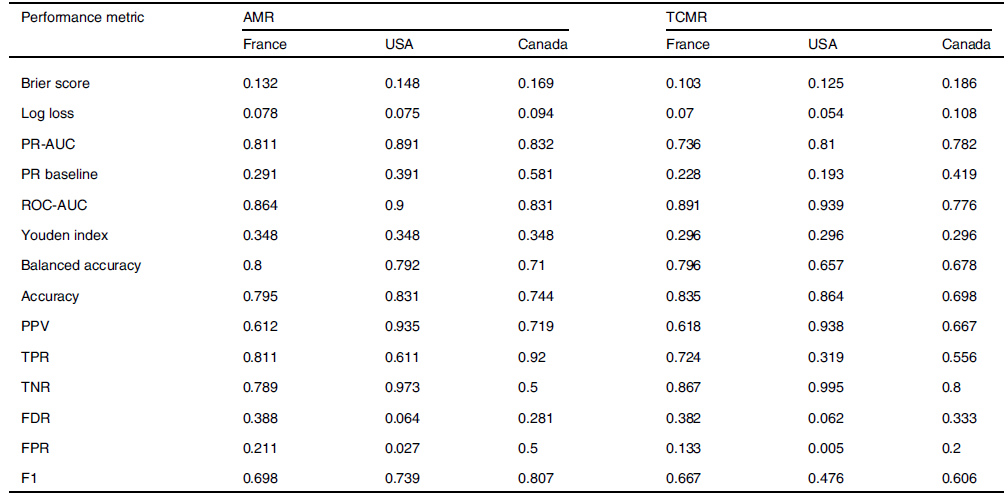
该研究一项极具临床价值的发现是,当设定50%为诊断阈值时,约30%的活检样本出现了分子诊断结果与初始组织学诊断不一致的情况。进一步分析表明,这些“差异案例”恰恰是临床诊断中棘手的“灰色地带”,例如:组织学病变程度未达当前Banff诊断阈值的早期排斥、由BK病毒肾病 等非排斥因素引起的炎症对组织学判读的干扰、以及缺乏C4d或供体特异性抗体(DSA)等典型证据的AMR病例(图1)。这些发现有力证实,分子诊断与组织学诊断分别揭示了移植物病理状态的不同维度。在组织学诊断面临困境时,分子诊断可提供关键补充信息,有效减少漏诊和误诊风险。
等非排斥因素引起的炎症对组织学判读的干扰、以及缺乏C4d或供体特异性抗体(DSA)等典型证据的AMR病例(图1)。这些发现有力证实,分子诊断与组织学诊断分别揭示了移植物病理状态的不同维度。在组织学诊断面临困境时,分子诊断可提供关键补充信息,有效减少漏诊和误诊风险。
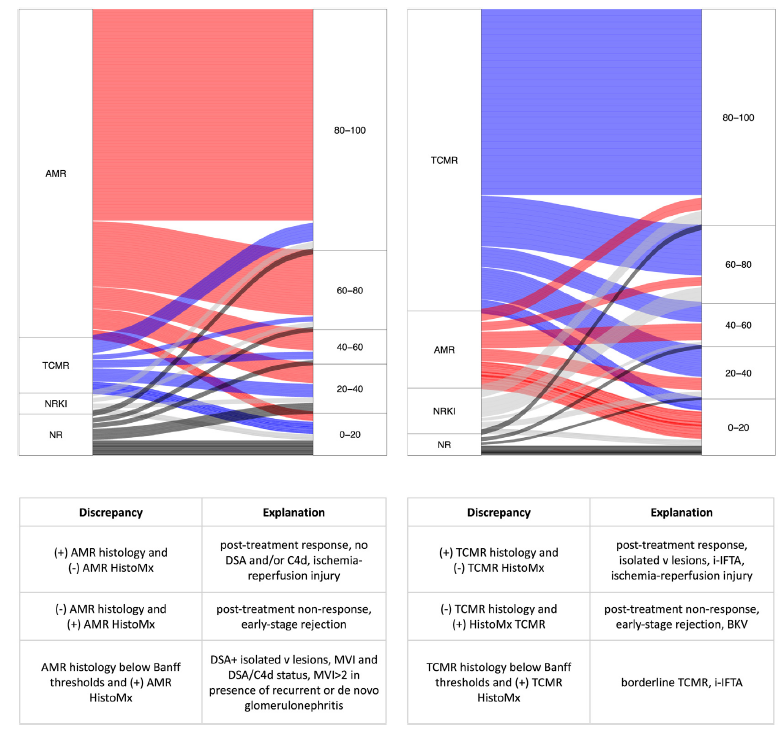
图1. 桑基图展示所有验证队列(n=413)中组织学的诊断与基因表达的预测概率的关系(左图对应AMR与右图对应TCMR)。附表详细描述了二者不一致情况及相关解释。
五、应用:HistoMx系统实现数据到报告自动转化,量化诊断把握度
本研究的核心亮点之一,是成功研发全自动诊断报告系统——HistoMx。该系统能够直接基于原始基因计数数据,一键生成包含概率评分、质控参数及可视化结果的标准化报告。如图2所示,报告不仅能给出“排斥”或“无排斥”的定性判断,更核心的是提供连续的排斥概率评分,并附有置信区间。
这种输出形式为临床医生提供了更丰富的决策依据,使其可精准评估诊断把握度,尤其适于临界病例的处理。例如:1例移植后12个月的指征性活检,组织学诊断为TCMR,但基因表达谱分析显示AMR或TCMR证据不足;1例指征性活检,组织学诊断为慢性活动性AMR(C4d和供体特异性抗体均为阴性),基因表达谱分析显示AMR概率极高,为临床确诊提供了有力支持。
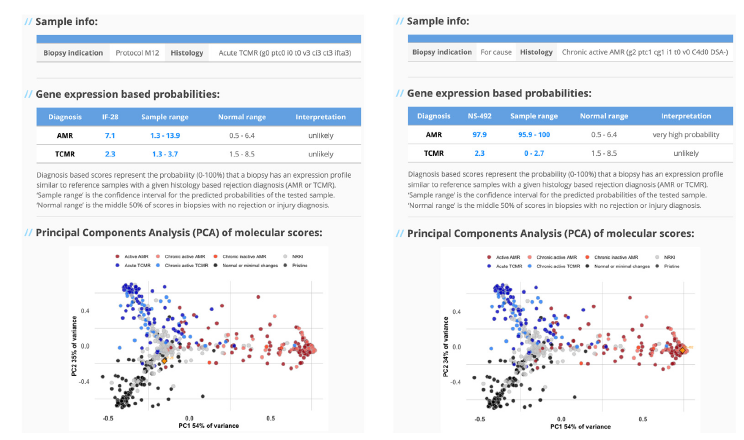
图2. HistoMx自动化分子报告示例。左图:样本信息为指征性活检 M12,指征为临床需要,组织学诊断为急性 TCMR(g0 ptc0 10 t0 v3 ci3 ct3 ifta3);基因表达概率显示 AMR 概率 7.1(正常范围 0.5-6.4)、TCMR 概率 2.3(正常范围 0-2.7),均判定为 “可能性低”。右图:样本编号 IF-28,组织学诊断为慢性活动性 AMR(g2 ptc1 cg1 i1 t0 v0 C4d0 DSA-);基因表达概率显示 AMR 概率 97.9(95% 置信区间 95.9-100),判定为 “极高概率”,TCMR 概率 23(正常范围 1.5-85),判定为 “可能性低”。注:评分基于活检样本基因表达谱与已知组织学排斥诊断参考样本的相似性概率(0-100%);“样本范围” 为测试样本预测概率的置信区间;“正常范围” 为无排斥或损伤诊断活检样本评分的中间 50%;下方为分子评分的主成分分析(PCA)结果,PC1 解释 54% 的方差。)
该项研究的新颖之处在于,并非简单堆砌临床数据,而是实现了临床医学、生物信息学与数据科学的深度融合,使整体研究框架更具立体性、深入和精准性。研究立足于肾移植排斥诊断的实际痛点,并非盲目追求“高精尖”新技术,而是聚焦于解决临床实际问题的“可用性”和“可及性”解决方案。通过选用经Banff 工作组共识筛选的B-HOT基因面板,研究确保了其起点的科学性与临床相关性;研究团队未止步于常规统计分析,而是引入LASSO回归、多种机器学习算法及集成学习等先进技术,从数据中挖掘出最具有预测价值的信号,从而构建出高精度诊断模型。
该研究成功创建了一套标准化、自动化且经济高效的分子诊断系统。其核心目的并非取代传统组织学诊断,而是作为后者强有力的补充与验证工具,尤其在那些组织学诊断不明确或存在争议的“灰色地带”病例中,可供客观、定量的诊断依据。
当前,移植领域的研究者多以临床医生和基础科学家为主,而这项研究成功地将数学算法和生物信息学分析的前沿力量注入其中。这种跨学科的“组合拳”正是其能够实现突破性进展的关键所在。该研究为如何利用计算力量解决复杂临床问题提供了范例,也为精准医疗在器官移植领域的落地树立了新标杆。
点评专家

刘磊 教授
➤医学博士,郑州大学第一附属医院肾移植科
➤主任医师,教授,科室副主任
➤中华医学会器官移植分会病理学组委员
➤中国医疗保健国际交流促进会病理学组委员
➤河南省医学会器官移植学分会委员
➤河南省医师协会器官移植分会委员
➤《中华器官移植》杂志通讯编委
➤参编著作9部,发表SCI 8篇,核心期刊十余篇
➤主持河南省省级课题1项,参与国自然面上项目2项
解读专家

成富民 医生
➤住院医师,医学硕士
➤2019年本科毕业于郑州大学临床医学专业
➤2022年硕士毕业于郑州大学泌尿外科(肾移植)专业
➤毕业后从事肾移植临床及病理相关工作至今
➤发表SCI论文、中华核心期刊论文数篇
参考文献:
1.Zielinski D, Goutaudier V, Sablik M, et al. Molecular diagnosis of kidney allograft rejection based on the Banff Human Organ Transplant gene panel: A multicenter international study. Am J Transplant. 2025 Aug;25(8):1631-1642.
2.Halloran PF, Madill-Thomsen KS, Reeve J. The Molecular Phenotype of Kidney Transplants: Insights From the MMDx Project. Transplantation. 2024 Jan 1;108(1):45-71.
3.Roedder S, Sigdel T, Salomonis N, et al. PLoS Med. 2014 Nov 11;11(11):e1001759. doi: 10.1371/journal.pmed.1001759IF: 9.9 Q1 . Erratum in: PLoS Med. 2015 Feb 20;12(2):e1001790.
4.Cheung R, Xu H, Jin X, et al. Validation of a gene expression signature to measure immune quiescence in kidney transplant recipients in the CLIA setting. Biomark Med. 2022 Jun;16(8):647-661.
5.Benning L, Morath C, Fink A, et al. Donor-Derived Cell-Free DNA (dd-cfDNA) in Kidney Transplant Recipients With Indication Biopsy-Results of a Prospective Single-Center Trial. Transpl Int. 2023 Nov 3;36:11899.
6.Suthanthiran M, Schwartz JE, Ding R, et al Urinary-cell mRNA profile and acute cellular rejection in kidney allografts. N Engl J Med. 2013 Jul 4;369(1):20-31.
7.Van Loon E, Giral M, Anglicheau D, et al. Diagnostic performance of kSORT, a blood-based mRNA assay for noninvasive detection of rejection after kidney transplantation: A retrospective multicenter cohort study. Am J Transplant. 2021 Feb;21(2):740-750.
8.Goussous N, Xie W, Dawany N, et al. Donor-derived Cell-free DNA in Infections in Kidney Transplant Recipients: Case Series. Transplant Direct. 2020 Jun 11;6(7):e568.
9.Gaudio C, D'Arpino E, Stefani S, et al. Urinary Exosomes in Nephrology: A New Frontier for Diagnosis and Prognosis of Kidney Diseases. Int J Mol Sci. 2025 Sep 5;26(17):8679.
10.Madill-Thomsen KS, Halloran PF. Precision diagnostics in transplanted organs using microarray-assessed gene expression: concepts and technical methods of the Molecular Microscope® Diagnostic System (MMDx). Clin Sci (Lond). 2024 Jun 5;138(11):663-685.
11.Beliančinová M, Kleinová P, Blichová T, et al. Molecular Microscope Diagnostic System in Patients after Kidney Transplantation-First Experience. Biomedicines. 2024 Feb 29;12(3):548.
免责声明:该信息仅作医学和科研参考,赛诺菲不建议以任何与您所在国家所批准的处方信息不符的方式使用本产品,本材料仅供医疗卫生专业人士使用。
审批编码:MAT-CN-2518685-V1.0-2025.12
