
EBMT 2026中国之声丨袁海龙教授:贝舒地尔治疗皮肤cGVHD疗效优异,二线治疗ORR达83.3%!
编者按:慢性移植物抗宿主病 (cGVHD)是异基因造血干细胞移植(allo-HSCT)后常见且严重的并发症,其中皮肤是最常累及的器官,其表现多样且显著影响患者生活质量[1-2]。传统糖皮质激素
(cGVHD)是异基因造血干细胞移植(allo-HSCT)后常见且严重的并发症,其中皮肤是最常累及的器官,其表现多样且显著影响患者生活质量[1-2]。传统糖皮质激素 治疗虽为一线方案,但仍存在耐药、反应不足及不良事件风险。2026年欧洲血液与骨髓移植协会(EBMT)年会上,新疆医科大学第一附属医院袁海龙
治疗虽为一线方案,但仍存在耐药、反应不足及不良事件风险。2026年欧洲血液与骨髓移植协会(EBMT)年会上,新疆医科大学第一附属医院袁海龙 教授团队关于“贝舒地尔在皮肤cGVHD患者中的疗效与安全性”的研究成功入选大会交流,为优化二线治疗进一步提供了中国证据。《肿瘤瞭望-血液时讯》特邀袁海龙教授结合皮肤cGVHD的诊疗现状,深入解读该研究结果及其临床启示,并分享团队在cGVHD管理及研究方面的未来部署。
教授团队关于“贝舒地尔在皮肤cGVHD患者中的疗效与安全性”的研究成功入选大会交流,为优化二线治疗进一步提供了中国证据。《肿瘤瞭望-血液时讯》特邀袁海龙教授结合皮肤cGVHD的诊疗现状,深入解读该研究结果及其临床启示,并分享团队在cGVHD管理及研究方面的未来部署。

《肿瘤瞭望-血液时讯》:皮肤是cGVHD最常累及的器官,其表现复杂且严重影响生活质量。能否请您分享一下当前皮肤cGVHD的诊疗现状。基于此,您认为当前诊疗模式中存在的挑战或未被满足的临床需求有哪些?
袁海龙教授:皮肤作为人体面积最大且处于最前线的免疫器官,是allo-HSCT后cGVHD最常累及的靶器官之一[1]。皮肤cGVHD的发生率高达80%,多在病程早期出现,对cGVHD的诊断具有重要价值[2]。此外,皮肤cGVHD与生活质量下降、症状负担加重以及非复发性死亡风险增加均独立相关[3-6]。尽管皮肤表现对于cGVHD的诊断和预后都至关重要,但其临床表现具有高度异质性,导致难以准确评估[7]。
美国国立卫生研究院(NIH)2014年cGVHD共识标准[8]建议,通过皮肤活检辅助进行皮肤cGVHD的诊断。然而,在临床实践中,由于患者依从性、操作风险以及资源限制等多重因素,皮肤活检并未被广泛开展。绝大多数病例的诊断仍主要依据明确的移植病史、典型的临床皮肤表现,并充分排除其他可能原因。皮肤cGVHD的主要表现包括苔藓样改变、色素减退或沉着,以及皮肤硬化。严重的硬化特征表现为皮肤增厚、紧绷且脆弱,常伴创伤愈合不良、淋巴引流功能不足,并可能因轻微外伤引发皮肤溃疡,从而显著影响患者的生活质量。
表1. 皮肤cGVHD的症状和体征[8]

皮肤cGVHD的治疗主要包括局部治疗和全身治疗,其中糖皮质激素仍为一线标准治疗方案[9]。然而,临床上仍面临激素反应不足、耐药及不良反应等问题,亟需探索更加安全、有效的二线治疗策略。
《肿瘤瞭望-血液时讯》:您团队开展的贝舒地尔治疗皮肤cGVHD中国回顾性研究(B068)在本届 EBMT 上亮相。能否请您简要介绍一下核心研究结果?基于以上结果,贝舒地尔将为皮肤cGVHD患者带来哪些获益?
袁海龙教授:非常荣幸,我们团队的研究入选2026年EBMT年会壁报交流。皮肤cGVHD的多样性表现与ROCK2信号通路的异常活化密切相关。贝舒地尔作为选择性ROCK2抑制剂,可同时靶向驱动cGVHD的炎症与纤维化过程,从而逆转组织损伤[10-11]。其于2023年8月在我国获批用于治疗对糖皮质激素或其他系统治疗应答不充分的≥12岁cGVHD患者,为cGVHD治疗带来全新选择[12]。ROCKstar研究显示,贝舒地尔皮肤特异性总体缓解率(ORR)为37%,在中国II期研究中为40%[13-14]。本研究基于我们中心的使用数据,进一步评估了其在皮肤cGVHD患者中的疗效和安全性[15]。
共纳入21例患者,中位年龄35岁(范围14-63岁)。皮肤cGVHD表现为非硬化型19例,硬化型2例。发生率>10%的皮肤表现包括丘疹斑疹/苔藓样皮疹 14例(67%)、瘙痒11例(52%)、红斑10例(48%)及色素沉着5例(24%)。基线时,轻度、中度和
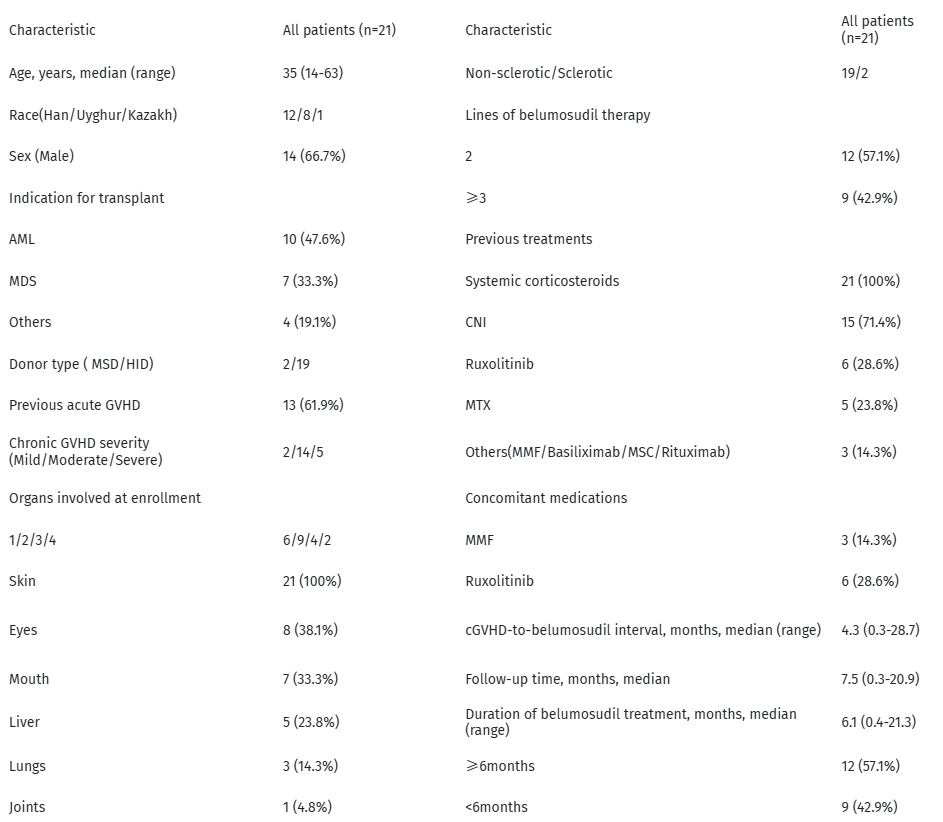
14例(67%)、瘙痒11例(52%)、红斑10例(48%)及色素沉着5例(24%)。基线时,轻度、中度和 重度cGVHD分别为2例(9.5%)、14例(66.7%)和5例(23.8%)。治疗方案包括二线治疗12例(57.1%)及三线或以上治疗9例(42.9%)。中位治疗持续时间为6.1个月(范围0.4-21.3),其中12例治疗超过6个月(表2)。
重度cGVHD分别为2例(9.5%)、14例(66.7%)和5例(23.8%)。治疗方案包括二线治疗12例(57.1%)及三线或以上治疗9例(42.9%)。中位治疗持续时间为6.1个月(范围0.4-21.3),其中12例治疗超过6个月(表2)。
表2. 患者特征[15]
结果显示,贝舒地尔治疗后皮肤特异性ORR为81%,即21例患者中有17例出现治疗反应。其中,完全缓解(CR)为42.9%(9例),部分缓解(PR)为38.1%(8例)。仅皮肤受累患者,ORR为83.3%;皮肤及其他多器官受累患者,ORR为73.3%。总体来看,糖皮质激素耐药且累及皮肤及其他器官的患者使用贝舒地尔治疗后显示出优异的疗效,并伴随患者生活质量的显著改善。
尤为值得关注的是,贝舒地尔二线治疗组ORR为83.3%(10/12),三线或以上治疗组ORR为66.7%(6/9),提示其作为二线治疗的疗效优于后线治疗。尽管样本量相对有限,但本研究结果提示,对于皮肤 cGVHD,在常规激素一线治疗效果不佳时,应尽早启用贝舒地尔进行治疗,有望为患者争取到更优的治疗效果。
此外,研究还观察到在治疗过程中糖皮质激素及钙调磷酸酶抑制剂(CNI)的减量非常常见,且多在贝舒地尔治疗2周后进行。且所有患者生存且无复发,未出现新的治疗相关不良事件或严重不良事件。鉴于免疫抑制剂和激素减量是cGVHD管理的核心目标之一,这一结果为实现临床目标和优化管理提供了有力支持。
综上,贝舒地尔在皮肤cGVHD患者中显示出良好疗效和安全性,为既往糖皮质激素及其他治疗不佳患者提供了更优选择,有利于充分实现临床目标。二线使用时的优越反应提示早期干预可能带来更大获益。
《肿瘤瞭望-血液时讯》:展望未来,为实现 cGVHD 的管理优化和患者生活质量的实质性提高,您的团队还将在cGVHD领域开展哪些研究和探索?
袁海龙教授:本次EBMT会议中,我们团队展示了ROCK2抑制剂在皮肤cGVHD治疗中的显著临床疗效,这对团队而言具有重要鼓舞意义。未来,我们将在以下几个方向持续推进cGVHD的临床管理与研究工作:
(1)加强系统性随访机制建设:针对allo-HSCT后cGVHD患者,建立完善的长期随访体系。目前已配备专职研究生及临床工作人员,对每位患者实施标准化、系统化的随访。同时,通过微信群、公众号等数字化平台维持与患者的密切联系,确保及时评估病情变化、治疗响应及生活质量。
(2)扩展ROCK2抑制剂在其他受累器官的临床研究:临床实践发现,贝舒地尔除对皮肤cGVHD具有显著获益之外,对口腔及眼部cGVHD表现亦有疗效。未来计划针对口腔和眼部慢性排斥反应开展专项临床研究,进一步验证其在这些部位的有效性和安全性。
(3)推进生物标志物研究:目前cGVHD仍缺乏经临床充分验证的可靠生物标志物,用于辅助诊断、风险分层或疗效预测。未来将加强实验室与临床的紧密结合,开展相关基础与转化研究,旨在为cGVHD的更精准诊断、早期识别及个性化治疗奠定基础。
最后,我们期望通过优化药物应用、加强团队管理以及患者和家属的积极配合,进一步降低allo-HSCT后cGVHD的发生率,从而显著改善患者的长期生活质量。
专家简介:

袁海龙,博士,主任医师,副教授,博士生导师
新疆医科大学第一附属医院血液病 中心一科副主任
中心一科副主任
中华医学会血液学分会第十二届委员会造血干细胞应用学组组员
中华医学会血液学分会第十一届青年委员会委员
中国抗癌协会血液肿瘤专业委员会第二届青年委员会委员
中国老年医学学会血液学分会第二届委员会委员
中国初级卫生保健基金会造血干细胞移植专业委员会委员
新疆医学会血液学分会常委
主要研究方向:异基因造血干细胞移植治疗恶性血液肿瘤,自体造血干细胞移植 治疗恶性血液肿瘤
治疗恶性血液肿瘤
转载自《血液时讯》
免责声明:该信息仅作医学和科研参考,赛诺菲不建议以任何与您所在国家所批准的处方信息不符的方式使用本产品,本材料仅供医疗卫生专业人士使用。
审核编码:MAT-CN-2601951/V1.0/2026.3
参考文献:
[1]Hong J, Fraebel J, Yang Y, et al. Understanding and treatment of cutaneous graft-versus-host-disease. Bone Marrow Transplant. 2023 Dec;58(12):1298-1313. doi: 10.1038/s41409-023-02109-x. Epub 2023 Sep 20. PMID: 37730800; PMCID: PMC11759061.
[2]Shi CR, Ferreira AL, Kaur M, et al. Cutaneous Chronic Graft-Versus-Host Disease: Clinical Manifestations, Diagnosis, Management, and Supportive Care. Transplant Cell Ther. 2024 Sep;30(9S):S513-S533. doi: 10.1016/j.jtct.2024.05.020. PMID: 39370234; PMCID: PMC12396616.
[3]Baumrin E, Baker LX, Byrne M, et al. Prognostic value of cutaneous disease severity estimates on survival outcomes in patients with chronic graft-vs-host disease. JAMA Dermatol. 2023;159(4):393–402. 10.1001/jamadermatol.2022.6624.
[4]Kurosawa S, Oshima K, Yamaguchi T, et al. Quality of life after allogeneic hematopoietic cell transplantation according to affected organ and severity of chronic graft-versus-host disease. Biol Blood Marrow Transplant J Am Soc Blood Marrow Transplant. 2017;23 (10):1749–1758. 10.1016/j.bbmt.2017.06.011.
[5]Jacobsohn DA, Kurland BF, Pidala J, et al. Correlation between NIH composite skin score, patient-reported skin score, and outcome: results from the Chronic GVHD Consortium. Blood. 2012;120(13):2545–2552. 10.1182/blood-2012-04-424135. quiz 2774.
[6]Curtis LM, Grkovic L, Mitchell SA, et al. NIH response criteria measures are associated with important parameters of disease severity in patients with chronic GVHD. Bone Marrow Transplant. 2014;49(12):1513–1520. 10.1038/bmt.2014.188.
[7]Paun O, Phillips T, Fu P, et al. Cutaneous complications in hematopoietic cell transplant recipients: impact of biopsy on patient management. Biol Blood Marrow Transplant J Am Soc Blood Marrow Transplant. 2013;19 (8):1204–1209. 10.1016/j.bbmt.2013.05.006.
[8]Jagasia MH, Greinix HT, Arora M, et al. National Institutes of Health Consensus Development Project on Criteria for Clinical Trials in Chronic Graft-versus-Host Disease: I. The 2014 Diagnosis and Staging Working Group report. Biol Blood Marrow Transplant. 2015 Mar;21(3):389-401.e1. doi: 10.1016/j.bbmt.2014.12.001. Epub 2014 Dec 18. PMID: 25529383; PMCID: PMC4329079.
[9]中华医学会血液学分会干细胞应用学组.慢性移植物抗宿主病诊断与治疗中国专家共识(2024年版)[J].中华血液学杂志, 2024, 45(08):713-726.DOI:10.3760/cma.j.cn121090-20240611-00217.
[10]Hill GR, Betts BC, Tkachev V, et al. Current Concepts and Advances in Graft-Versus-Host Disease Immunology. Annu Rev Immunol. 2021 Apr 26;39:19-49. doi: 10.1146/annurev-immunol-102119-073227. Epub 2021 Jan 11. PMID: 33428454; PMCID: PMC8085043.
[11]Rosenstein RK, Rose JJ, Brooks SR, et al. Identification of Fibroinflammatory and Fibrotic Transcriptomic Subsets of Human Cutaneous Sclerotic Chronic Graft-Versus-Host Disease. JID Innov. 2023 Dec 7;4(2):100246. doi: 10.1016/j.xjidi.2023.100246. PMID: 38357212; PMCID: PMC10864809.
[12]https://www.nhsa.gov.cn/attach/Ypsn2024/YPSW202400359/YPSW202400359(PPT).pdf
[13]Cutler C, Lee SJ, Arai S, et al. Belumosudil for chronic graft-versus-host disease after 2 or more prior lines of therapy: the ROCKstar study. Blood. 2021;138(22):2278-2289. Blood. 2022 Mar 17;139(11):1772. doi: 10.1182/blood.2022015598. Erratum for: Blood. 2021 Dec 2;138(22):2278-2289. doi: 10.1182/blood.2021012021. PMID: 35298600; PMCID: PMC9211503.
[14]Wang Y, Wu D, Zhang X, et al. A phase II study of belumosudil for chronic graft-versus-host disease in patients who failed at least one line of systemic therapy in China. BMC Med. 2024 Mar 26;22(1):142. doi: 10.1186/s12916-024-03348-5. PMID: 38532458; PMCID: PMC10964632.
[15]Fengjie Kang, Gang Chen, Jianli Xu, et al. EFFECTIVENESS AND SAFETY OF BELUMOSUDIL FOR CUTANEOUS CHRONIC GRAFT-VERSUS-HOST DISEASE: A RETROSPECTIVE STUDY FROM CHINA.2026 EBMT:Abstract B068.
