
从机制到疗法:靶向降解STING为治疗玫瑰痤疮提供新思路
前言
玫瑰痤疮 是一种慢性炎症性皮肤病,以面部持续性红斑、毛细血管扩张为主要临床特征,常伴有丘疹、脓疱及阵发性潮红,严重影响患者生活质量。其发病机制复杂,涉及先天免疫失调、神经血管功能异常、微生物因素及环境触发等。抗菌肽LL37在玫瑰痤疮皮损
是一种慢性炎症性皮肤病,以面部持续性红斑、毛细血管扩张为主要临床特征,常伴有丘疹、脓疱及阵发性潮红,严重影响患者生活质量。其发病机制复杂,涉及先天免疫失调、神经血管功能异常、微生物因素及环境触发等。抗菌肽LL37在玫瑰痤疮皮损 中显著高表达,被认为是启动炎症的关键分子。肥大细胞作为先天免疫的哨兵细胞及关键炎症效应细胞,在玫瑰痤疮发病中扮演核心角色,但其被LL37激活的具体分子机制尚未完全阐明。近年来,氧化应激与线粒体功能紊乱在慢性炎症性疾病中的作用备受关注,而胞质DNA感应通路cGAS-STING在连接线粒体损伤与先天免疫激活中具有重要地位。本研究旨在探究LL37是否通过诱导肥大细胞线粒体应激、线粒体DNA(mtDNA)泄漏,进而激活cGAS/STING/核因子κB(NF-κB)信号通路,从而驱动玫瑰痤疮炎症反应。
中显著高表达,被认为是启动炎症的关键分子。肥大细胞作为先天免疫的哨兵细胞及关键炎症效应细胞,在玫瑰痤疮发病中扮演核心角色,但其被LL37激活的具体分子机制尚未完全阐明。近年来,氧化应激与线粒体功能紊乱在慢性炎症性疾病中的作用备受关注,而胞质DNA感应通路cGAS-STING在连接线粒体损伤与先天免疫激活中具有重要地位。本研究旨在探究LL37是否通过诱导肥大细胞线粒体应激、线粒体DNA(mtDNA)泄漏,进而激活cGAS/STING/核因子κB(NF-κB)信号通路,从而驱动玫瑰痤疮炎症反应。
 (NAC)、mPTP抑制剂环孢素A
(NAC)、mPTP抑制剂环孢素A (CsA)以及STING靶向蛋白降解嵌合体(PROTAC)化合物SP23进行干预。体内实验通过皮内注射LL37构建小鼠玫瑰痤疮样皮炎模型,局部外用CsA或SP23乳膏,评估皮肤炎症程度、肥大细胞活化及相关分子表达。
(CsA)以及STING靶向蛋白降解嵌合体(PROTAC)化合物SP23进行干预。体内实验通过皮内注射LL37构建小鼠玫瑰痤疮样皮炎模型,局部外用CsA或SP23乳膏,评估皮肤炎症程度、肥大细胞活化及相关分子表达。1. 转录组分析揭示cGAS-STING信号通路在玫瑰痤疮皮损中显著富集
对GSE65914数据集的分析显示,玫瑰痤疮皮损中存在1608个差异表达基因。KEGG通路富集分析发现“胞质DNA感应通路”和“NF-κB信号通路”显著富集(图1D)。基因集富集分析进一步证实cGAS-STING相关基因集在皮损中高表达(图1E)。相关性分析显示,cGAS(MB21D1)和STING(TMEM173)的表达与静息态肥大细胞浸润呈负相关(图1F, G),提示该通路的激活可能与肥大细胞功能活化同步发生。
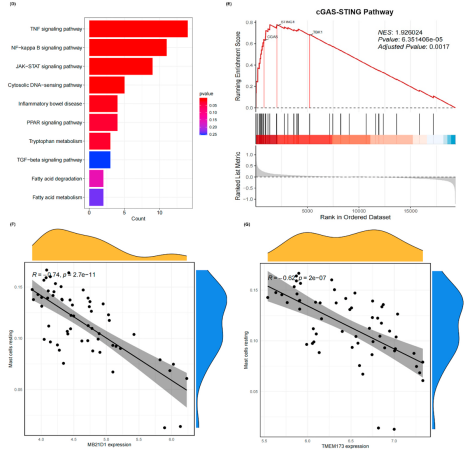
图1:转录组分析显示玫瑰痤疮皮损中cGAS-STING信号通路显著富集
2. LL37诱导肥大细胞氧化应激、mPTP开放及脱颗粒
LL37刺激显著升高LUVA细胞内ROS水平(图2A),并促进其线粒体ROS生成、降低线粒体膜电位(图2C, D)。透射电镜观察显示LL37导致线粒体肿胀、空泡化和嵴结构破坏(图2E)。Calcein AM染色表明LL37诱导mPTP开放(图2F),且ROS积累早于mPTP开放(图2G)。酶联免疫吸附试验 (ELISA)检测发现,LL37刺激后组胺、β-己糖胺酶(β-Hex)以及白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)、CCL2、MMP-9等炎症介质释放显著增加(图2H),证实肥大细胞脱颗粒。
(ELISA)检测发现,LL37刺激后组胺、β-己糖胺酶(β-Hex)以及白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)、CCL2、MMP-9等炎症介质释放显著增加(图2H),证实肥大细胞脱颗粒。
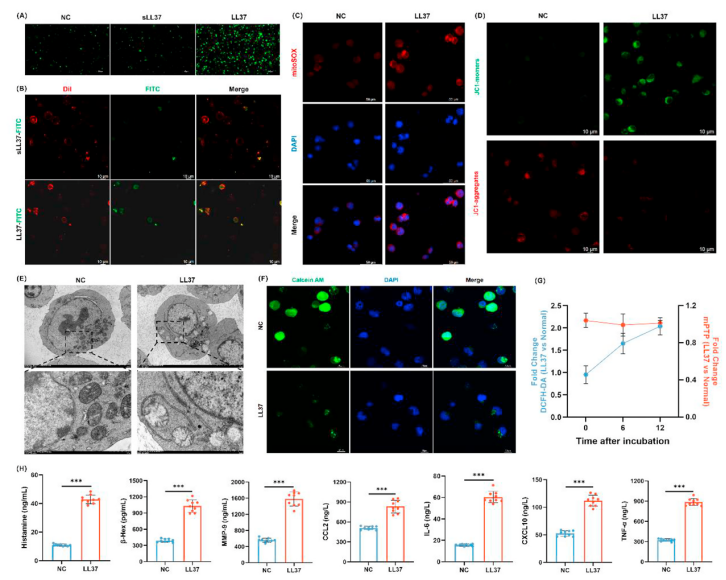
图2:LL37在肥大细胞中诱导氧化应激、mPTP开放和脱颗粒
3. LL37促进mtDNA泄漏并激活cGAS/STING/NF-κB通路
qPCR检测显示LL37刺激后胞质mtDNA(ND1, ND2)水平显著升高(图3A),免疫荧光亦观测到胞质双链DNA增多(图3B)。Western blot及免疫荧光显示cGAS、STING表达上调,NF-κB亚基p65磷酸化增强(图3D, E)。为明确mtDNA来源,研究构建了mtDNA耗竭的ρ0细胞。在ρ0细胞中,LL37未能诱导cGAS、STING、p-p65上调(图3D, E),胞质DNA与cGAS的共定位及CUT&RUN结合信号也显著减弱(图3F, G),且细胞因子释放和脱颗粒被抑制(图3H)。这些结果证实LL37通过诱导线粒体损伤和mtDNA泄漏激活cGAS/STING/NF-κB通路。
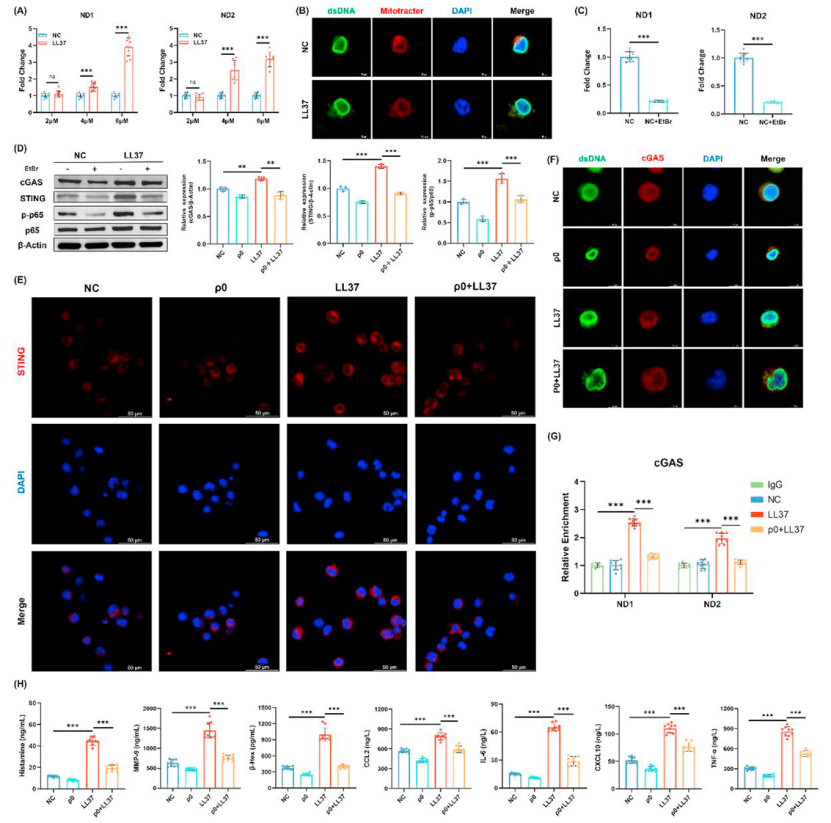
图3:LL37 促进线粒体 DNA 泄漏并激活肥大细胞中的 cGAS/STING/NF-κB 通路
4. 抑制氧化应激、mPTP或降解STING可阻断LL37诱导的肥大细胞活化
抗氧化剂NAC预处理能恢复线粒体膜电位、降低mtROS,抑制胞质mtDNA积累(图4A-D),并减少cGAS与胞质DNA的结合及下游信号激活(图4E-H),进而抑制炎症介质释放(图4I)。
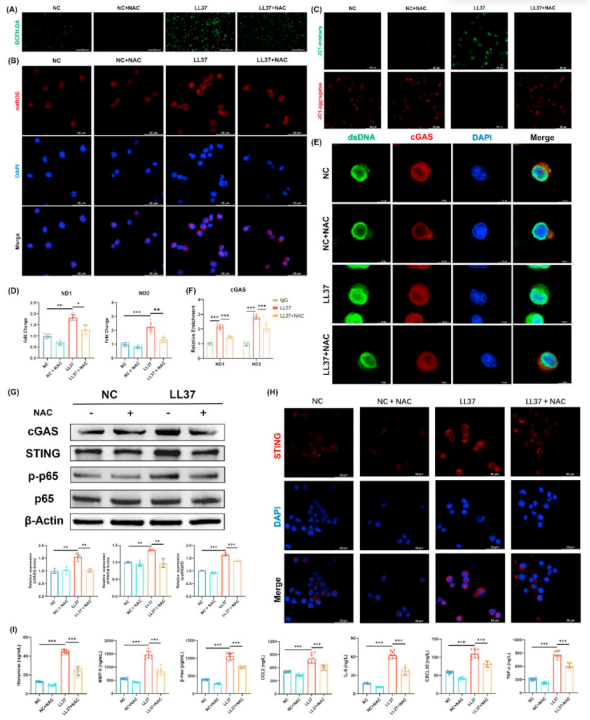
图4:抑制氧化应激可抑制LL37诱导的线粒体DNA泄漏和肥大细胞脱颗粒
mPTP抑制剂CsA能显著抑制LL37诱导的mPTP开放、mtDNA泄漏(图5A, B)及cGAS/STING/NF-κB通路活化(图5C-F),并降低脱颗粒标志物和细胞因子水平(图5G)。STING降解剂SP23可特异性降低STING蛋白表达及p65磷酸化(图5I, J),而不影响上游cGAS,同样有效抑制肥大细胞脱颗粒(图5K)。
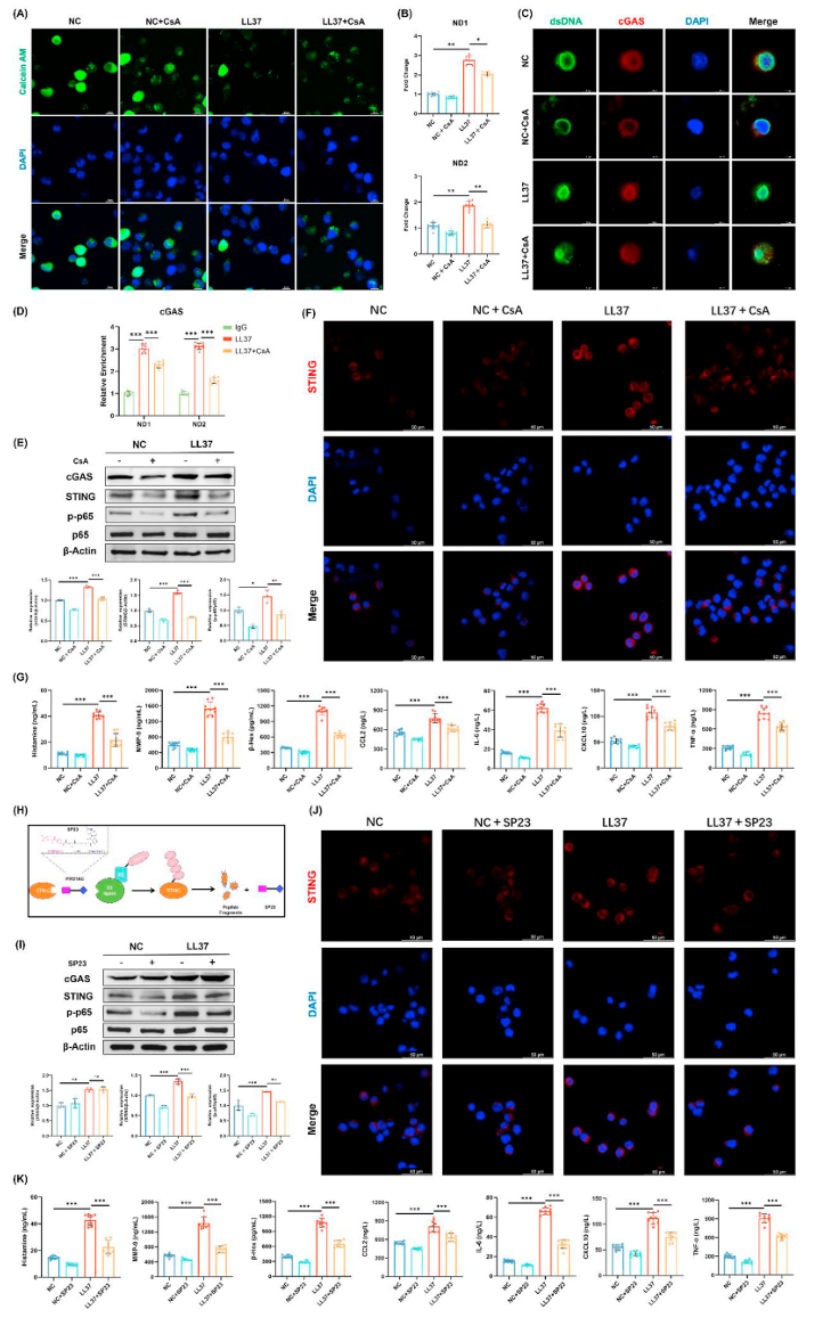
图5:mPTP抑制和STING降解抑制LL37诱导的肥大细胞脱颗粒
5. 靶向干预mPTP和STING缓解小鼠玫瑰痤疮样皮炎
在LL37诱导的小鼠玫瑰痤疮样模型中,皮损区域ROS水平升高(图6B),氧化DNA损伤标志物8-羟基脱氧鸟苷(8-OH-dG)与肥大细胞共定位(图6C),cGAS、STING及p-p65在真皮肥大细胞中表达上调(图6F, G)。局部外用CsA或SP23乳膏可显著减轻皮肤红斑、缩小皮损面积(图6D),减少真皮炎症细胞浸润(图6E),并抑制cGAS/STING/NF-κB通路活化及相关炎症介质释放(图6F-H)。
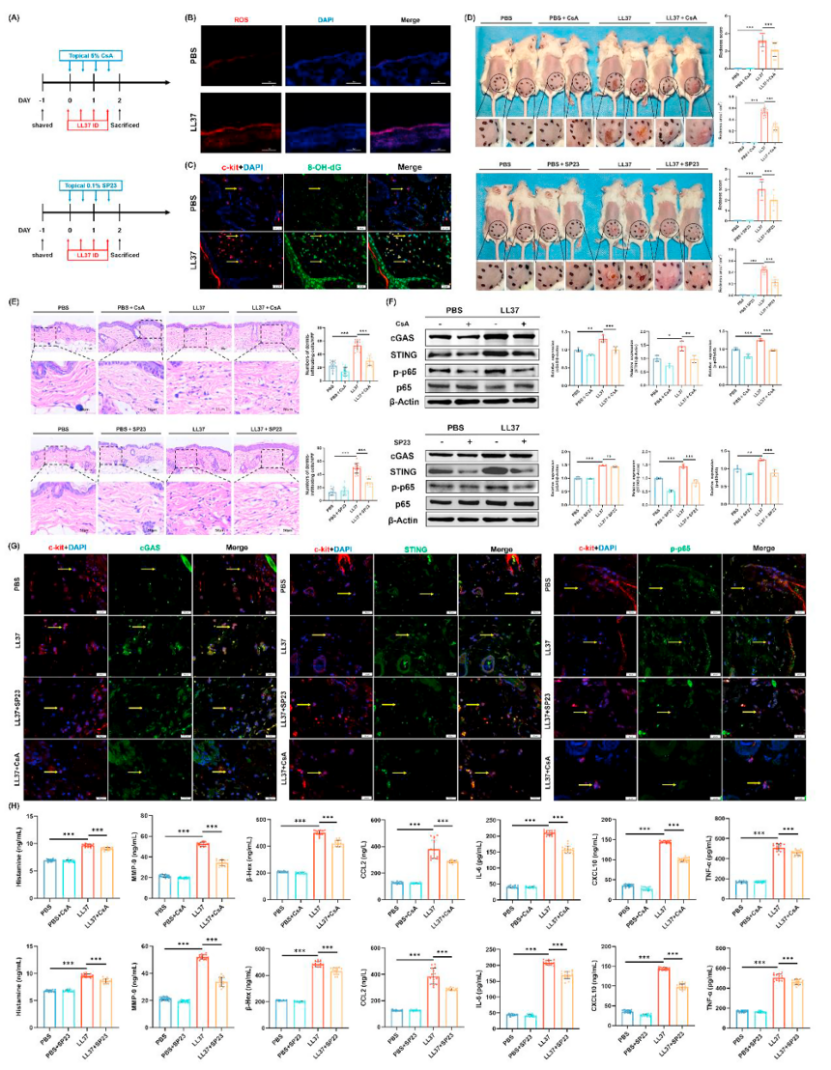
图6:抑制mPTP和降解STING缓解LL37诱导的小鼠玫瑰痤疮样皮炎
本研究系统阐明了LL37通过诱导线粒体氧化应激、损伤线粒体结构、开放mPTP,导致mtDNA泄漏至胞质;胞质mtDNA进而激活cGAS/STING/NF-κB先天免疫信号通路,驱动肥大细胞脱颗粒及炎症介质释放,最终促进玫瑰痤疮皮肤炎症的发生发展。研究揭示了LL37–mtDNA–cGAS/STING轴在肥大细胞介导的玫瑰痤疮炎症中的关键作用,并从多环节验证了靶向该通路(如抗氧化、抑制mPTP、降解STING)的有效性,为玫瑰痤疮的靶向治疗提供了新的理论依据和潜在策略。
参考文献:Sun R, Fan H, Ma Q, Li X, Liu J, Xu C, Liu C, Zhang D, Ma W. LL37-induced mitochondrial stress activates the mtDNA/cGAS/STING pathway to promote mast cell-mediated rosacea inflammation. Free Radic Biol Med. 2026 Feb 16;244:422-434.
医脉通是专业的在线医生平台,“感知世界医学脉搏 ,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。

