
王黎、刘玉、赵维莅教授:精准免疫重塑,西达本胺上调ALOX15B表达,逆转del(17p)DLBCL免疫抑制,破解高危患者治疗难题
del(17p)是恶性肿瘤中常见的染色体 异常,与不良预后密切相关1。临床发现,在接受标准免疫化疗方案的弥漫性大B细胞淋巴瘤
异常,与不良预后密切相关1。临床发现,在接受标准免疫化疗方案的弥漫性大B细胞淋巴瘤 (DLBCL)患者中,携带del(17p)的患者临床转归存在较大差异,而位于染色体17p的花生四烯酸15-脂氧合酶B型(ALOX15B)可通过调控花生四烯酸(AA)代谢参与免疫反应调节,或在疾病进展和治疗应答中起关键作用2。
(DLBCL)患者中,携带del(17p)的患者临床转归存在较大差异,而位于染色体17p的花生四烯酸15-脂氧合酶B型(ALOX15B)可通过调控花生四烯酸(AA)代谢参与免疫反应调节,或在疾病进展和治疗应答中起关键作用2。
近日,上海交通大学医学院附属瑞金医院和四川大学华西医院 在《Journal of Experimental & Clinical Cancer Research》上联合发表了题为“Low expression of ALOX15B modulates immunosuppressive tumor microenvironment in diffuse large B-cell lymphoma via the TAP1/MHC-I axis”的研究成果,深入探索了ALOX15B在DLBCL中的作用和潜在治疗价值2。借此契机,医脉通特邀改为上海交通大学医学院附属瑞金医院王黎
在《Journal of Experimental & Clinical Cancer Research》上联合发表了题为“Low expression of ALOX15B modulates immunosuppressive tumor microenvironment in diffuse large B-cell lymphoma via the TAP1/MHC-I axis”的研究成果,深入探索了ALOX15B在DLBCL中的作用和潜在治疗价值2。借此契机,医脉通特邀改为上海交通大学医学院附属瑞金医院王黎 教授、四川大学华西医院刘玉教授、上海交通大学医学院附属瑞金医院赵维莅
教授、四川大学华西医院刘玉教授、上海交通大学医学院附属瑞金医院赵维莅 教授就该研究成果进行深入解读,以飨读者。
教授就该研究成果进行深入解读,以飨读者。

携带del(17p)的DLBCL患者接受标准R-CHOP(利妥昔单抗 、环磷酰胺
、环磷酰胺 、多柔比星
、多柔比星 、长春新碱
、长春新碱 和泼尼松
和泼尼松 )方案的预后异质性较强,而ALOX15B位于染色体17p,可通过参与AA代谢,生成前列腺素等脂质介质,影响炎症和免疫调节,本研究旨在探讨ALOX15B在DLBCL进展中的作用,明确其是否通过调控免疫微环境及抗原呈递影响患者治疗反应与预后。
)方案的预后异质性较强,而ALOX15B位于染色体17p,可通过参与AA代谢,生成前列腺素等脂质介质,影响炎症和免疫调节,本研究旨在探讨ALOX15B在DLBCL进展中的作用,明确其是否通过调控免疫微环境及抗原呈递影响患者治疗反应与预后。
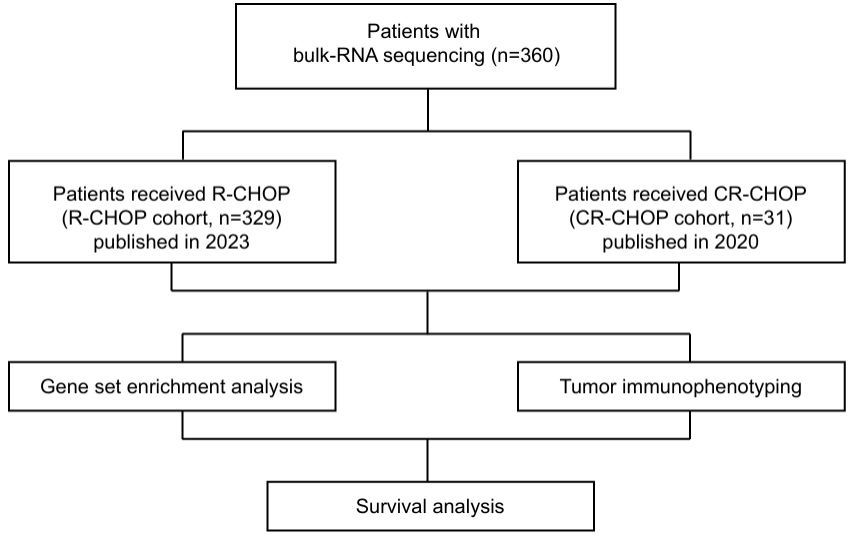
研究分析了360例新诊断DLBCL患者的总体转录组与单细胞转录组数据,以评估ALOX15B表达情况,以及其与临床结局、免疫微环境和治疗耐药的关系(图1,分别为R-CHOP组[n=329]和西达本胺 联合R-CHOP组[n=31])。在DLBCL细胞系中,通过siRNA敲低实验、荧光素酶报告基因实验以及细胞增殖实验进行功能验证;通过小鼠模型与患者来源异种移植(PDX)模型评估体内肿瘤行为及治疗效果;通过染色质免疫沉淀测序(ChIP-seq)和转座酶可及染色质测序(ATAC-seq)探究ALOX15B的表观遗传调控机制。
联合R-CHOP组[n=31])。在DLBCL细胞系中,通过siRNA敲低实验、荧光素酶报告基因实验以及细胞增殖实验进行功能验证;通过小鼠模型与患者来源异种移植(PDX)模型评估体内肿瘤行为及治疗效果;通过染色质免疫沉淀测序(ChIP-seq)和转座酶可及染色质测序(ATAC-seq)探究ALOX15B的表观遗传调控机制。
通过差异基因分析和Kaplan-Meier生存分析,研究者发现ALOX15B低表达与DLBCL患者无进展生存期(PFS)较差相关,提示其具有重要的预后预测价值(图2)。
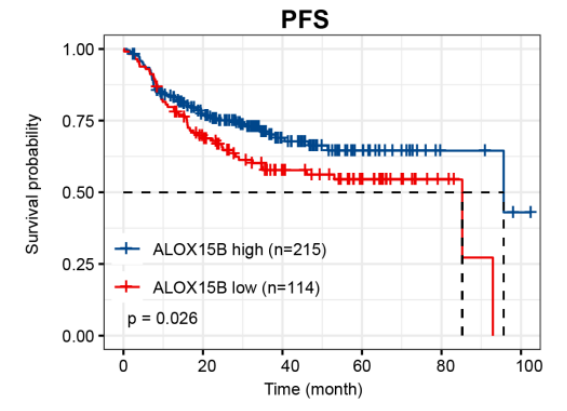
图2 不同ALOX15B表达程度的患者应用R-CHOP的PFS
基因本体富集分析显示,ALOX15B低表达组中多个前列腺素相关生物学过程显著富集(图3);基因集富集分析表明,肿瘤中免疫相关通路显著下调,前列腺素信号通路及多种致癌信号通路显著上调(图4),提示ALOX15B低表达导致AA代谢失衡,使代谢通路偏向COX-2/PGE2信号轴异常激活,而PGE2的升高可促进肿瘤细胞增殖、抑制凋亡,并通过多种途径重塑免疫抑制性肿瘤微环境。
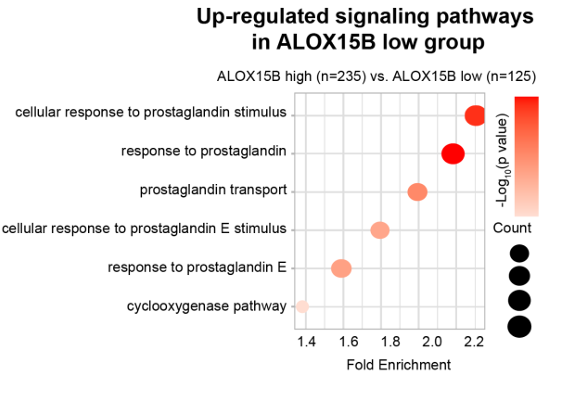
图3 ALOX15B低表达组的上调信号通路
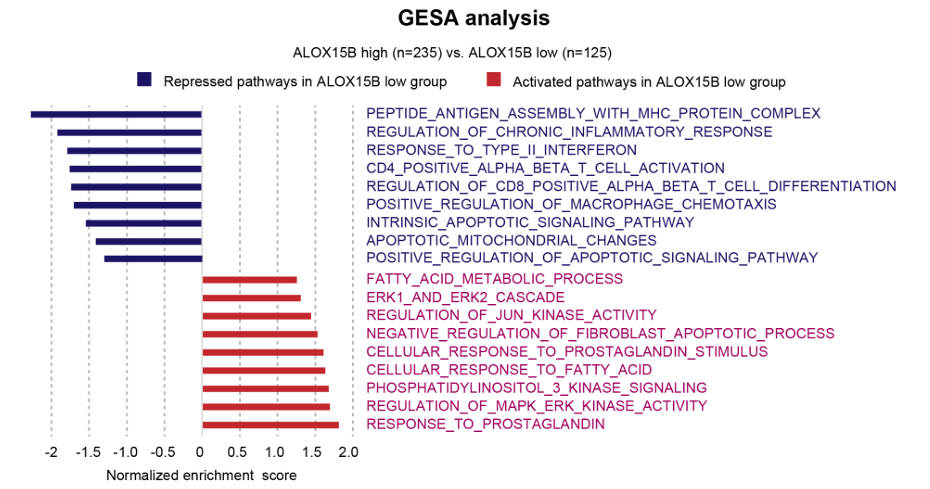
图4 不同ALOX15B表达组的抑制和激活信号通路
单细胞RNA测序进一步揭示,在ALOX15B低表达的肿瘤免疫微环境中,TAP1及MHC-I分子(HLA-A/B/C)显著下调(图5),导致抗原加工与呈递能力受损,从而削弱CD8+T细胞对肿瘤细胞的识别和杀伤功能。
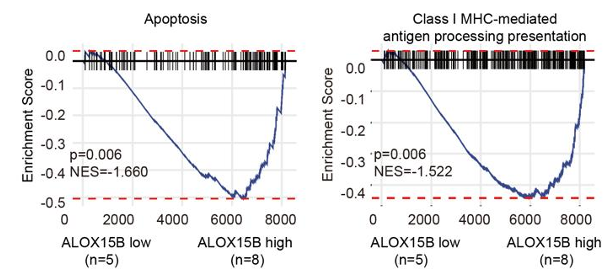
图5 不同ALOX15B表达组的TAP1及MHC-I分子抗原加工与呈递能力
相应地,ALOX15B低表达患者中CD8+T细胞的细胞毒性评分明显降低,表明存在显著的免疫逃逸现象,提示其是潜在的治疗靶点(图6)。
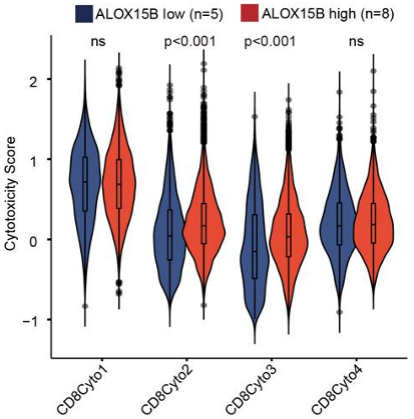
图6 不同ALOX15B表达组CD8+T细胞的细胞毒性评分
体外实验证实,沉默ALOX15B可促进DLBCL细胞增殖(DB、U2932),并增强其对多柔比星的耐药性(图7A-B);体内实验发现,改为ALOX15B敲低的小鼠模型表现为免疫细胞浸润减少(图7C-D)、抗原呈递信号减弱(图7E)、MHC-I介导的细胞间通讯减弱(图7F-G)的特征,从而形成免疫抑制性微环境。
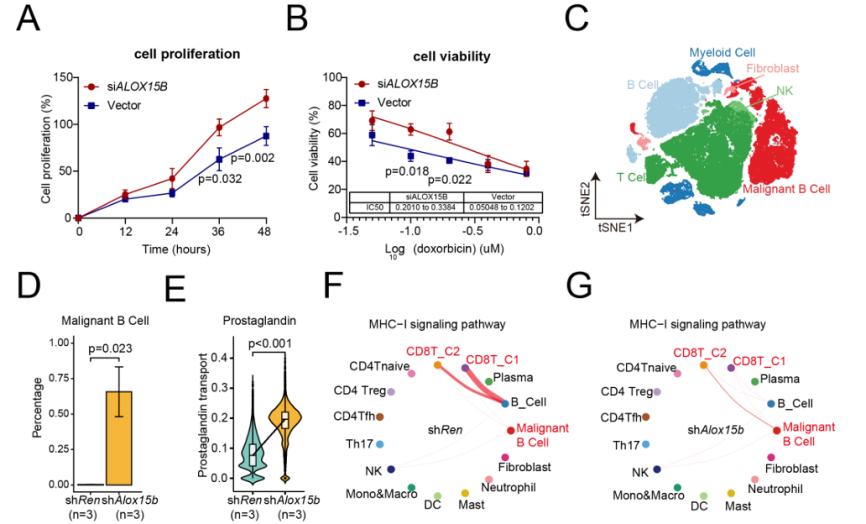
图7 ALOX15B敲除对细胞增殖、存活和免疫应答的影响
免疫组化及ChIP-seq分析显示,HDAC1和HDAC2在ALOX15B启动子区域高度富集,可通过抑制组蛋白乙酰化下调ALOX15B转录(图8)。
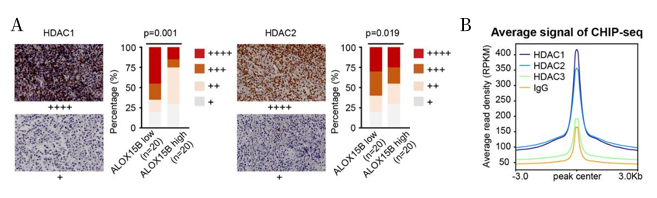
图8 免疫组化(A)及ChIP-seq(B)结果
HDAC抑制剂西达本胺单药或联合治疗可显著恢复ALOX15B的染色质可及性和表达水平(图9A),抑制PGE2通路,重建TAP1/MHC-I抗原呈递轴,增强CD8+T细胞介导的抗肿瘤免疫反应,促进肿瘤细胞凋亡(图9B)。临床相关性分析也进一步表明,在R-CHOP方案中加入西达本胺可明显改善ALOX15B低表达患者的不良预后(图10)。
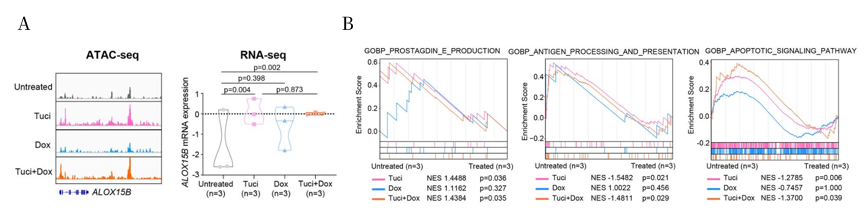
图9 西达本胺可恢复ALOX15B表达并重塑抗肿瘤免疫
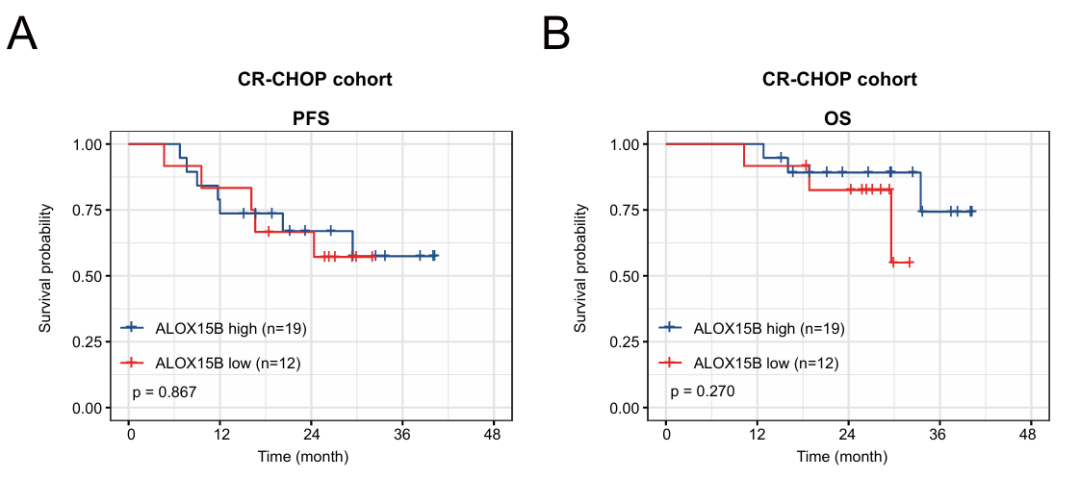
图10 西达本胺联合R-CHOP方案的疗效
ALOX15B是DLBCL发生发展中关键的表观遗传调控基因,可通过调控肿瘤免疫微环境影响DLBCL对化疗的应答,其下调可促进免疫逃逸和治疗耐药,而西达本胺能有效恢复ALOX15B的表达并增强抗肿瘤免疫反应。该研究提示ALOX15B在作为预后生物标志物和治疗靶点方面的潜力,尤其适用于携带del(17p)的DLBCL患者。

王黎教授
染色体拷贝数变异是肿瘤的常见特征之一,其中del(17p)与预后不良密切相关,携带del(17p)的DLBCL患者接受标准免疫化疗策略获益有限,一直是临床中的治疗难题。本研究系统揭示了位于染色体17p的ALOX15B在DLBCL中的关键免疫调控作用,证实其低表达与患者免疫逃逸和治疗耐药密切相关。值得注意的是,ALOX15B低表达受到HDAC1和HDAC2调控,而HDAC抑制剂西达本胺可通过恢复ALOX15B表达,增强抗原呈递,促进淋巴瘤细胞凋亡,重塑抗肿瘤免疫,并有效抑制DLBCL细胞的体内外增殖,一项采用西达本胺联合R-CHOP方案治疗新诊断DLBCL患者的II期研究亦显示,西达本胺的加入改善了ALOX15B低表达且对R-CHOP应答不佳患者的预后,PFS明显延长2。该研究表明,西达本胺可通过恢复ALOX15B表达,改善ALOX15B低表达患者的免疫微环境和治疗反应,为未来优化高危患者的个体化治疗策略,实现西达本胺在DLBCL中的精准应用提供了理论依据2。

刘玉教授
传统观点认为,del(17p)仅通过导致TP53杂合性缺失影响预后,但研究者们发现,del(17p)带来的表型超出了仅通过TP53缺失展现出的表型,证明染色体片段缺失事件可能由多个基因的选择性优势破坏而产生1,3。
除ALOX15B这一在DLBCL发生发展中起关键作用的表观遗传调控基因外,我中心此前也就del(17p)促进肿瘤发生发展的机制展开探索,发现位于染色体17p的全新抑癌基因PHF23缺失会严重妨碍B细胞分化,导致B细胞淋巴瘤的发生:PHF23通过PSH复合物抑制HDAC的组蛋白H3K27去乙酰化功能,从而协调H3K4me3和H3K27ac两个不同的组蛋白修饰促进基因表达,尤其抑癌基因以及p53通路相关基因的上调1。研究发现,PHF23基因敲除鼠的肿瘤发生时间较野生型明显提前,生存时间显著缩短;而HDAC抑制剂如西达本胺可特异性诱导PHF23缺失的淋巴瘤细胞死亡,且对正常细胞无显著影响,为HDAC抑制剂治疗PHF23基因缺失型血液肿瘤奠定了理论基础。研究同时指出,这一网络的失调有一个共同的调控弱点——即对表观遗传修饰的依赖性(HDAC介导的抑制)。这正是西达本胺发挥独特作用的科学基础,它通过逆转该区域内多个关键基因的沉默,系统性修复由染色体缺失驱动的恶性肿瘤生物学行为,为真正意义上的“高危型DLBCL精准治疗”策略提供了支撑。

赵维莅教授
近年来,临床对DLBCL生物学特征的认识不断深入,其中携带del(17p)的患者预后异质性较强,成为研究者探索的热点。我中心参与的这项研究阐明了位于染色体17p区域的AA代谢相关基因ALOX15B在DLBCL发生发展、免疫微环境调控及治疗反应中的关键作用:ALOX15B低表达可导致AA代谢失衡,激活COX-2/PGE2信号轴,而PGE2的升高可促进肿瘤细胞增殖、抑制凋亡,通过多种途径重塑免疫抑制性肿瘤微环境。在ALOX15B低表达的免疫抑制性肿瘤微环境中,TAP1及MHC-I分子均显著下调,造成抗原加工与呈递能力受损,CD8+ T细胞的识别和杀伤功能减弱,导致免疫逃逸现象。
值得一提的是,HDAC1/2在ALOX15B启动子区域高度富集,可通过抑制组蛋白乙酰化下调ALOX15B转录,而西达本胺可通过恢复ALOX15B的染色质可及性与表达水平,逆转上述过程,重建抗肿瘤免疫。这一发现不仅丰富了临床对17p区域基因功能的认知,也为西达本胺在DLBCL中的精准应用提供了重要参考。未来仍需继续探索高危细胞遗传学因素在DLBCL治疗中的关键作用,为高危人群开辟更多有效的精准治疗路径。

王黎 教授
上海交通大学医学院附属瑞金医院血液科, 主任医师, 博导,教授
国家优秀青年医师
法国国立生命与健康研究院博士后
中国抗癌协会淋巴瘤整合康复委员会副主任委员
中国CSCO淋巴瘤专委会常委
中华医学会第十一届血液学分会青年委员
中国抗癌协会淋巴浆细胞肿瘤协作组副组长
上海市抗癌协会淋巴瘤专委会副主任委员
主要完成人获国家/省部级奖项10项
上海市教委高原高峰人才
上海市杰出青年医学人才
上海市巾帼创新新秀
上海市东方英才
上海市三八红旗手
刘玉 教授
四川大学华西医院生物治疗全国重点实验室教授、博士生导师
教育部长江学者
中国医药生物技术协会基因编辑技术分会常务委员
中国病理生理学会实验血液学专委会委员
中国抗癌协会肿瘤代谢专业委员会全国委员
中国细胞生物学会细胞代谢分会理事
长期从事血液肿瘤发病机制的研究和新治疗方案的探索。利用基因编辑、小鼠肿瘤模型和多组学分析等技术解析染色体拷贝数变异在癌症发生发展中的生物学功能与分子机制。在Nature、Cancer Discovery、Cancer Cell、Blood和STTT等期刊发表36篇研究论文
主持国家科技重大专项、国家自然基金委重点/面上项目等

赵维莅 教授
主任医师,教授,博士生导师
国家杰出青年科学基金获得者
教育部长江学者特聘教授
科技部万人计划领军人才
百千万人才工程国家级人选
上海交通大学医学院附属瑞金医院副院长
上海血液学研究所所长,上海市重中之重临床医学中心主任
国家血液内科专业医疗质量控制中心(筹)共同主任
中华医学会血液学分会副主任委员,淋巴细胞疾病学组组长
中国病理生理学会理事,实验血液学专委会副主任委员
中国临床肿瘤学会淋巴瘤专家委员会副主任委员
致力于淋巴细胞疾病的临床和基础研究,以通讯/第一作者在《The New England Journal of Medicine 》、《CANCER CELL》、《NATURE GENETICS》、《BLOOD》、《LANCET HAEMATOL》、《SIGNAL TRANSDUCT TARGET THER》、《J HEMATOL ONCOL》等国际权威杂志发表文章110余篇,总影响因子超过1600。以团队带头人获国家科技进步奖创新团队奖,以第一完成人获国家科学技术进步奖二等奖1项、省部级一等奖6项,获国际发明专利2项、国家发明专利16项,主持国家科技部重点研发计划、863 重大项目、国家自然科学基金重点项目等22项。先后荣获 “全国卫生系统先进工作者”、“全国三八红旗手”、中国青年女科学家奖、法国国家医学科学院Charpak-Dubousset奖、EBMT青年领袖奖、吴阶平医药创新奖、谈家桢生命科学奖、上海市科技精英等多项荣誉。
参考文献
1.Chen M, et al. An Epigenetic Mechanism Underlying Chromosome 17p Deletion-Driven Tumorigenesis. Cancer Discov. 2021 Jan;11(1):194-207.
2.Wang L, et al. Low expression of ALOX15B modulates immunosuppressive tumor microenvironment in diffuse large B-cell lymphoma via the TAP1/MHC-I axis. J Exp Clin Cancer Res. 2026 Jan 12.
3.Liu Y, et al. Deletions linked to TP53 loss drive cancer through p53-independent mechanisms. Nature. 2016 Mar 24;531(7595):471-475.
戳“阅读原文”,查看更多内容

