
基于多维度机制与人工智能驱动的宫颈上皮内病变精准诊疗研究进展
作者:晏玉玲,杨 欢,王延琨,李思 婧等,重庆市妇幼保健院(重庆医科大学附属妇女儿童医院)妇产科,重庆市妇幼疾病预防控制与公共卫生研究中心,国家临床重点专科(妇产科)
婧等,重庆市妇幼保健院(重庆医科大学附属妇女儿童医院)妇产科,重庆市妇幼疾病预防控制与公共卫生研究中心,国家临床重点专科(妇产科)
子宫颈鳞状细胞肿瘤前驱病变命名分为低级别鳞状上皮内病变(low⁃gradesquamousintraepitheliallesion,LSIL)和高级别鳞状上皮内病变(high⁃gradesquamousintraepithelialle⁃sions,HSIL)。一项荟萃分析显示,宫颈LSIL患者自然消退概率为57.81%,持续宫颈LSIL概率为40.01%,而进展为宫颈HSIL的概率仅为5.69%[1]。一项前瞻性观察研究显示,经保守治疗,宫颈HSIL患者中有73.5%的患者消退,14.8%的患者持续感染,11.7%进展为更高级别病变[2]。2019年美国阴道镜和子宫颈病理学会(TheAmericanSocietyforColpos⁃copyandCervicalPathology,ASCCP)指南中提到根据不同风险阈值,进行规范化、个性化、精准化的基于风险的分层管理。宫颈上皮内病变的转归受HPV感染、宿主微环境等多维度因素调控,这些可量化的关键因素,为AI驱动的精准评估提供了核心依据。
1 HPV感染特征与疾病进展
人乳头瘤病毒(humanpapillomavirus,HPV)是一种常见的性传播病毒,HPV持续感染仍是宫颈病变的主要因素,目前国内外对宫颈病变的研究现状主要集中在HPV感染情况、宫颈病变的筛查和预防以及宫颈病变的治疗策略上。研究表明,宫颈癌 患者中90%以上伴有HR⁃HPV感染,其中HPV16型及HPV18型占比70%以上,宫颈疾病的发生依赖于HPVE6/E7基因的组成性表达[3]。
患者中90%以上伴有HR⁃HPV感染,其中HPV16型及HPV18型占比70%以上,宫颈疾病的发生依赖于HPVE6/E7基因的组成性表达[3]。
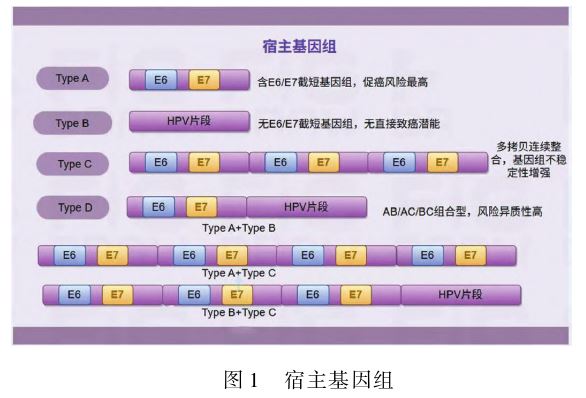
1.1 HPV整合与致癌机制 HPV整合指的是HPV的DNA序列插入到宿主细胞的基因组中,HPV整合是宫颈癌发生的关键步骤。HPV整合事件在宫颈癌中具有不同的类型,包括含E6/E7基因的截短HPV基因组(TypeA)、不含E6/E7基因的截短HPV基因组(TypeB)、含多个连续的HPV基因组(TypeC)以及这些类型的组合(TypeD)[4]。见图1。于艳芳等[5]认为,HPV病毒基因与宿主基因的整合可能导致宿主细胞基因组不稳定,增加基因组不稳定性,导致大的染色体 重排和拷贝数变异,与宫颈癌的发生发展有关。马丁
重排和拷贝数变异,与宫颈癌的发生发展有关。马丁 等[6]研究表明,HPV基因整合不仅可用于癌症筛查、疾病检测,同时也可用于治疗,即直接靶向切除基因整合序列达到治疗效果,但基因双链的断裂可能作为新的致癌因素,使基因组损伤以及出现重排的风险。
等[6]研究表明,HPV基因整合不仅可用于癌症筛查、疾病检测,同时也可用于治疗,即直接靶向切除基因整合序列达到治疗效果,但基因双链的断裂可能作为新的致癌因素,使基因组损伤以及出现重排的风险。
1.2 HPV病毒载量动态监测 HPV病毒载量与宫颈病变程度之间存在相关性,对于HPV16感染,其病毒载量可有效区分宫颈HSIL和宫颈LSIL,且在单一和多重HPV感染中均展现出良好的敏感性和特异性[7]。HPV病毒载量越高,患者发展为更高级别宫颈病变或宫颈癌的风险几率越大,总体预后也相对越差[8]。高病毒载量常提示持续感染状态,消退的概率较低,而非持续性HPV感染的病毒载量在感染后约两个月达到平稳期,持续13~20个月后迅速下降[9]。因此,动态监测HPV病毒载量可更准确地评估感染风险、预测疾病进展,并为临床决策提供重要参考。
1.3 HPV疫苗接种HPV疫苗接种目前仍是预防宫颈癌的主要手段。据WHO2023年全球疫苗接种覆盖率统计,全球女孩接种第一剂HPV疫苗的覆盖率从2022年的20%增长到27%,全程接种覆盖率从2019年的13%增长到20%。数据显示,未接种HPV疫苗人群中HPV感染者占16.2%,而接种HPV疫苗人群中HPV感染者占1.48%[10],可见HPV疫苗在宫颈癌的预防中发挥着重要作用,能有效降低HPV感染的风险。越来越多研究表明,对于宫颈HSIL进行手术治疗的患者,接种宫颈HPV疫苗可明显降低再次发生宫颈病变的机率[11-13]。
2 宿主微环境与病变进展
阴道微生态是指由阴道微生物群、宿主的内分泌物系统、阴道解剖结构及阴道局部免疫系统共同组成的生态系统。正常情况下,大量微生物聚集在女性生殖道中,并在宿主形成相互约束的动态平衡。健康的阴道菌群可预防阴道感染、消除炎症、维持阴道微生态平衡。
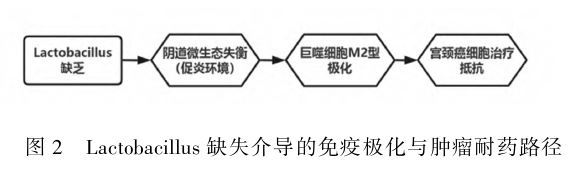
2.1 阴道菌群⁃免疫交互作用 阴道微环境与HPV持续感染、宫颈癌前病变及宫颈癌的发生发展密切相关。阴道微生态中所含有的脯氨酰氨肽酶以及乙酰氨基葡萄糖 苷酶阳性均可增加患者HPV感染的风险,同时有明显诊断效果[14]。国内外研究显示,癌症生物标志物的表达与阴道微生物群组成和阴道pH相关,宫颈癌前病变患者阴道微生态失衡、各类细菌、真菌异常发生率明显高于正常患者[15-16]。同时,阴道微生态中乳酸杆菌缺乏可能导致阴道的促炎环境,从而增加恶性细胞增殖和HPVE6、E7癌基因表达[17],乳酸杆菌科缺乏可导致巨噬细胞诱导为M2型[18]。研究表明,诱导巨噬细胞的M2型极化可促进宫颈癌细胞的治疗抵抗[19]。见图2。同时,阴道微生态失衡也不利于HPV转阴,可能形成恶性循环,促进宫颈病变的发展。此外,宫颈病变与免疫系统疾病有关,如HIV感染等。目前HIV感染人群呈逐渐上升趋势,截至2022年年底,大约有3900万例HIV感染者,130万新发病例,63万例死于HIV相关疾病。HIV感染很大程度上会促进HPV的传播,HIV阳性患者宫颈病变发展为HSIL的概率约为HIV阴性患者的3倍[20]。同时HR⁃HPV的感染也增加了基因型脆弱性[21]。国外一项横断面研究显示[22],HIV感染与宫颈癌前病变密切相关,对于宫颈LSIL患者,HIV阳性患者比HIV阴性患者更为常见。
苷酶阳性均可增加患者HPV感染的风险,同时有明显诊断效果[14]。国内外研究显示,癌症生物标志物的表达与阴道微生物群组成和阴道pH相关,宫颈癌前病变患者阴道微生态失衡、各类细菌、真菌异常发生率明显高于正常患者[15-16]。同时,阴道微生态中乳酸杆菌缺乏可能导致阴道的促炎环境,从而增加恶性细胞增殖和HPVE6、E7癌基因表达[17],乳酸杆菌科缺乏可导致巨噬细胞诱导为M2型[18]。研究表明,诱导巨噬细胞的M2型极化可促进宫颈癌细胞的治疗抵抗[19]。见图2。同时,阴道微生态失衡也不利于HPV转阴,可能形成恶性循环,促进宫颈病变的发展。此外,宫颈病变与免疫系统疾病有关,如HIV感染等。目前HIV感染人群呈逐渐上升趋势,截至2022年年底,大约有3900万例HIV感染者,130万新发病例,63万例死于HIV相关疾病。HIV感染很大程度上会促进HPV的传播,HIV阳性患者宫颈病变发展为HSIL的概率约为HIV阴性患者的3倍[20]。同时HR⁃HPV的感染也增加了基因型脆弱性[21]。国外一项横断面研究显示[22],HIV感染与宫颈癌前病变密切相关,对于宫颈LSIL患者,HIV阳性患者比HIV阴性患者更为常见。
图2 Lactobacillus缺失介导的免疫极化与肿瘤耐药路径 该路径中,乳酸杆菌科缺乏通过诱导巨噬细胞向M2转化,削弱抗肿瘤免疫并增强治疗抵抗,与宫颈病变进展直接相关[18-19]。
2.2 代谢异常与表观遗传调控 血清中高密度脂蛋白的浓度异常以及甘油三酯的异常也被认为是宫颈癌发生的影响因素[23]。根据Frontela⁃Noda等[24]报道,血脂异常 与宫颈HSIL之间存在一定关联。国外一项研究发现[25],血清中IG⁃FBP⁃3以及甘油三酯浓度的降低可能与宫颈病变的消除有关,但目前没有明确的统计学意义。该研究数据显示,64%的宫颈LSIL患者血清中IGFBP⁃3浓度有所升高,而仅17%的患者血清甘油三酯异常。Lin等[26]推测血清胆固醇
与宫颈HSIL之间存在一定关联。国外一项研究发现[25],血清中IG⁃FBP⁃3以及甘油三酯浓度的降低可能与宫颈病变的消除有关,但目前没有明确的统计学意义。该研究数据显示,64%的宫颈LSIL患者血清中IGFBP⁃3浓度有所升高,而仅17%的患者血清甘油三酯异常。Lin等[26]推测血清胆固醇 及甘油三酯水平升高会导致机体免疫力下降以及肿瘤生长,血清总胆固醇高与宫颈LSIL有显著关系;而低高密度脂蛋白和高甘油三酯与宫颈HSIL密切相关,高甘油三酯和高低密度脂蛋白与癌性病变有关[27]。上述HPV感染特征(HPV整合、HPV病毒载量)与宿主微环境(阴道菌群、代谢)等关键影响因素,正是后续AI精准诊疗模型构建的核心数据基础。
及甘油三酯水平升高会导致机体免疫力下降以及肿瘤生长,血清总胆固醇高与宫颈LSIL有显著关系;而低高密度脂蛋白和高甘油三酯与宫颈HSIL密切相关,高甘油三酯和高低密度脂蛋白与癌性病变有关[27]。上述HPV感染特征(HPV整合、HPV病毒载量)与宿主微环境(阴道菌群、代谢)等关键影响因素,正是后续AI精准诊疗模型构建的核心数据基础。
3 人工智能驱动的精准诊疗创新
3.1 AI在筛查诊断中的应用升级 AI已广泛应用于宫颈病变诊疗的多个环节,包括宫颈细胞学筛查、阴道镜检查 、MRI图像分析、预后预测等。在宫颈细胞学筛查中,AI技术通过深度学习算法,能快速分析宫颈细胞学图像,自动识别异常细胞,显著提高了筛查效率和准确性。研究显示,AI模型在检测宫颈上皮内瘤变(CIN)2级及以上病变时,灵敏度达到90.1%,特异度为94.8%[28];在阴道镜检查中,AI辅助病变识别与定位,指导活检取材,减少漏诊;在MRI图像分析中,AI有助于判断肿瘤分期及制定治疗方案;在预后预测中,AI模型可整合多因素数据,预测患者复发风险及生存情况。此外,结合低延迟网络技术的远程诊断和自取样技术,AI辅助诊断系统能进一步简化宫颈癌筛查流程,提高筛查的可接受性和便利性。例如,基于AI的远程诊断技术可减少患者前往医疗机构的次数,尤其在资源有限的地区,能显著提高筛查覆盖率。
、MRI图像分析、预后预测等。在宫颈细胞学筛查中,AI技术通过深度学习算法,能快速分析宫颈细胞学图像,自动识别异常细胞,显著提高了筛查效率和准确性。研究显示,AI模型在检测宫颈上皮内瘤变(CIN)2级及以上病变时,灵敏度达到90.1%,特异度为94.8%[28];在阴道镜检查中,AI辅助病变识别与定位,指导活检取材,减少漏诊;在MRI图像分析中,AI有助于判断肿瘤分期及制定治疗方案;在预后预测中,AI模型可整合多因素数据,预测患者复发风险及生存情况。此外,结合低延迟网络技术的远程诊断和自取样技术,AI辅助诊断系统能进一步简化宫颈癌筛查流程,提高筛查的可接受性和便利性。例如,基于AI的远程诊断技术可减少患者前往医疗机构的次数,尤其在资源有限的地区,能显著提高筛查覆盖率。
3.2 多模态预测模型构建 近年来,随着AI和多模态数据融合技术的发展,宫颈病变的预测模型取得了显著进展。多模态预测模型的核心价值,正是将前文所述的HPV分型/载量、阴道微生态、代谢指标等分散影响因素,与医学影像、临床特征深度融合,通过AI算法实现风险的精准量化。多模态预测模型通过整合多种数据类型,包括医学影像(如阴道镜图像、MRI)、临床特征(如年龄、病史)以及实验室检测结果(如HPV分型、细胞学检查),能更全面地评估宫颈病变的风险,提高诊断的准确性和效率。研究显示,结合AI的阴道镜图像分析能有效区分宫颈LSIL和HSIL,灵敏度和特异度分别达到95.6%和83.3%[28]。此外,通过非线性支持向量机(SVM)模型,利用MRI图像预测局部晚期宫颈癌的诊断及临床分期,T2矢状图像的预测准确率最高,达到81%[29]。多模态预测模型在临床应用中展现出巨大潜力,能为宫颈病变的早期筛查和个性化治疗提供支持。未来,多模态预测模型通过扩大数据集和改进算法,提高模型的泛化能力和预测精度,同时在更多医疗机构中验证模型的有效性,并推动其在临床实践中的广泛应用,结合更多类型的数据(如基因组学、转录组学),进一步提升模型的性能。
4 临床转化与未来方向
4.1 新型标志物的临床验证 除传统危险因素外,表观遗传学改变正成为CIN研究的新焦点。这些标志物对宫颈病变的全程管理具有巨大临床潜力,有待进一步临床验证。4.1.1 DNA甲基化 DNA甲基化是表观遗传学中的一种重要机制,其通过在基因的启动子区域添加甲基化基团调控基因表达。在宫颈病变中,特定基因的甲基化状态与宫颈癌的发生、发展密切相关,包括PAX1基因甲基化、SOX1基因甲基化、ZNF582基因甲基化、DAPK1基因甲基化、HPV16基因组甲基化等。其中,PAX1、DAPK1基因甲基化在宫颈癌组织中明显增加;SOX1基因作为抑癌基因,其在宫颈癌组织中表达明显降低;而ZNF582基因甲基化在正常组织到宫颈上皮内瘤变中显著增加,而在侵袭性癌症中减少[30]。
4.1.2 MicroRNA 近年来,研究人员在探索新的分子标记物方面取得了一定进展。MicroRNA(miRNA)是一类内源性编码的长度大约为22个核苷酸的非编码单链RNA分子。在病理状态下,miRNA表达常出现失调,可与肿瘤抑制功能丧失或癌基因激活有关,进而影响癌症相关信号通路,促进低级别宫颈上皮内瘤变进展[31]。
4.1.3 LncRNA LncRNA是无编码蛋白质功能的RNA,主要在转录及转录后水平参与表观遗传调控,与人类癌症的发生、侵袭、转移等过程密切相关。张邢等[32]研究表明,lncR⁃NAs在宫颈病变的发生发展及预后中起重要作用,同时受多种基因影响。近年研究中,lncRNA有望成为宫颈病变新型标志物以及治疗靶点,但其在宫颈病变中的具体机制仍未阐明。
4.1.4 其他肿瘤标志物 目前已应用于临床的宫颈癌相关肿瘤标志物,包括鳞状细胞癌
目前已应用于临床的宫颈癌相关肿瘤标志物,包括鳞状细胞癌 抗原(SCC⁃Ag)、CA125、CA199、CEA;宫颈癌潜在肿瘤标志物,包括血管内皮生长因子(vas⁃cularendothelialgrowthfactor,VEGF)、特异性生长因子(tumorsuppliedgroupoffactors,TSGF)、骨桥蛋白(Osteopontin,OPN)、血清细胞角蛋白19片段抗原(CYFRA21⁃1)、p53、p16/Ki⁃67、COX⁃2、CD44、MMP⁃9、miRNA、TPA等。这些单一指标易受炎症或出血等影响,且在肿瘤发展不同时期表达水平有所不同。因此,联合检测多种肿瘤标志物可提高检测的敏感性与特异性[33]。
抗原(SCC⁃Ag)、CA125、CA199、CEA;宫颈癌潜在肿瘤标志物,包括血管内皮生长因子(vas⁃cularendothelialgrowthfactor,VEGF)、特异性生长因子(tumorsuppliedgroupoffactors,TSGF)、骨桥蛋白(Osteopontin,OPN)、血清细胞角蛋白19片段抗原(CYFRA21⁃1)、p53、p16/Ki⁃67、COX⁃2、CD44、MMP⁃9、miRNA、TPA等。这些单一指标易受炎症或出血等影响,且在肿瘤发展不同时期表达水平有所不同。因此,联合检测多种肿瘤标志物可提高检测的敏感性与特异性[33]。
4.1.5 HMGB3 HMGB3是一个潜在的宫颈癌前病变早期检测的分子标志物。HMGB3在宫颈病变细胞中的表达,特别是在CINI病例中,具有比传统p16标志物更高的灵敏度和特异性[34]。
4.2 技术瓶颈与突破路径 当前AI应用仍面临三大挑战:(1)数据异质性:不同医疗机构TCT制片标准差异导致模型泛化能力下降,这种数据异质性使得AI模型在跨机构应用时难以保持一致的性能,限制了其广泛应用。针对这个问题,我们可建立统一的TCT制片和数据采集标准,减少因操作差异导致的数据异质性;采用数据增强技术(如物理级、语义级增强)和多模态数据融合(结合影像、病理、基因数据),提升模型对不同数据源的适应性;通过联邦学习框架,允许不同机构在不共享原始数据的情况下联合训练模型,增强模型的泛化能力。(2)算法黑箱:深度学习决策过程缺乏医学可解释性,医生和患者难以理解AI模型是如何从复杂的医学数据中得出诊断结论,增加了诊断结果的不确定性和应用难度。因此,可利用可视化工具(如热力图)展示模型在分析医学影像时关注的区域,帮助医生理解模型的决策依据;开发如LIME(局部可解释模型无关解释)和Shapley值等工具,量化特征对模型预测结果的贡献度,提升模型的透明度;结合自上而下(基于伦理原则)和自下而上(基于案例学习)的设计方法,构建具有部分可解释性的“算法灰箱”,平衡准确性和透明度。(3)实时性不足:阴道镜AI辅助系统响应延迟达2.3s,这在临床实践中可能影响诊断效率和医生的操作体验。为此,可利用边缘计算技术,将部分计算任务分配到靠近数据源的边缘设备上,减少数据传输时间和延迟。同时,使用神经拟态芯片等高效硬件,提升系统的实时处理能力;开发轻量级的AI模型,减少模型的复杂度和计算量,从而提高响应速度;优化AI系统与阴道镜设备的集成,减少软件和硬件之间的通信延迟,确保实时反馈。
5 结语
宫颈病变的精准诊疗已进入多组学联合AI的新时代。未来研究需重点关注:(1)建立中国人群特有的风险预测模型:开展针对不同地区、不同年龄层和不同生活方式人群的宫颈病变队列研究,收集详细的临床数据、生活方式信息和生物样本;结合基因组学、转录组学、蛋白质组学和代谢组学数据,构建综合的风险预测模型。(2)致力于开发基于生物标志物检测的无创监测新方法:基于血液、尿液或其他体液的生物标志物检测方法,结合基因组学、蛋白质组学和代谢组学标志物,开发多维度的无创检测方法;利用AI技术对生物标志物检测数据进行分析和解读,提高诊断的准确性和可靠性。(3)探索AI驱动的个体化治疗决策系统,利用AI技术对患者的治疗过程进行动态监测,根据治疗反应及时调整治疗方案。总之,通过跨学科协作,构建一个集“多维度机制研究、多组学数据整合、人工智能分析”于一体的精准诊疗体系,最终实现宫颈癌从“治已病”向“治未病”的跨越式转变,为患者提供更精准、更有效的医疗服务,最终实现消除宫颈癌的目标。
参考文献略。
来源:晏玉玲,杨欢 ,王延琨,等.基于多维度机制与人工智能驱动的宫颈上皮内病变精准诊疗研究进展[J].现代妇产科进展,2026,35(01):54-57.
,王延琨,等.基于多维度机制与人工智能驱动的宫颈上皮内病变精准诊疗研究进展[J].现代妇产科进展,2026,35(01):54-57.
