
湘雅二医院盛志峰教授团队综述:抗骨吸收药物导致的非典型性股骨骨折
近日,来自中南大学湘雅二医院代谢内分泌科的盛志峰 教授团队在国际SCI期刊 Current Osteoporosis Reports(IF=5.3)发表了题为“Atypical Femoral Fractures Induced by Anti-Resorptive Medications”的综述文章。中南大学湘雅医学院李妍妍、史悦晴为文章的共同第一作者,盛志峰教授和瞿晓莉博士为文章的共同通讯作者。
教授团队在国际SCI期刊 Current Osteoporosis Reports(IF=5.3)发表了题为“Atypical Femoral Fractures Induced by Anti-Resorptive Medications”的综述文章。中南大学湘雅医学院李妍妍、史悦晴为文章的共同第一作者,盛志峰教授和瞿晓莉博士为文章的共同通讯作者。

骨质疏松 症是一种中老年人常见的,以骨量低下、骨微结构退变、骨脆性增加、易发生骨折
症是一种中老年人常见的,以骨量低下、骨微结构退变、骨脆性增加、易发生骨折 为特征的全身性代谢性骨病。目前的药物治疗主要通过抑制破骨细胞以减少骨吸收、激活成骨细胞以促进骨形成,或两者兼有。常用的抗骨吸收药物包括双膦酸盐(Bisphosphonates, BPs)和地舒单抗
为特征的全身性代谢性骨病。目前的药物治疗主要通过抑制破骨细胞以减少骨吸收、激活成骨细胞以促进骨形成,或两者兼有。常用的抗骨吸收药物包括双膦酸盐(Bisphosphonates, BPs)和地舒单抗 。这些药物通过抑制破骨细胞的形成、存活和活性,从而减少骨吸收,降低髋部和椎体骨折的风险。值得注意的是,长期抗骨吸收治疗可能伴随罕见但严重的不良反应,包括下颌骨坏死和非典型性股骨骨折(Atypical Femoral Fractures, AFFs)。
。这些药物通过抑制破骨细胞的形成、存活和活性,从而减少骨吸收,降低髋部和椎体骨折的风险。值得注意的是,长期抗骨吸收治疗可能伴随罕见但严重的不良反应,包括下颌骨坏死和非典型性股骨骨折(Atypical Femoral Fractures, AFFs)。
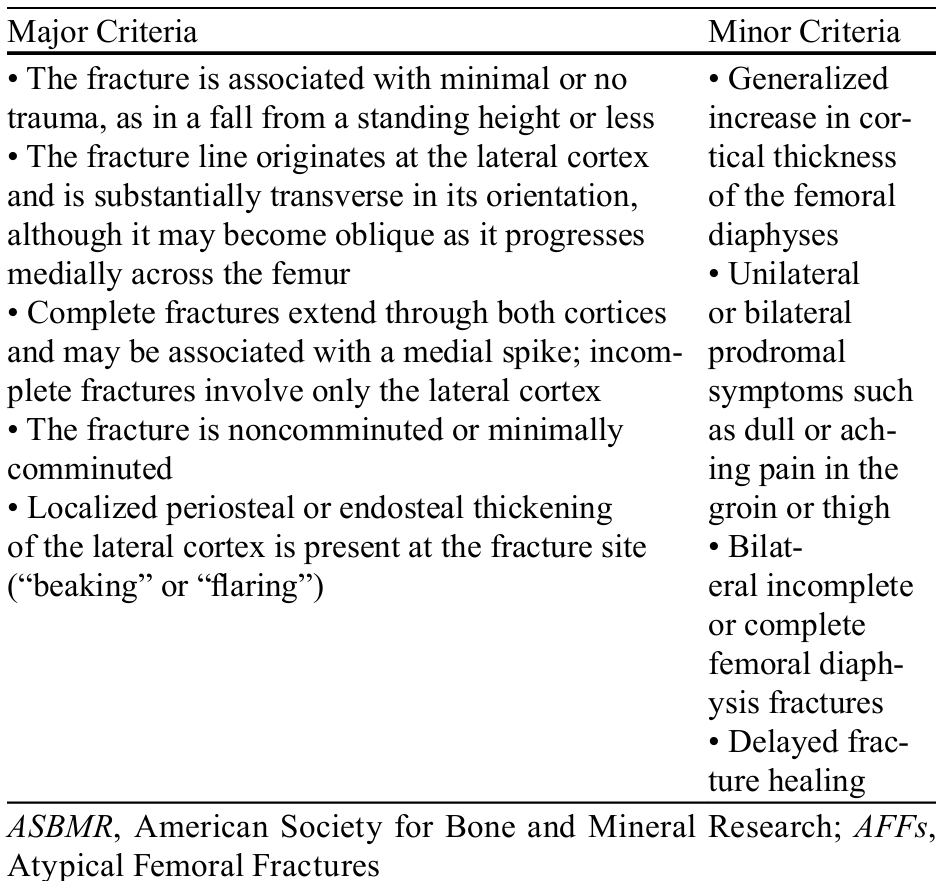
AFFs是指非创伤或轻微创伤或扭转造成的股骨转子下或股骨干骨折。根据 2013年美国骨与矿物质研究学会(American Society for Bone and Mineral Research, ASBMR)工作组的标准(表1),确诊AFFs至少需要满足五个主要标准中的四个,并排除其他骨折。次要标准支持诊断,但非诊断所必需。
表1. ASBMR工作组2013年修订的非典型性股骨骨折病例定义
Q1
非典型性股骨骨折的危险因素有哪些?
高龄:接受BPs治疗的女性患者,AFFs发病风险随年龄增长呈上升趋势,但85岁及以上患者风险有所降低,可能与该年龄段死亡率增高有关。
种族:亚洲女性是AFFs的高风险群体。在接受BPs治疗的女性队列中,亚洲女性的AFFs发生率为每年每万人5.95例,而白人女性为1.09例。
女性:基于瑞典2008-2010年数据,55岁以上接受BPs治疗的AFFs患者90%为女性,可能与女性骨骼结构(股骨更窄、骨盆更宽)及BPs较高使用率有关。
遗传易感性:LOXL4基因变异和甲羟戊酸通路突变个体风险显著增高。
药物因素:长期使用BPs(口服>5年或静脉>3年且无药物假期)、质子泵抑制剂(可能抑制骨吸收)以及高剂量/长期糖皮质激素
 ,均会增加AFFs发病风险。
,均会增加AFFs发病风险。
Q2
抗骨吸收药物导致非典型性股骨骨折的发生机制是什么?
骨重建抑制:抗骨吸收药物过度抑制破骨细胞活性,导致微损伤修复受阻,微裂纹积累,骨转换率降低。
骨材料性能下降:抗骨吸收药物虽可提高骨密度,但骨基质中矿物质沉积过多,胶原纤维排列紊乱,导致骨硬度上升但韧性下降。
股骨几何形态影响:亚洲女性特有的股骨形态(股骨颈长度较短、较大内翻角和弯曲度)使外侧皮质承受更高应力,易发生骨折(图1)。
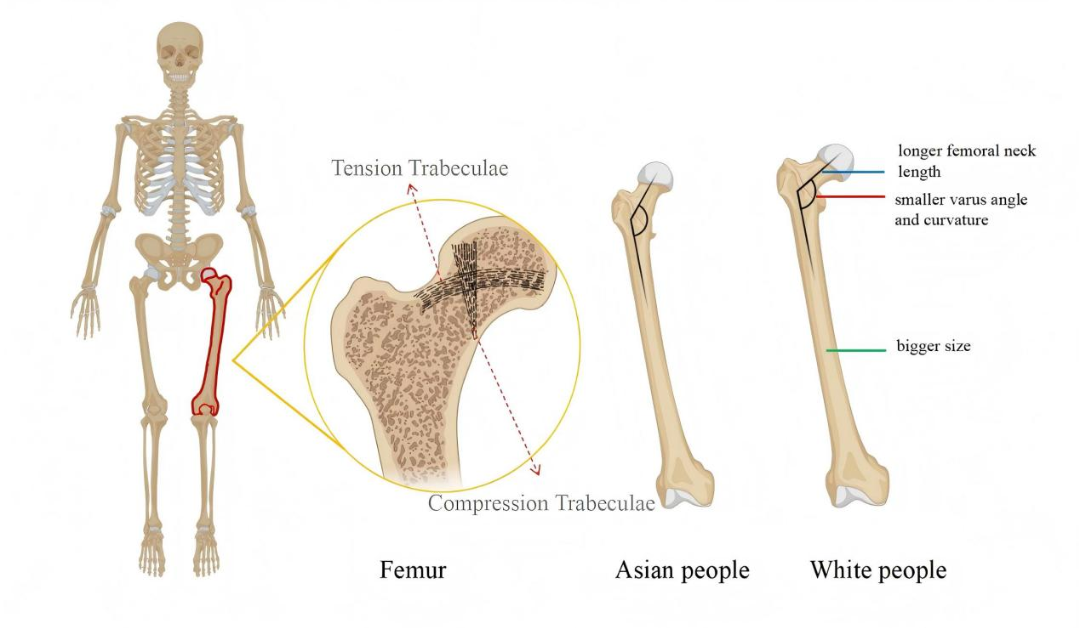
图1. 亚洲人与白人股骨几何结构示意图
Q3
不同抗骨吸收药物的最佳用药时间窗?(图2)
口服阿仑膦酸
 钠超过5年或静脉输注唑来膦酸
钠超过5年或静脉输注唑来膦酸 超过3年可能因骨重建过度抑制导致微损伤累积及AFFs风险升高,因此需通过风险-收益评估决定是否暂停治疗。低风险患者(无新发骨折、BMD稳定且骨代谢标志物CTX<0.3 ng/mL)可进入药物假期,口服制剂停药2-3年、静脉制剂停药3-5年,期间每年监测BMD,若年降幅>5%或CTX持续上升>50%需重启治疗;高风险患者(近期骨折、BMD持续下降或CTX>0.6 ng/mL)则需延长治疗至10年,并持续动态评估。
超过3年可能因骨重建过度抑制导致微损伤累积及AFFs风险升高,因此需通过风险-收益评估决定是否暂停治疗。低风险患者(无新发骨折、BMD稳定且骨代谢标志物CTX<0.3 ng/mL)可进入药物假期,口服制剂停药2-3年、静脉制剂停药3-5年,期间每年监测BMD,若年降幅>5%或CTX持续上升>50%需重启治疗;高风险患者(近期骨折、BMD持续下降或CTX>0.6 ng/mL)则需延长治疗至10年,并持续动态评估。地舒单抗通过抑制核因子κB受体激活蛋白配体(Receptor Activator of Nuclear Factor-κB Ligand, RANKL)快速降低骨吸收,但停药后骨吸收标志物CTX可在1-2个月内反弹至基线3倍以上,导致骨量快速丢失(尤其皮质骨)和椎体骨折风险骤增(第1年风险升高6.6%),因此通常不推荐药物假期,需持续治疗或停药后6个月内进行序贯治疗。高骨折风险患者(如多发性椎体骨折)停药后应首选序贯双膦酸盐,可降低椎体骨折风险46%;若存在严重骨质疏松或骨量极度低下,可替代为特立帕肽
 (疗程≤2年)。序贯治疗期间需每3个月监测BMD和CTX,若CTX持续>0.6 ng/mL或BMD下降>5%需调整方案。临床管理需强化患者教育,确保依从性以避免因停药反弹导致骨折风险失控。
(疗程≤2年)。序贯治疗期间需每3个月监测BMD和CTX,若CTX持续>0.6 ng/mL或BMD下降>5%需调整方案。临床管理需强化患者教育,确保依从性以避免因停药反弹导致骨折风险失控。
表2. 关于停用抗骨吸收药物的建议

Q4
停药后风险何时降至安全水平?
AFFs的风险与BPs的停药时间密切相关。对于未使用BPs的人群,AFFs的绝对风险极低,每年每万人仅0.03-0.07例。当BPs使用少于5年的患者停药后,AFFs发生率持续降低,停药4年以上时,发生率降至每年每万人0.1例,接近正常人群水平,此时可考虑恢复用药。然而,对于BPs使用超过5年的患者,停药1.25-4年后AFFs发生率降至最低点,即每年每万人1.91例,但仍高于未用药人群。推测长期用药者停药后难以完全恢复至正常风险水平,若继续停药,AFFs发生率可能上升。因此,建议用药超过5年的患者在停药1.25-4年时评估恢复用药的必要性。
AFFs的治疗方案涵盖基础、药物及手术三个层面(图3)。在基础治疗方面,一旦确诊AFFs,需立即停用抗骨吸收药物,并及时补充钙和维生素D
 。药物治疗上,围手术期尽早应用特立帕肽,实践表明其能有效降低骨折率、提升骨密度并改善骨结构,对有骨折史或罹患骨质疏松症的患者效果更为显著。手术治疗则需分步骤进行,首先要判断外皮质是否存在放射性骨折线;若存在,需进一步综合评估患者股骨的弯曲程度、髓腔狭窄情况、是否存在预存植入物、骨顶点骨内膜愈伤组织状况以及股骨弯曲程度等因素。对于完全性AFFs,首选髓内钉固定手术,若因特殊情况髓内钉难以插入,则选择钢板固定作为替代方案;对于不完全性AFFs,依据危险因素评估评分,评分小于7可先密切观察,评分大于8则进展为完全性AFFs的可能性较大,需进行预防性固定手术。术后要密切关注不愈合、植入物失败等常见并发症,必要时进行翻修手术。
。药物治疗上,围手术期尽早应用特立帕肽,实践表明其能有效降低骨折率、提升骨密度并改善骨结构,对有骨折史或罹患骨质疏松症的患者效果更为显著。手术治疗则需分步骤进行,首先要判断外皮质是否存在放射性骨折线;若存在,需进一步综合评估患者股骨的弯曲程度、髓腔狭窄情况、是否存在预存植入物、骨顶点骨内膜愈伤组织状况以及股骨弯曲程度等因素。对于完全性AFFs,首选髓内钉固定手术,若因特殊情况髓内钉难以插入,则选择钢板固定作为替代方案;对于不完全性AFFs,依据危险因素评估评分,评分小于7可先密切观察,评分大于8则进展为完全性AFFs的可能性较大,需进行预防性固定手术。术后要密切关注不愈合、植入物失败等常见并发症,必要时进行翻修手术。
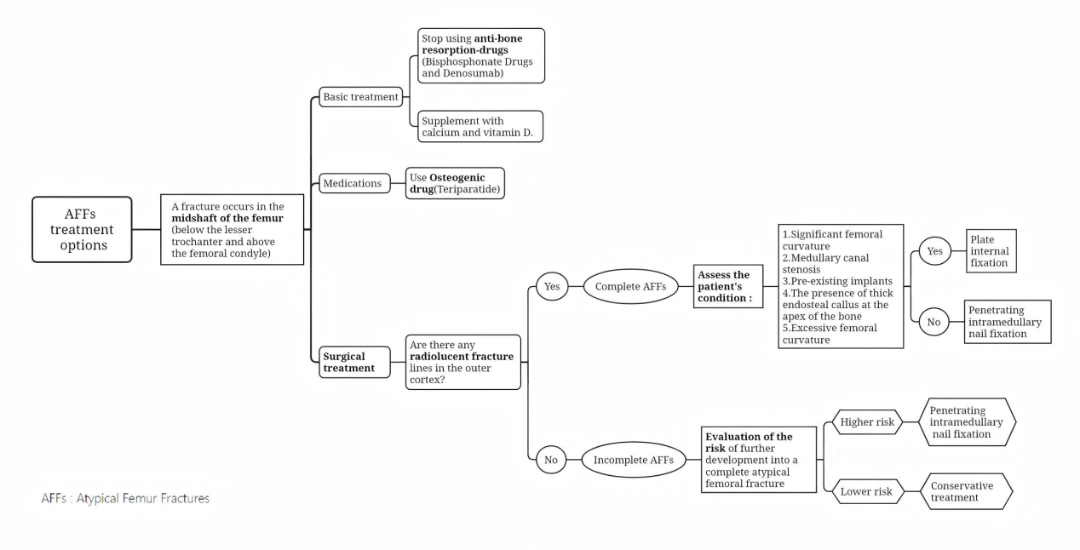
图2. 非典型性股骨骨折的治疗方案
盛志峰 教授
中南大学湘雅二医院
该综述系统总结了抗骨吸收药物导致的非典型性股骨骨折的风险因素与临床管理策略的研究进展,详细论述了药物过度抑制骨重建、微损伤累积及股骨几何形态在骨折发生中的协同作用机制,并提出了基于个体化风险评估的药物假期策略、停药后序贯治疗方案以及手术与非手术综合管理路径,为临床实践中安全、精准地应用抗骨吸收药物提供了重要指导。
值得注意的是,未来应重点研究地舒单抗的作用机制,拓展骨折的非典型部位认识,并推进新药研发与诊疗规范建立,以提升防治水平。
李妍妍
中南大学湘雅医学院临床医学八年制在读
史悦晴
中南大学湘雅医学院临床医学五年制在读
瞿晓莉
现复旦大学华山医院博士研究生在读
盛志峰教授
•主任医师,教授
•博导,博士后合作导师
•研究方向:大数据与慢性病管理(骨质疏松症)
•中南大学湘雅二医院健康管理中心主任
•湖南省智慧化慢病管理临床医学研究中心主任
•代谢性骨病湖南省重点实验室副主任
•中华医学会内分泌学分会委员
•中华医学会内分泌学分会骨代谢学组副组长
•中国医师协会内分泌代谢科医师分会第五届委员兼副总干事长
•湖南省医学会理事
•湖南省医学会内分泌专业委员会副主任委员
相关文章与链接:https://doi.org/10.1007/s11914-025-00948-9






