
2025年度糖尿病与代谢疾病领域TOP10论文揭晓,擘画健康新蓝图 | EHJ年度盘点
近期,European Heart Journal发表的年度汇总文章精选了糖尿病与代谢疾病领域2025年度10大论文,涵盖糖尿病、肥胖和心血管疾病 (CVD)领域的重大进展和趋势。不可否认,当前人群心血管-肾脏-代谢健康问题的沉重负担对CVD发病率产生深远影响。2025年度多项里程碑式试验取得重大突破,其揭示的代谢与肾脏保护效应为降低CVD不良事件及死亡率提供了全新循证依据。
(CVD)领域的重大进展和趋势。不可否认,当前人群心血管-肾脏-代谢健康问题的沉重负担对CVD发病率产生深远影响。2025年度多项里程碑式试验取得重大突破,其揭示的代谢与肾脏保护效应为降低CVD不良事件及死亡率提供了全新循证依据。
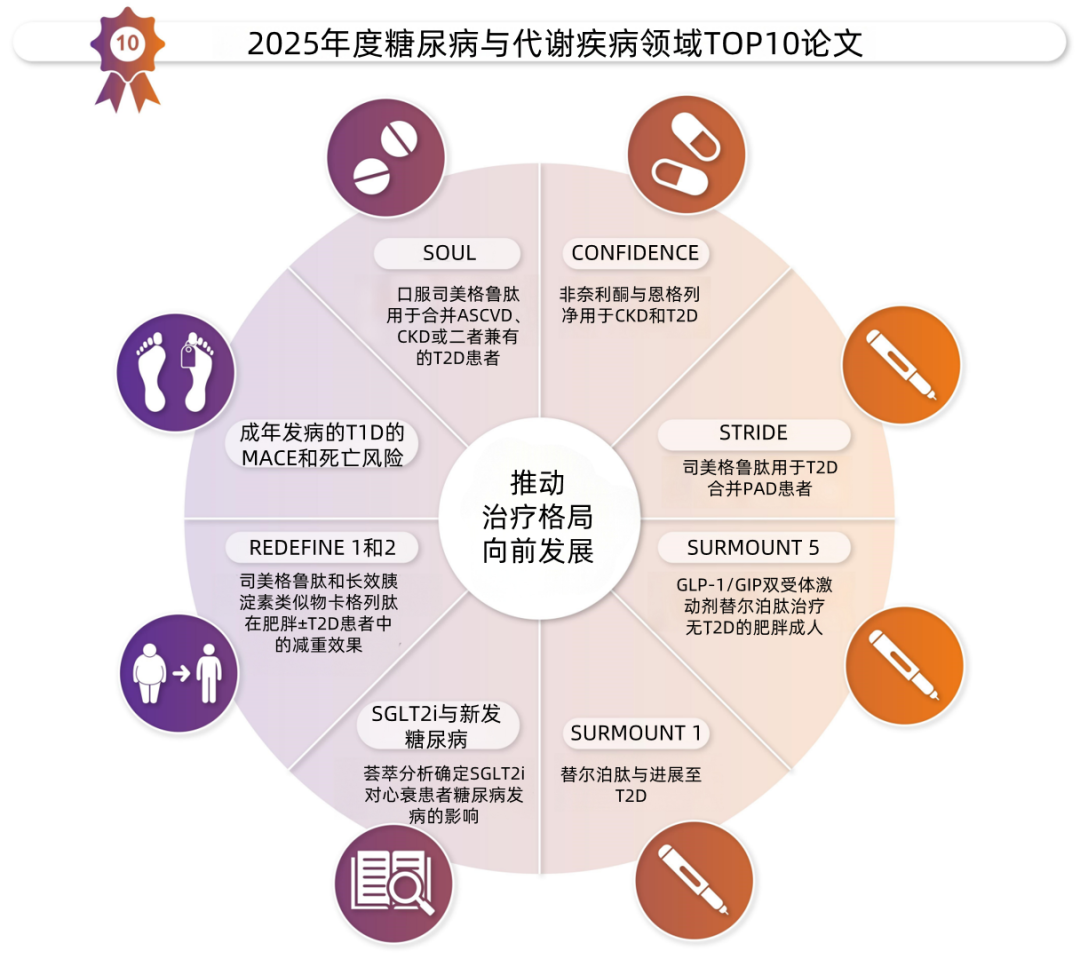
中心图
注:ASCVD,动脉粥样硬化 性心血管疾病;CKD,慢性肾脏病
性心血管疾病;CKD,慢性肾脏病 ;T2D,2型糖尿病
;T2D,2型糖尿病 ;T1D,1型糖尿病
;T1D,1型糖尿病 ;MACE,主要不良心血管事件;PAD,外周动脉疾病
;MACE,主要不良心血管事件;PAD,外周动脉疾病 。
。
 用于T2D合并ASCVD/CKD患者的心肾保护探索
用于T2D合并ASCVD/CKD患者的心肾保护探索在2型糖尿病(T2D)患者心血管风险管理领域,胰高血糖素 样肽-1受体激动剂(GLP-1 RA)和钠-葡萄糖
样肽-1受体激动剂(GLP-1 RA)和钠-葡萄糖 协同转运蛋白2(SGLT2)抑制剂已在主要临床实践指南中获IA类推荐。SUSTAIN-6研究显示,皮下注射型GLP-1 RA司美格鲁肽可显著降低心血管终点事件。为改善患者对注射治疗的顾虑,口服司美格鲁肽应运而生。PIONEER-6研究验证了口服司美格鲁肽的心血管安全性。
协同转运蛋白2(SGLT2)抑制剂已在主要临床实践指南中获IA类推荐。SUSTAIN-6研究显示,皮下注射型GLP-1 RA司美格鲁肽可显著降低心血管终点事件。为改善患者对注射治疗的顾虑,口服司美格鲁肽应运而生。PIONEER-6研究验证了口服司美格鲁肽的心血管安全性。
SOUL研究进一步探讨了口服司美格鲁肽对比安慰剂对T2D合并动脉粥样硬化性心血管病(ASCVD)和/或慢性肾脏病(CKD)患者的心肾保护作用。研究共纳入9650例T2D合并ASCVD和/或CKD患者,其中随机分配至口服司美格鲁肽组4825例、安慰剂组4825例。主要终点为心血管死亡、非致死性心肌梗死 或卒中的复合终点。中位随访47.5±10.9个月显示,口服司美格鲁肽治疗使主要不良心血管事件(MACE)相对风险降低14%(HR 0.86,95%CI 0.77–0.96;P=0.006),主要终点优效性统计假设达成。
或卒中的复合终点。中位随访47.5±10.9个月显示,口服司美格鲁肽治疗使主要不良心血管事件(MACE)相对风险降低14%(HR 0.86,95%CI 0.77–0.96;P=0.006),主要终点优效性统计假设达成。
在SOUL研究中,起始接受SGLT2抑制剂治疗的患者占27.9%,研究期间该比例升至48.9%。其预设亚组分析显示:无论是否联用SGLT2抑制剂,口服司美格鲁肽均显著降低T2D合并ASCVD和/或CKD患者的心血管终点事件风险(HR 0.86,95%CI 0.77–0.96)。该研究具有重要临床意义:为心血管风险极高危的T2D患者提供了口服剂型新选择,疗效与注射剂型相当;同时也证实与SGLT2抑制剂联合治疗的有效性与安全性。
 联合恩格列净
联合恩格列净 用于T2D合并CKD患者
用于T2D合并CKD患者CONFIDENCE研究对纳入了818例T2D合并CKD患者,旨在评估非奈利酮联合恩格列净治疗,对比单药非奈利酮或恩格列净治疗180天对尿白蛋白 /肌酐比值(UACR)的影响。主要结果显示,联合治疗组的UACR降幅,分别较恩格列净单药组高32%、较非奈利酮单药组高29%。
/肌酐比值(UACR)的影响。主要结果显示,联合治疗组的UACR降幅,分别较恩格列净单药组高32%、较非奈利酮单药组高29%。
外周动脉疾病(PAD)是T2D患者的常见合并症,会限制患者的运动能力,并影响其生活质量。此外,PAD常导致感染,甚至截肢。STRIDE研究是一项双盲、随机、安慰剂对照研究,探讨了司美格鲁肽能否改善患者症状、步行距离和生活质量。该研究共纳入792例患者,并将其随机分配接受司美格鲁肽或安慰剂治疗。主要终点为52周后最大步行距离(WD)的改善情况。结果显示,相较于安慰剂组,司美格鲁肽组总体WD增加40m,生活质量显著改善,踝关节指数(ABI)也有所改善。鉴于这些患者生活质量受损,且除西洛他唑 外无其他药物治疗,数据表明司美格鲁肽可能成为一种新的临床相关治疗选择。其改善血流动力学的具体机制有待深入探索。
外无其他药物治疗,数据表明司美格鲁肽可能成为一种新的临床相关治疗选择。其改善血流动力学的具体机制有待深入探索。
 与司美格鲁肽在肥胖治疗中的比较
与司美格鲁肽在肥胖治疗中的比较当生活方式干预未能实现充分减重效果时,联用减重药物已成为降低肥胖者心血管代谢风险的有效策略。在减重药物中,替尔泊肽通过双重激动机制,可同时模拟内源性GIP(葡萄糖依赖性促胰岛素 肽)与GLP-1 PA(胰高血糖素样肽-1受体激动剂)的作用。其中GIP激动可通过中枢途径增强饱腹感,通过外周途径延缓胃排空。
肽)与GLP-1 PA(胰高血糖素样肽-1受体激动剂)的作用。其中GIP激动可通过中枢途径增强饱腹感,通过外周途径延缓胃排空。
SURMOUNT-5研究评估了替尔泊肽与司美格鲁肽在肥胖但无T2D成人中的疗效和安全性。在这项3b期开放标签对照研究中,参与者被按1:1比例随机分配接受最大耐受剂量的替尔泊肽(10或15mg)或司美格鲁肽(1.7或2.4mg)皮下注射,每周一次,持续72周。研究结果显示,替尔泊肽组在体重减轻和腰围缩小方面优于司美格鲁肽。替尔泊肽的双重激动机制可能是其减重效果更显著的原因。评估替尔泊肽对非T2D肥胖成人心血管结局影响的SURMOUNT-MMO试验正在进行中。该研究将以更大的人群(计划入组>15000例患者)和5年随访期,提供关于肥胖且确诊ASCVD或CVD高风险患者的CVD预防数据。
在SURMOUNT-1试验的前72周(该试验的主要阶段)内,接受替尔泊肽15mg治疗的肥胖患者平均体重减轻超过20%。替尔泊肽的3年安全性和有效性结果显示,基线时为糖尿病前期的患者体重持续减轻,并可预防T2D。绝对值上,近99%接受替泽帕肽的患者未进展为糖尿病。该长效肽类双受体激动剂(GIP与GLP-1)展现出持续3年以上的显著获益及良好安全性。
心衰(HF)、其他CVD或肾脏疾病患者发生糖尿病的风险显著升高,因此,预防和延缓糖尿病成为其关键治疗目标。
一项荟萃分析旨在明确SGLT2抑制剂对全射血分数谱系HF患者及更广泛CVD/肾病 人群中新发糖尿病的影响。首先,基于DAPA-HF与DELIVER试验的个体水平数据汇总分析,评估了达格列净
人群中新发糖尿病的影响。首先,基于DAPA-HF与DELIVER试验的个体水平数据汇总分析,评估了达格列净 与安慰剂对新发糖尿病的影响。新发糖尿病定义为随机分组后随访期间新启动降糖治疗。随后,对7项心血管与肾脏临床试验进行固定效应荟萃分析,总结SGLT2抑制剂对新发糖尿病发生率的治疗效应。
与安慰剂对新发糖尿病的影响。新发糖尿病定义为随机分组后随访期间新启动降糖治疗。随后,对7项心血管与肾脏临床试验进行固定效应荟萃分析,总结SGLT2抑制剂对新发糖尿病发生率的治疗效应。
在包含5623例基线无糖尿病的HF患者的DAPA-HF和DELIVER汇总分析中:与安慰剂相比,达格列净可使新发糖尿病风险降低33%(HR=0.67,95%CI 0.49-0.91;P=0.012)。在连续LVEF各水平及各关键亚组间未发现异质性。在包含17855例受试者的7项随机对照试验中:SGLT2抑制剂可使新发糖尿病风险降低26%(HR=0.74,95%CI 0.65-0.85;P<0.001),各试验间效应保持一致。这些发现凸显了SGLT2抑制剂在心血管-肾脏-代谢健康中的关键作用。
REDEFINE 1与2研究评估了长效人胰淀素类似物卡格列肽与司美格鲁肽的复合制剂用于合并基础疾病的超重/肥胖人群的减重效果。胰淀素作为饱腹激素参与摄食、体重及血糖的中枢调节。卡格列肽可直接作用于大脑调控食欲。
REDEFINE 1研究共纳入3417例超重/肥胖患者,结果显示,从基线至第68周,复合制剂组体重较基线的平均估计变化百分比为-20.4%,安慰剂组为-3.0%(估计差值:-17.3%;95%CI -18.1 ~-16.6;P<0.001)。REDEFINE 2研究结果显示,从基线至第68周,复合制剂组体重较基线的平均估计变化为-13.7%,安慰剂组为-3.4%(估计差值:-10.4%;95%CI -11.2 ~-9.5;P<0.001)。复合制剂组胃肠道不良反应发生率较高。总体而言,该新型复合制剂在肥胖与糖尿病治疗中颇具前景,更多更大规模的临床试验正在进行中。
既往1型糖尿病(T1D)流行病学研究多聚焦于儿童和青少年,因为T1D是儿童期最常见的疾病之一。成人发病T1D患者的死亡风险和预后数据仍然缺乏。一项基于瑞典国家糖尿病登记库与全人群对照数据的研究,比较了40岁后被诊断为T1D和T2D成人患者的全因死亡率、特定原因死亡率、心血管事件及预后因素。结果显示,相较于对照组,成人发病T1D患者的死亡风险和MACE风险显著升高,但MACE风险低于T2D患者。此类患者与早发T1D具有相似的超额风险,且血糖控制较差,提示亟需优化管理策略。吸烟、糖化血红蛋白 (HbA1c)升高和肥胖是主要的预后影响因素。此外,无论确诊年龄如何,T1D患者糖尿病昏迷/酮症酸中毒死亡风险达T2D的7倍。这些发现表明,成人发病的T1D具有急性并发症与慢性并发症并存的双重负担,且危险因素数量与不良结局之间存在剂量-反应关系,凸显了尽可能全面干预多重风险因素的重要性。长效胰岛素、单受体/双受体/三受体肠促胰素类似物等新型治疗药物的出现,有望改善这一人群的临床结局。
(HbA1c)升高和肥胖是主要的预后影响因素。此外,无论确诊年龄如何,T1D患者糖尿病昏迷/酮症酸中毒死亡风险达T2D的7倍。这些发现表明,成人发病的T1D具有急性并发症与慢性并发症并存的双重负担,且危险因素数量与不良结局之间存在剂量-反应关系,凸显了尽可能全面干预多重风险因素的重要性。长效胰岛素、单受体/双受体/三受体肠促胰素类似物等新型治疗药物的出现,有望改善这一人群的临床结局。
信源:Francesco Cosentino, Nikolaus Marx, Christopher Paul Cannon, The year in cardiovascular medicine 2025: the top 10 papers in diabetes and metabolic disorders, European Heart Journal, 2026;, ehaf1125, https://doi.org/10.1093/eurheartj/ehaf1125
编辑&排版:siqili
医脉通是专业的在线医生平台,“感知世界医学脉搏 ,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

