
ECCO.26 药研新声丨真实世界证据、创新疗法与新靶点,直击IBD诊疗难点
第21届欧洲克罗恩病 和结肠炎组织大会(ECCO
和结肠炎组织大会(ECCO 2026)于2026年2月18-21日在瑞典首都斯德哥尔摩盛大召开。本次大会亮点纷呈,全方位展现了全球炎症性肠病
2026)于2026年2月18-21日在瑞典首都斯德哥尔摩盛大召开。本次大会亮点纷呈,全方位展现了全球炎症性肠病 (IBD)领域的最新科研成果,为IBD的个体化与精准化治疗提供了关键新证据。本文精选5项亮点研究,涵盖从真实世界临床实践到前沿作用机制探索的多重维度。这些研究从不同侧面推动了IBD治疗边界的拓展,勾勒出IBD精准治疗的未来方向,彰显了全球学者在攻克这一慢性炎症性疾病上的持续突破。
(IBD)领域的最新科研成果,为IBD的个体化与精准化治疗提供了关键新证据。本文精选5项亮点研究,涵盖从真实世界临床实践到前沿作用机制探索的多重维度。这些研究从不同侧面推动了IBD治疗边界的拓展,勾勒出IBD精准治疗的未来方向,彰显了全球学者在攻克这一慢性炎症性疾病上的持续突破。
要点一览

接受非戈替尼(Filgotinib)治疗的溃疡性结肠炎患者在至第24周的真实世界皮质类固醇使用情况:前瞻性观察性研究(GALOCEAN研究)的中期分析
摘要编号:DOP036
非戈替尼(Filgotinib,FIL)是一种口服选择性Janus激酶1抑制剂(每日一次),已被批准用于治疗中度至重度活动性溃疡性结肠炎(UC)成人患者(欧盟)。在2b/3期SELECTION试验中,FIL在UC患者中显示出皮质类固醇(CS)节约效应。本研究旨在描述接受FIL治疗的UC患者在真实世界中的全身性CS使用情况。
GALOCEAN是一项正在进行的欧洲多中心、前瞻性、观察性研究,纳入在常规治疗中接受FIL治疗的溃疡性结肠炎成人患者;本次中期分析报告了截至第24周(W24)的数据。分析了基线(BL)时使用CS(FIL+CS组)或不使用CS(FIL–CS组)并接受FIL治疗患者的基线特征、FIL治疗期间全身性CS使用情况以及至第24周的有效性结局。在基线、第10周(W10)和第24周评估的有效性结局包括部分梅奥诊所评分(pMCS)、两项患者报告结局(PRO2)评分以及达到pMCS或PRO2缓解的患者比例。
截至2025年1月15日,353例入组患者有基线数据;分别有253例和164例患者有第10周和第24周数据。在基线时,CS使用率较低;FIL+CS组和FIL–CS组分别有93例(26.3%)和260例(73.7%)患者。基线特征见表1。
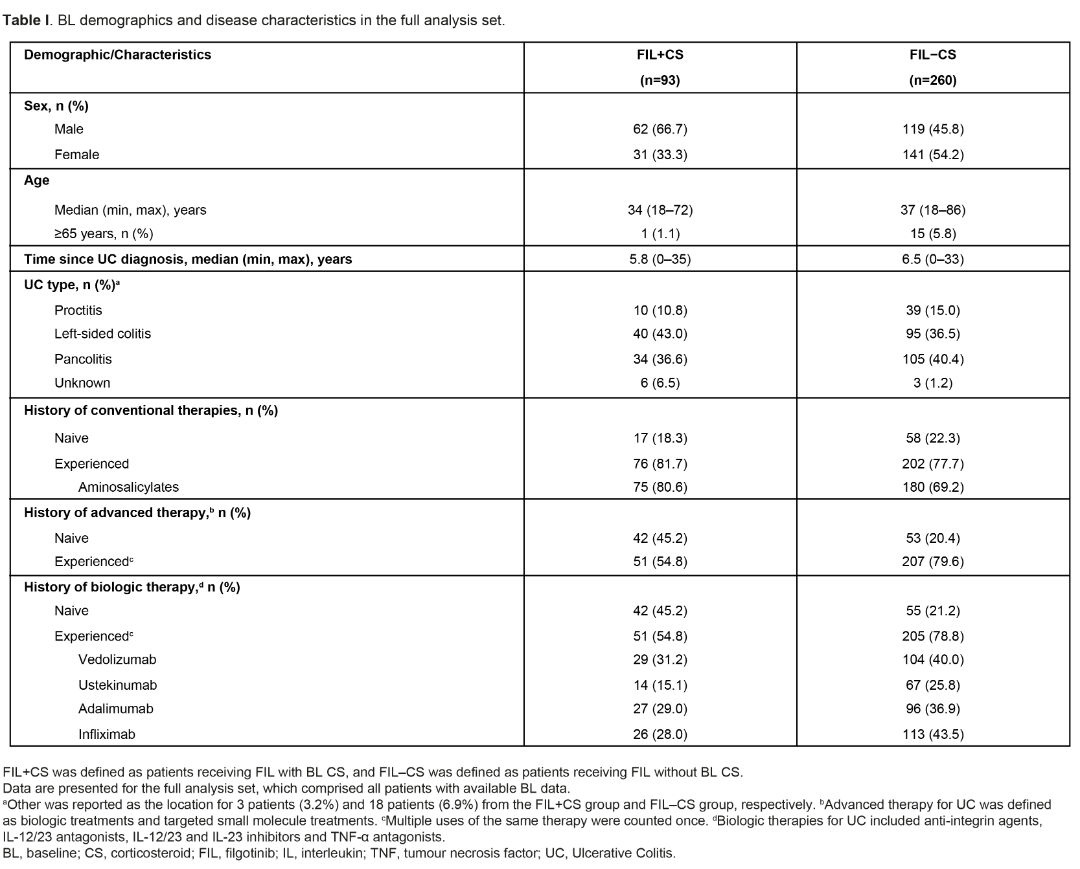
与FIL–CS组相比,FIL+CS组男性比例更高(66.7% vs 45.8%),既往使用过5-氨基水杨酸 类药物的患者更多(80.6% vs 69.2%),但既往接受过先进疗法的患者较少(54.8% vs 79.6%)。
类药物的患者更多(80.6% vs 69.2%),但既往接受过先进疗法的患者较少(54.8% vs 79.6%)。
在FIL+CS组中,第10周使用CS的患者比例从基线降至59.4%(41/69),第24周时降至46.5%(20/43)。FIL–CS组中有少数患者在第10周(8/180,4.4%)和第24周(3/88,3.4%)使用了CS(图1)。
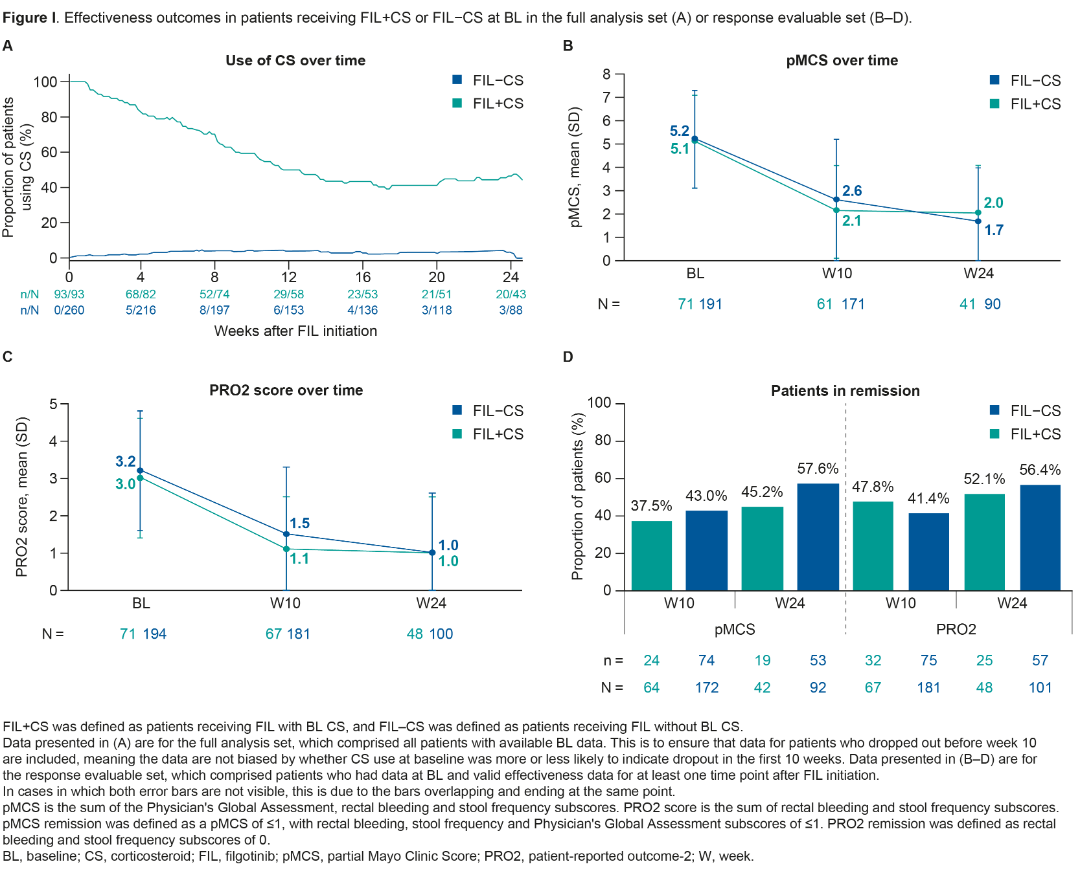
在FIL+CS组和FIL–CS组中,均观察到第10周和第24周pMCS和PRO2评分较基线改善(图1)。此外,FIL+CS组第10周达到pMCS缓解的患者比例为37.5%(24/64),第24周增加到45.2%(19/42);FIL–CS组第10周这一比例为43.0%(74/172),第24周增加到57.6%(53/92)。PRO2缓解方面也观察到相似的情况(图1)。
这项真实世界分析表明,在基线时使用CS的少数UC患者中,超过一半在启动FIL治疗后第24周不再使用CS。无论基线时是否使用CS,患者在接受FIL治疗后症状均得到缓解,并且临床症状随时间推移而改善。这些发现支持FIL治疗为患者提供了减少CS或最低剂量使用CS的机会,这与SELECTION试验的结果一致。
评估AVB-114治疗持续性克罗恩病肛瘘的随机、等待列表对照STOMP2试验的扩展初步分析
摘要编号:DOP008
STOMP2试验旨在确定可植入自体细胞疗法AVB-114是否对持续性克罗恩病肛瘘患者是一种有效的附加疗法。试验设计纳入了等待列表对照(WLC)要素,允许在第一部分研究中完成9个月主要终点随访、符合条件的对照组受试者在第二部分研究中申请接受AVB-114治疗,以加强对AVB-114安全性和有效性的评估。
符合条件的患者需有单一的肛周瘘管,且既往治疗失败或有记录显示对生物制剂或常规克罗恩病(CD)治疗药物不耐受。来自美国14个中心的受试者按1:1比例随机分配至标准治疗组(SoC;包括挂线放置在内的瘘管优化治疗)或AVB-114植入组。
主要终点是第9个月时联合瘘管缓解,定义为MRI上无>2cm的积液、外部开口肉眼可见闭合,以及手指轻压无液体流出。使用第一部分研究完整数据和所有可用的第二部分研究数据,通过逻辑回归模型(基于暴露时间,至9个月)来估计AVB-114的综合有效性。
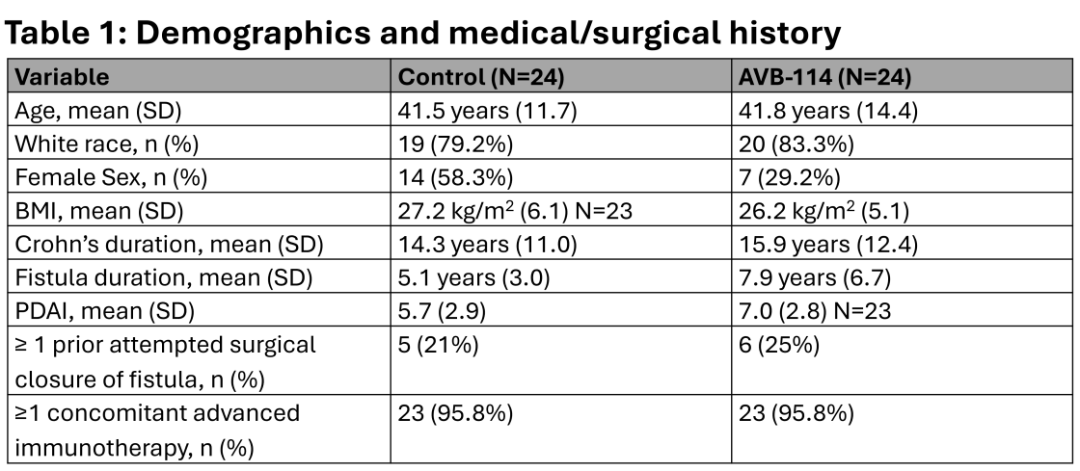
第一部分研究(采用无应答者填补法)的联合缓解率:SoC组为8.3%(2/24),AVB-114组为45.8%(11/24)(差异38%,95% CI:11-60%,post-hoc p值0.0078)。20例SoC组受试者在第二部分研究中接受了AVB-114治疗。第二部分研究中有第9个月联合缓解数据的9例受试者中,有4例(44.4%)达到联合瘘管缓解。没有受试者在第9个月的放射学缓解(主要终点的第一个组成部分)上失败,因此临床缓解(后两个组成部分的复合终点)相当于联合缓解。
在第一部分和第二部分(迄今为止)研究中,AVB-114治疗的临床缓解率相似,两部分数据合并后在覆盖范围相同的前提下得到了更窄的估计值(图1)。SoC组、第一部分AVB-114组和第二部分AVB-114组的第9个月肛周疾病活动指数(PDAI)评分平均值(标准差)分别为5.0(2.6)、4.1(2.9)和3.8(3.5)。较低的第9个月评分以及较基线下降与临床缓解率增加独立相关。
研究中发生了2例严重的治疗期出现的不良事件(TEAEs;假性息肉病和直肠痛),后者归因于AVB-114。非严重的产品相关TEAE主要与术后肛周疼痛有关。2例2级(中度)蜂窝织炎和腹壁脓肿不良事件归因于脂肪组织采集。
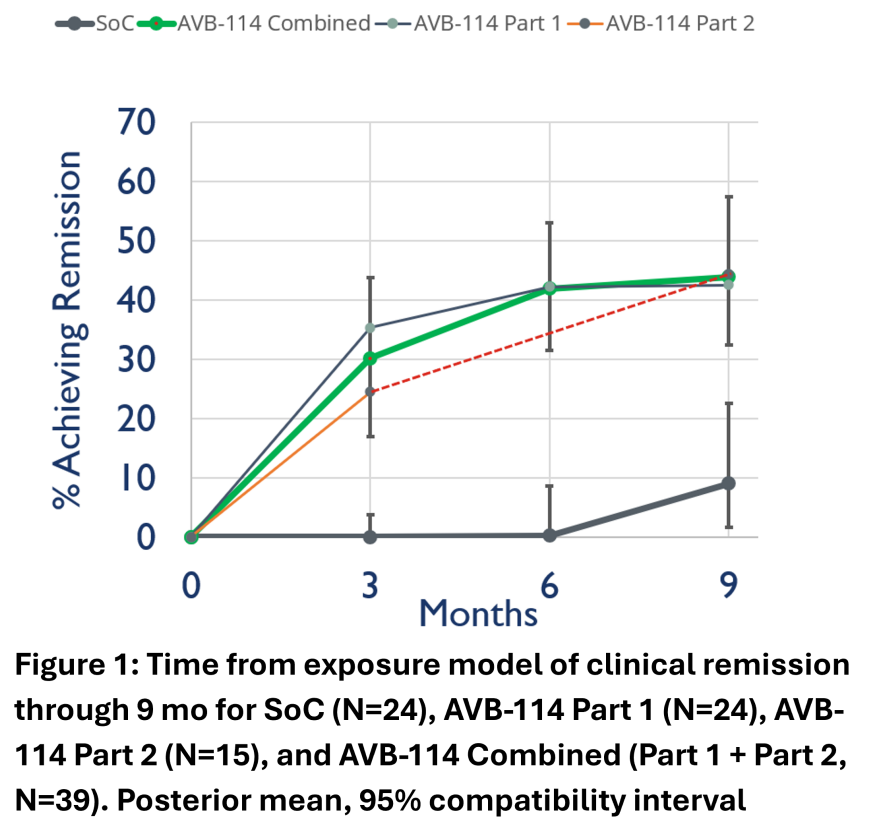
随机和联合(all-treated)分析均证明,在这一具有挑战性的患者群体中,AVB-114在9个月内具有显著疗效,不良事件在预期之内,通常轻微且不常见。
STENOVA试验结果:一项评估Ontunisertib(AGMB-129)在纤维狭窄性克罗恩病患者中安全性、药代动力学和药效学的2a期、随机、安慰剂对照、双盲研究
摘要编号:OP20
Ontunisertib是一种口服、胃肠道限制性ALK5抑制剂,用于治疗纤维狭窄性克罗恩病(FSCD),可有效阻断关键的促纤维化TGFβ通路信号传导。到目前为止,全身性ALK5抑制剂的研发一直受到全身性(尤其是心脏)毒性的阻碍。Ontunisertib可实现较高的局部胃肠道暴露,同时通过高首过肝脏代谢避免临床相关的全身暴露。STENOVA是首个在FSCD患者中进行的随机、安慰剂对照临床试验,本次报告完成了12周安慰剂对照治疗期的初步分析结果,一项开放标签治疗扩展研究正在进行中。
纳入有症状且至少有一处回肠狭窄(经MRE证实)的FSCD成年患者,按照1:1:1比例随机分配接受Ontunisertib 200mg BID、100mg QD或安慰剂(PBO)治疗12周。主要目的是评估安全性和耐受性。血浆PK评估被列为次要目标。探索性结局包括回肠和结肠黏膜药代动力学、SES-CD变化以及基于MRE的狭窄参数变化。
主要分析包括103例参与者(Ontunisertib 200mg组/100mg组/安慰剂组分别为34例/34例/35例),其中92例完成了治疗期。各组基线特征具有可比性(表)。
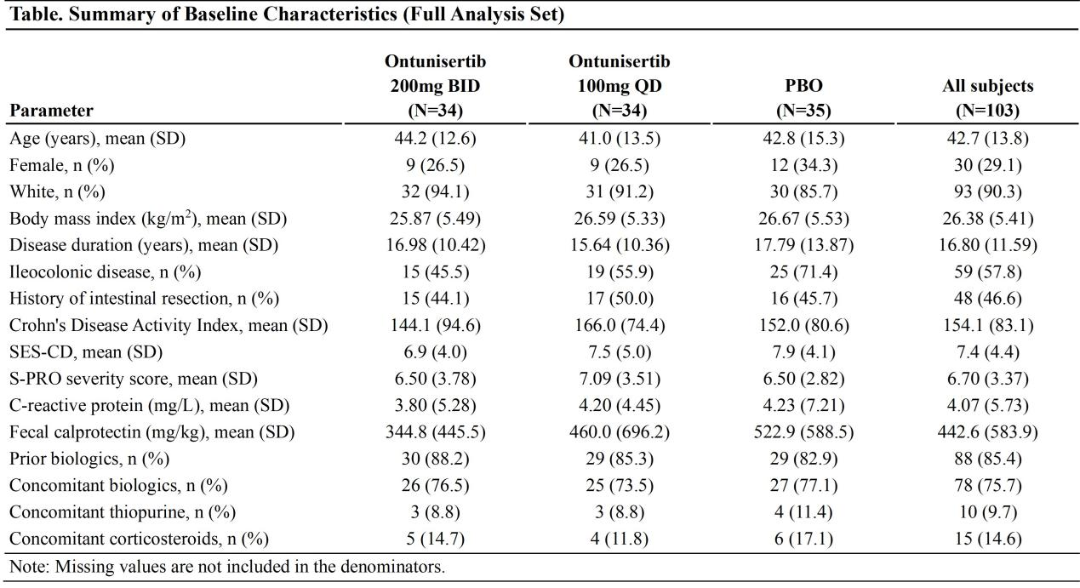
两种剂量的Ontunisertib总体耐受性良好。在Ontunisertib 200mg BID组、100mg QD组和安慰剂组中,至少发生1次TEAE的患者比例分别为61.8%、64.7%和71.4%。Ontunisertib 200mg BID组、100mg QD组和安慰剂组严重不良事件(SAE)数量分别为4、0和4。在实验室检查、生命体征、体格检查和心脏参数(包括心电图 和超声心动图
和超声心动图 )方面,未发现与治疗相关的安全性信号。
)方面,未发现与治疗相关的安全性信号。
研究观察到Ontunisertib的全身性暴露较低,但无活性主要代谢物MET-158的暴露较高。证实了回肠和结肠中Ontunisertib的高暴露。
与安慰剂相比,Ontunisertib 200mg BID组的SES-CD显示出更高的内镜应答和缓解率,这一获益由炎症与狭窄组分的同步改善所驱动,同时不可通过的狭窄转为可通过的比例更高。与安慰剂相比,Ontunisertib两个剂量组在MRE上均呈现积极改善趋势,主要在狭窄长度方面。在梗阻症状方面未发现显著差异。
两种剂量的Ontunisertib治疗12周的总体耐受性良好。研究证实了Ontunisertib的胃肠道限制性药物分布特征。同时观察到内镜和MRE结局呈现改善趋势。数据提示,Ontunisertib有望成为首个适用于人体长期给药的ALK5抑制剂,可能为FSCD患者提供新的治疗选择。
首个选择性阻断白介素-23受体的靶向口服肽Icotrokinra可减轻溃疡性结肠炎患者的全身和组织炎症负荷:ANTHEM-UC研究结果
摘要编号:OP29
Icotrokinra是首个选择性阻断白介素-23受体(IL-23R)并精确抑制IL-23通路的靶向口服肽。ANTHEM-UC是一项针对中度至重度活动性UC成人患者的2b期、随机、双盲、安慰剂对照、剂量范围研究,所有剂量的Icotrokinra均达到了第12周(W12)临床应答的主要终点,并在关键次要终点上实现了具有临床意义的改善,这些改善在第28周(W28)得以维持或进一步增加。本次,研究者报告了Icotrokinra对UC全身和组织炎症负荷生物标志物的影响。
将参与者按照1:1:1:1的比例随机分配接受Icotrokinra 100mg、200mg、400mg或安慰剂治疗,每日一次。采用临床炎症生物标志物、C反应蛋白(CRP)和粪便钙 卫蛋白(FCP),以及血清IL-23通路生物标志物(IL-22、IL-17A和IL-17F)来确定Icotrokinra对全身炎症的影响;采用结肠活检中的基因表达变化来确定组织IL-23通路的参与以及Icotrokinra对组织炎症的抑制作用。
卫蛋白(FCP),以及血清IL-23通路生物标志物(IL-22、IL-17A和IL-17F)来确定Icotrokinra对全身炎症的影响;采用结肠活检中的基因表达变化来确定组织IL-23通路的参与以及Icotrokinra对组织炎症的抑制作用。
在第12周主要时间点,所有剂量的Icotrokinra均降低了血清CRP和FCP水平(图1)。与基线相比,所有剂量的Icotrokinra(而非安慰剂)均显著降低了第12周时血清IL-22、IL-17A和IL-17F水平。与100mg剂量相比,Icotrokinra 200mg和400mg剂量组观察到IL-23通路激活的血清生物标志物有更大的降低(图1,nominal p<0.05)。
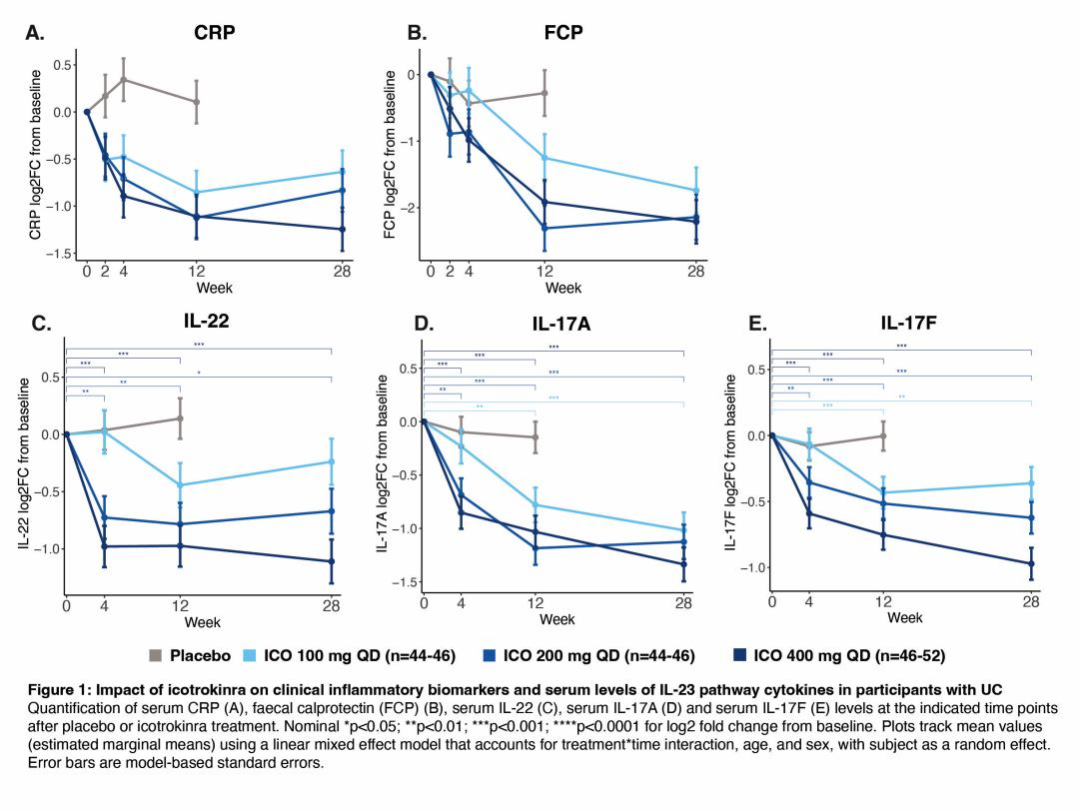
所有剂量的Icotrokinra(而非安慰剂)在第12周时均显著降低了组织中与IL-23驱动炎症相关的基因集表达(图2,nominal p<0.0001)。经Icotrokinra治疗后,组织转录组更接近于健康个体,与UC相关炎症细胞类型有关的基因组表达降低,而健康上皮细胞特征基因表达增加。重要的是,Icotrokinra对全身和组织炎症的抑制作用在第28周时持续存在(图1和图2)。
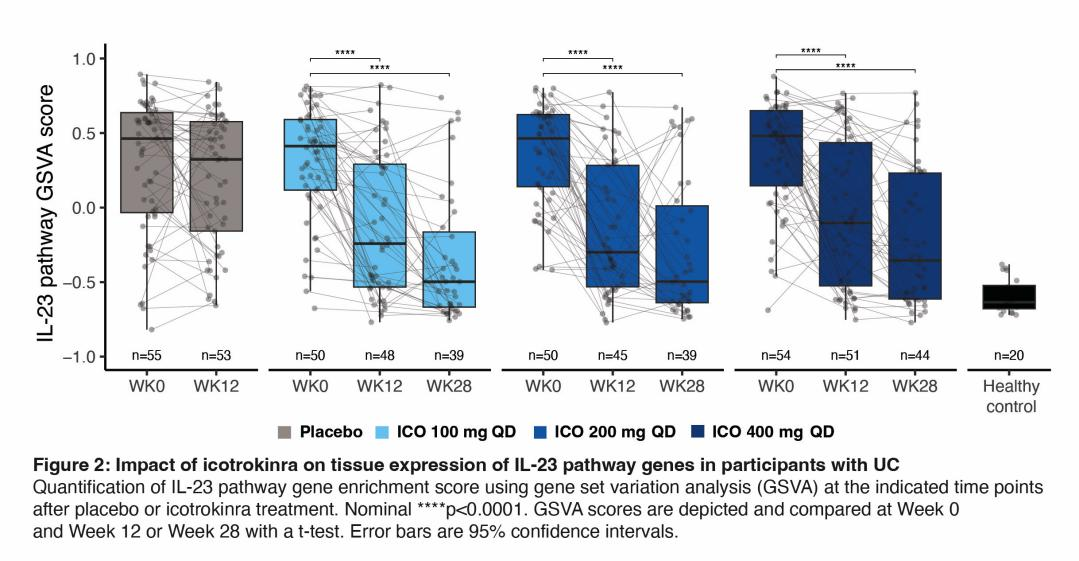
本研究首次证明阻断IL-23R可以抑制溃疡性结肠炎患者中IL-23介导的炎症信号传导。在UC中,Icotrokinra治疗可带来全身和组织炎症负荷生物标志物的持续降低(第28周)。此外,Icotrokinra诱导的转录组改变与抑制IL-23驱动的炎症和组织转录组正常化是一致的。虽然所有每日一次剂量的Icotrokinra均减轻了全身和组织炎症,但200mg和400mg剂量在减轻全身炎症负荷方面效果更显著。
TL1A/IL-23双特异性抗体治疗免疫介导的炎症性疾病的临床前评价
摘要编号:DOP122
细胞因子网络失调是免疫介导炎症性疾病(IMIDs,如IBD和银屑病)的主要驱动因素。TL1A和IL-23是这些病理过程中的关键细胞因子。TL1A促进Th1/Th17分化和成纤维细胞活化,导致纤维化和慢性炎症;IL-23维持致病性Th17细胞并驱动组织损伤。TL1A和IL-23双重抑制剂可能通过破坏互补的炎症通路产生协同效应。本次报告描述了ALX001的设计和临床前评价,ALX001是一种靶向TL1A和IL-23的人源化双特异性抗体(bsAb),旨在增强其IMIDs治疗效力。
通过竞争性ELISA表征靶点结合活性。分别在TF-1细胞凋亡和IL-23报告细胞测定中评估ALX001对TL1A和IL-23信号通路的阻断活性。通过测量人外周血单个核细胞(PBMCs)中IL-17/IL-22的释放来评估双靶点抑制的协同效应。在TNBS诱导的结肠炎模型和细胞因子诱导的银屑病模型中评估体内疗效,检测疾病活动指数(DAI)、组织病理学和细胞因子水平。在非人灵长类动物(NHPs)中测定单次给药后的药代动力学(PK)特征。
ALX001是一种具有“2+2”对称型的双特异性抗体。ALX001表现出与TL1A(KD<0.1nM)和IL-23(KD<0.01nM)的高亲和力结合,特异性阻断DR3而不影响DcR3。它抑制TL1A诱导的TF1细胞凋亡和IL-23诱导的信号传导,效力与参考单克隆抗体(mAbs)相当。
在小鼠结肠炎模型中,ALX001降低了DAI评分,减少了隐窝丢失,并抑制了黏膜细胞因子,效果优于单抗。在人外周血单个核细胞和小鼠银屑病模型中,观察到ALX001对细胞因子释放(INF-γ,IL-17,IL-22)的协同抑制作用,并伴有表皮厚度降低和IL-17A分泌减少。在非人灵长类动物的药代动力学研究中,该双特异性抗体具有较长的半衰期。
TL1A/IL-23双特异性抗体可同时中和两种主要的炎症调节因子,显示出优于单药治疗的临床前疗效。研究证实其存在机制协同作用,并可有效缓解肠道与皮肤炎症。该抗体具有良好的药代动力学特征,支持延长给药间隔,这对慢性免疫介导的炎症性疾病患者而言是一个关键优势。上述发现支持进一步研发ALX001用于治疗IMIDs。
