
从困境到希望:锁定EGFR-TP53共突变NSCLC,TOP研究的破局之道
引言
EGFR酪氨酸激酶抑制剂(EGFR-TKI)的出现重塑了EGFR突变非小细胞肺癌 (NSCLC)的治疗格局。然而,临床实践中依然存在一部分患者,即便接受了标准的EGFR-TKI治疗,其临床获益仍未达预期,甚至出现快速的耐药进展。深入的基因组学研究揭示,肿瘤内在的基因异质性,特别是共存驱动基因突变,是导致这一困境的关键1,2。其中,TP53基因的共存突变尤为突出,它不仅是频率较高的共存突变,更是界定一个预后不良、具有更高耐药潜能的高风险NSCLC亚群的重要生物标志物2,3。本文将梳理EGFR-TP53共突变特点、临床诊疗现状以及研究进展,并解析即将登陆欧洲肺癌大会(ELCC)的TOP研究。
(NSCLC)的治疗格局。然而,临床实践中依然存在一部分患者,即便接受了标准的EGFR-TKI治疗,其临床获益仍未达预期,甚至出现快速的耐药进展。深入的基因组学研究揭示,肿瘤内在的基因异质性,特别是共存驱动基因突变,是导致这一困境的关键1,2。其中,TP53基因的共存突变尤为突出,它不仅是频率较高的共存突变,更是界定一个预后不良、具有更高耐药潜能的高风险NSCLC亚群的重要生物标志物2,3。本文将梳理EGFR-TP53共突变特点、临床诊疗现状以及研究进展,并解析即将登陆欧洲肺癌大会(ELCC)的TOP研究。
TP53基因位于17号染色体 短臂(17p13.1),其编码的p53蛋白
短臂(17p13.1),其编码的p53蛋白 在维持基因组稳定性和调控细胞应激反应中发挥核心作用。在细胞损伤时,p53通过调控细胞周期停滞、凋亡、衰老和DNA修复等一系列过程来维持基因组稳定。然而,TP53的突变不仅会导致蛋白功能丧失,破坏基因组稳定性并抑制凋亡;还可能获得异常的“功能增益”,加速肿瘤的进展与治疗耐药2, 4。
在维持基因组稳定性和调控细胞应激反应中发挥核心作用。在细胞损伤时,p53通过调控细胞周期停滞、凋亡、衰老和DNA修复等一系列过程来维持基因组稳定。然而,TP53的突变不仅会导致蛋白功能丧失,破坏基因组稳定性并抑制凋亡;还可能获得异常的“功能增益”,加速肿瘤的进展与治疗耐药2, 4。
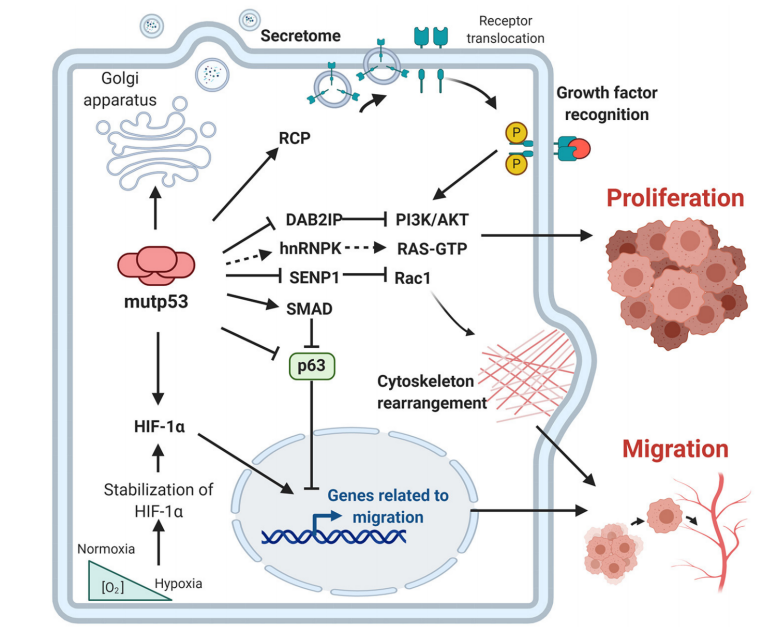
图1. 突变型p53的功能增益对增殖、侵袭及转移的影响4
TP53是EGFR突变患者群体常见的共存突变,前瞻性研究显示EGFR-TP53共突变的发生率高达40%-63.9%5。基于2979例EGFR突变患者的Meta分析证实,TP53突变是EGFR突变NSCLC预后不良因素:TP53突变患者的总生存期(OS)较TP53野生型患者更差(HR=1.73,95%CI:1.22-2.44,p=0.002)6。
不仅如此,TP53突变可通过多种途径介导对EGFR-TKI的耐药,包括破坏DNA损伤修复、诱导基因组不稳定性以加速耐药克隆进化,以及激活PI3K/AKT、mTOR等旁路信号通路,从而绕过被TKI抑制的EGFR信号轴,维持肿瘤细胞存活与增殖7。一项收集了157例EGFR-TKI经治NSCLC患者数据研究显示,相较TP53野生型组患者,EGFR-TP53共突变预后显著更差(无进展生存期[PFS]:6.5个月vs. 14.0个月,p=0.025;OS:28.0个月vs. 52.0个月,p=0.023)8。此外,研究显示,无论患者使用何种代际EGFR-TKI,TP53-EGFR共突变患者的PFS与OS均更短5。
EGFR-TP53共突变与EGFR突变NSCLC患者的不良预后密切相关,因此精准锁定EGFR-TP53共突变人群并给予针对性治疗显得尤为重要。目前,二代测序(NGS)是检测TP53突变的主要技术手段。基于扩增子的NGS测序虽因流程简化、所需DNA量少而广泛应用,但在低频突变识别方面相对有限,而基于杂交捕获的NGS方法因基因覆盖度广、灵敏度较高,在突变检出完整性方面表现更优9。
令人遗憾的是,虽然TP53突变检测已相对成熟,但针对这一高危人群目前尚无大型前瞻性证据,其治疗仍以EGFR-TKI单药为基础,临床决策长期缺乏高级别循证医学证据。为突破这一治疗瓶颈,研究者积极探索联合治疗策略。FLAURA2探索性分析结果显示,对于基线存在TP53共突变这一预后不良因素的患者,奥希替尼 联合化疗对比奥希替尼单药显示出获益趋势(PFS HR 0.57 [95% CI 0.29, 1.12];OS HR 0.71 [95% CI 0.40, 1.27])10,11。
联合化疗对比奥希替尼单药显示出获益趋势(PFS HR 0.57 [95% CI 0.29, 1.12];OS HR 0.71 [95% CI 0.40, 1.27])10,11。
为进一步在更大规模、更严格设计的临床框架中验证联合化疗策略在该分子亚型中的价值,一项专门针对TP53-EGFR共突变人群的Ⅲ期随机对照研究(TOP研究)已正式启动12。该研究采用开放标签、随机对照设计,以研究者评估的PFS(RECIST 1.1)为主要终点,在未经治的EGFR-TP53共突变非鳞状NSCLC患者中比较奥希替尼联合化疗对比奥希替尼单药的疗效和安全性,研究依据PS评分、脑转移状态及EGFR突变类型(19del vs L858R)进行分层随机。该研究结果即将于2026年3月25日,在欧洲肺癌大会(ELCC)的优选论文环节(proffered paper session)上首次公布,期待这一专门针对共突变人群设计的Ⅲ期研究能为该类患者的治疗策略优化提供重要指引!
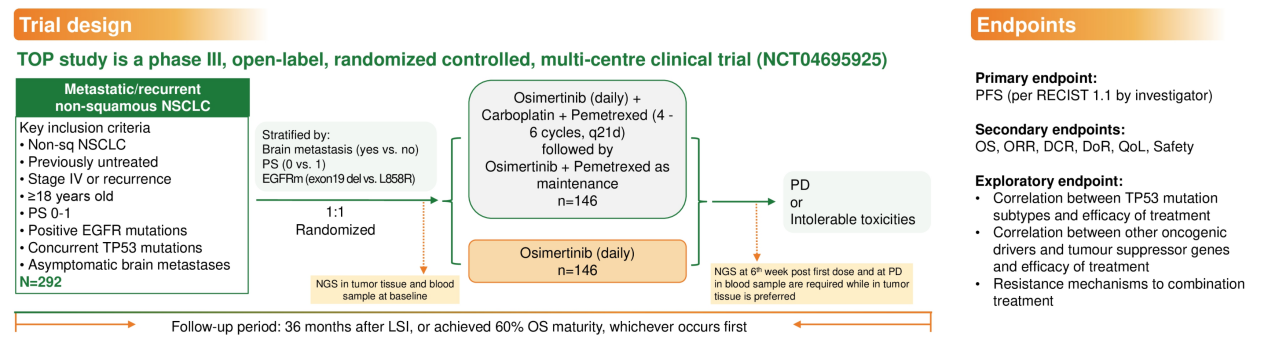
图2. TOP研究设计
审批编号:CN-179055
有效期至:2026-05-24
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
