
背着“书包”去透析?中国团队Nature发文:无透析液可穿戴人工肾问世
慢性肾脏病 及终末期肾病
及终末期肾病 具有较高发病率与死亡率。肾功能受损可导致体内水分及尿毒症
具有较高发病率与死亡率。肾功能受损可导致体内水分及尿毒症 毒素蓄积,进而引发一系列病理生理紊乱。当前终末期肾病常用疗法为血液透析与血液透析滤过
毒素蓄积,进而引发一系列病理生理紊乱。当前终末期肾病常用疗法为血液透析与血液透析滤过 ,需依赖大型设备,且患者每周需赴院3-4次。与天然肾脏持续维持体液稳态相比,此间歇性治疗模式严重影响生活,不仅耗时费力,还会增加心血管并发症风险。
,需依赖大型设备,且患者每周需赴院3-4次。与天然肾脏持续维持体液稳态相比,此间歇性治疗模式严重影响生活,不仅耗时费力,还会增加心血管并发症风险。
近期,电子科技大学邓旭、王德辉 教授团队联合四川大学等机构,在《Nature Chemical Engineering》发表突破性研究成果,开发出一种无透析液的可穿戴人工肾脏原型机器(图1)。该装置采用基于蒸汽驱动的液-气相变技术进行血液净化以去除水分,并结合吸附功能清除尿毒症毒素。该系统水清除通量达约7 ml/min/m²,并已在急性肾损伤
教授团队联合四川大学等机构,在《Nature Chemical Engineering》发表突破性研究成果,开发出一种无透析液的可穿戴人工肾脏原型机器(图1)。该装置采用基于蒸汽驱动的液-气相变技术进行血液净化以去除水分,并结合吸附功能清除尿毒症毒素。该系统水清除通量达约7 ml/min/m²,并已在急性肾损伤 兔模型中成功实施肾脏替代治疗,有效清除了水分、肌酐和β2-微球蛋白。该原型目前重量低于3.8 kg,具备进一步优化潜力,验证了便携式血液净化的可行性,为肾病治疗开辟了新途径。
兔模型中成功实施肾脏替代治疗,有效清除了水分、肌酐和β2-微球蛋白。该原型目前重量低于3.8 kg,具备进一步优化潜力,验证了便携式血液净化的可行性,为肾病治疗开辟了新途径。

图1 可穿戴人工肾(WAK)装置的便携可穿戴展示
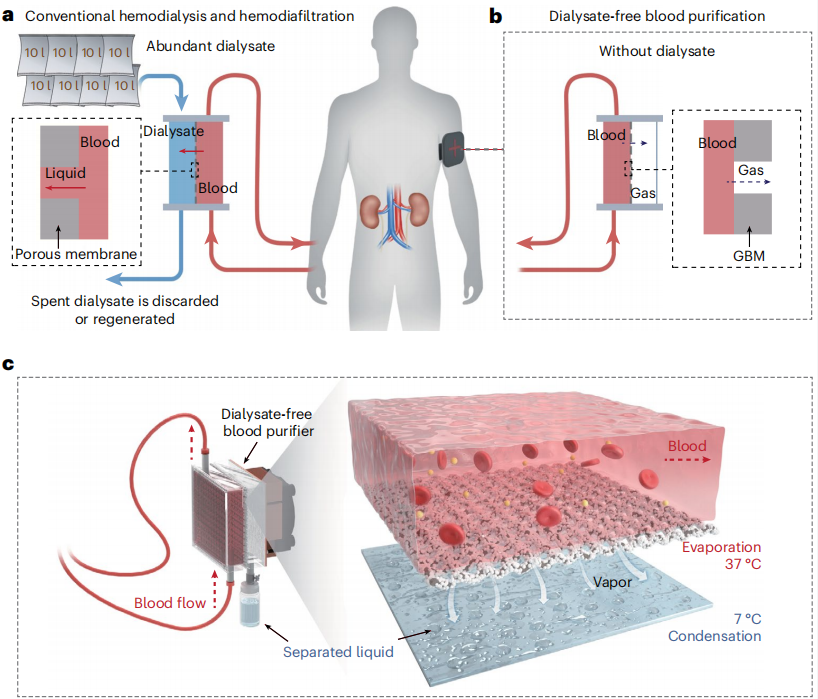
图2 无透析液可穿戴人工肾(WAK)设计
a.传统血液透析与血液透析滤过:基于液‑液分离原理,依赖大量透析液清除血液中水分。
b.无透析液方案:通过跨GBM 膜的液‑气相变实现血液脱水。
c.基于液‑气相变分离的血液净化器设计思路。
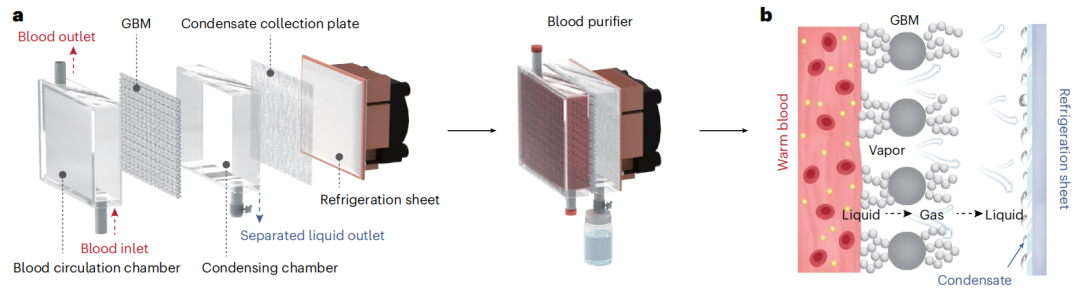
图3 无透析液血液净化器的设计
a 血液净化器组件示意图,b 液‑气相变脱水分离机制示意图。
本研究在20只健康兔中评估了该血液净化器的有效性与安全性(图4a)。经灭菌处理和麻醉后,分离兔股动脉及静脉并置管。留置针穿刺成功后,肝素 化兔通过血液净化器建立体外循环(图4b),在温控调节下维持3 ml/min的流速。体外血液净化持续约6小时,期间在石墨烯基底膜(GBMs)上未见明显血液黏附或血栓形成。成功实现兔血液液体提取,但产量较体外模拟血液实验略有降低,该差异可能反映体内生理环境的复杂性及相对较慢的血流速度。分离液呈无色透明状,白蛋白
化兔通过血液净化器建立体外循环(图4b),在温控调节下维持3 ml/min的流速。体外血液净化持续约6小时,期间在石墨烯基底膜(GBMs)上未见明显血液黏附或血栓形成。成功实现兔血液液体提取,但产量较体外模拟血液实验略有降低,该差异可能反映体内生理环境的复杂性及相对较慢的血流速度。分离液呈无色透明状,白蛋白 始终未检出,表明相分离过程中实现了有效的蛋白质保留。成分分析意外发现16只兔分离液中存在尿素
始终未检出,表明相分离过程中实现了有效的蛋白质保留。成分分析意外发现16只兔分离液中存在尿素 和尿酸(UA),13只兔检出肌酐,浓度差异提示该群体可能存在肾功能差异。推测这些微量小分子代谢产物可能与水分子形成氢键,通过水分子簇蒸发过程被排出,其中部分随后冷凝并被收集。
和尿酸(UA),13只兔检出肌酐,浓度差异提示该群体可能存在肾功能差异。推测这些微量小分子代谢产物可能与水分子形成氢键,通过水分子簇蒸发过程被排出,其中部分随后冷凝并被收集。
治疗后,五只实验兔在喂养期间接受后续观察,一周内健康状况保持稳定。实验分析证实动脉血气参数无显著改变,干预前后的动脉血氧分压及二氧化碳分压无统计学差异。外周血氧饱和度始终高于95%,证实经血液净化器及GBMs的体外循环未产生气栓或引起血氧水平波动。红细胞在不同递增压力下的变形能力曲线高度重合,最大变形系数约为0.56。溶血率始终低于5%阈值,血浆游离血红蛋白 浓度稳定在20 ng/ml。实验期间血液学指标保持稳定,血小板计数及红细胞计数波动无临床意义。整个治疗过程中肝脏及代谢参数保持稳定,血清白蛋白和总蛋白水平无统计学显著偏差。电解质稳态同样得以维持,包括钾离子、钠离子、氯离子和钙离子。关键的是,细胞因子(IL-1β、IL-6及TNF-α)及损伤相关蛋白HMGB1的血浆浓度均维持在基线水平,证实体外循环未诱发延迟性炎症级联反应。肾、肺及肝组织的苏木精-伊红染色显示,与对照组相比,治疗组实验兔实质结构完整,证实装置或GBMs未引起器官毒性。血液及主要器官中硅的定量分析显示元素浸出极少,验证了二氧化硅包覆的GBMs表面结构完整性。综上所述,这些研究结果支持利用无透析液血液安全有效地清除动物体内多余水分。
浓度稳定在20 ng/ml。实验期间血液学指标保持稳定,血小板计数及红细胞计数波动无临床意义。整个治疗过程中肝脏及代谢参数保持稳定,血清白蛋白和总蛋白水平无统计学显著偏差。电解质稳态同样得以维持,包括钾离子、钠离子、氯离子和钙离子。关键的是,细胞因子(IL-1β、IL-6及TNF-α)及损伤相关蛋白HMGB1的血浆浓度均维持在基线水平,证实体外循环未诱发延迟性炎症级联反应。肾、肺及肝组织的苏木精-伊红染色显示,与对照组相比,治疗组实验兔实质结构完整,证实装置或GBMs未引起器官毒性。血液及主要器官中硅的定量分析显示元素浸出极少,验证了二氧化硅包覆的GBMs表面结构完整性。综上所述,这些研究结果支持利用无透析液血液安全有效地清除动物体内多余水分。
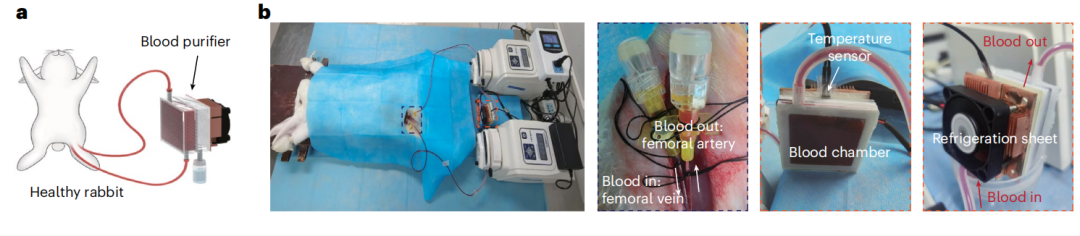
图4 血液净化器在兔模型体内的疗效与安全性
a 兔血液净化装置作用示意图,b 血液净化器用于兔体内血液循环的实物图。
为推进无透析液可穿戴人工肾脏原型机的研发,本研究采用协同策略将血液净化器与血液灌流 柱相结合,实现了从血液中同步清除过量水分和广谱尿毒症毒素的功能。选用市售树脂吸附剂,基于标准商用血液灌流柱构建吸附柱模型。研究证实,该树脂除具备公认的中大分子毒素吸附能力外,对肌酐具有高平衡吸附量,且其低解吸率表明结合稳定性强,具备与血液净化器协同联用实现尿毒症毒素与体液超载同步清除的潜力。在急性肾损伤兔模型中,血液灌流技术的引入未影响血液净化器的水清除效能。与假手术组相比,单纯血液净化器治疗组与无透析液WAK原型机治疗组的急性肾损伤兔血清白蛋白及总蛋白水平均无统计学显著差异。
柱相结合,实现了从血液中同步清除过量水分和广谱尿毒症毒素的功能。选用市售树脂吸附剂,基于标准商用血液灌流柱构建吸附柱模型。研究证实,该树脂除具备公认的中大分子毒素吸附能力外,对肌酐具有高平衡吸附量,且其低解吸率表明结合稳定性强,具备与血液净化器协同联用实现尿毒症毒素与体液超载同步清除的潜力。在急性肾损伤兔模型中,血液灌流技术的引入未影响血液净化器的水清除效能。与假手术组相比,单纯血液净化器治疗组与无透析液WAK原型机治疗组的急性肾损伤兔血清白蛋白及总蛋白水平均无统计学显著差异。
对于小分子肌酐而言,当血液流经GBMs时,肌酐可能以分子团簇形式伴随水蒸气一同透过GBMs。树脂吸附剂所增强的额外清除效能,进一步促进了肌酐从血液循环中的排泄。相比之下,对于中分子毒素β2-微球蛋白,该血液净化器的清除效果可忽略不计,表明GBMs对蛋白质的吸附作用极小。然而,当与血液灌流柱联合使用时,观察到对β2-微球蛋白的清除效果显著提升,使其水平降至建模前状态。这一现象可归因于血液灌流中树脂颗粒对中、高分子量物质卓越的吸附效率。显然,通过将血液净化器与特定匹配的血液灌流吸附柱整合以构建无需透析液的WAK原型,能够实现从血液中持续清除多余水分及多种尿毒症毒素。

图5 无透析液可穿戴人工肾(WAK)原型机的研制
a.通过并联堆叠多个血液循环腔与浓缩腔,提升无透析液WAK脱水效率的设计思路
b.WAK原型机实物图
传统的血液透析和血液透析滤过方法需要大量的液体来实现液-液交换,这对WAK的便携性构成了挑战。基于液-气相变的水分移除机制,为开发真正便携的WAK设备提供了新的可能性。本研究提出一种无透析液的可穿戴人工肾原型,采用基于梯度泡沫金属的血液净化器选择性清除体内多余水分,并结合血液灌流吸附树脂去除尿毒症毒素。通过精确调控饱和蒸气压差,该系统可高效控制液-气相变过程,实现超越传统血液透析的水分清除通量。在20只兔子的体内循环实验中,我们验证了该血液净化器的安全性、可行性和有效性。此外,当与血液灌流联用时,该无透析液WAK原型能够实时、持续地清除急性肾损伤模型兔体内的多余水分和尿毒症毒素(肌酐和β2-微球蛋白)。
当前原型机的主要优势在于其脱水能力。尽管通过集成血液灌流柱改善了毒素清除效果,但尿毒症毒素的清除谱仍有待进一步开发。同样,未来的迭代版本可以采用先进的血液相容性涂层或区域抗凝策略,以最大限度地减少全身抗凝剂的暴露。尽管当前原型机在轻量化和人体工程学设计后仍重约3.8公斤,日常佩戴可能仍有负担,但其性能标志着无透析液净化技术取得了关键性进展。未来在微型化、轻质材料以及与移动辅助设备集成方面的工程努力,对于实现实用的可穿戴应用至关重要。这款无透析液的可穿戴人工肾可被患者持续佩戴,使他们无需每周多次定期前往血液透析中心,这有望提高血液净化治疗的可负担性,减轻经济负担,并改善患者的生活质量和行动能力。这款基于气液相变技术的无透析液可穿戴人工肾原型机,有望成为开发便携式或可穿戴血液净化系统的一条途径,最终为居家血液净化带来希望。
参考文献:
Luo J, Yu H, Yang X, et al. A dialysate-free wearable artificial kidney prototype driven by a liquid–gas phase transition. Nat Chem Eng 3, 128–138 (2026). https://doi.org/10.1038/s44286-026-00355-6.
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。仅供HCP观看。

