
填补国内大疱性类天疱疮靶向治疗空白!度普利尤单抗中国获批,Ⅲ期研究显示持续缓解率提升5倍 | 皮科大事件
来源:
2026.02.28
我要投稿
编者按
2月27日,赛诺菲宣布度普利尤单抗注射液 获国家药品监督管理局(NMPA)正式批准两项新适应症:用于治疗大疱性类天疱疮
获国家药品监督管理局(NMPA)正式批准两项新适应症:用于治疗大疱性类天疱疮 (bullous pemphigoid,BP)成人患者,以及用于6岁及以上儿童哮喘
(bullous pemphigoid,BP)成人患者,以及用于6岁及以上儿童哮喘 患者的维持治疗。此次获批标志着度普利尤单抗成为中国首个且目前唯一获批用于治疗大疱性类天疱疮的靶向生物制剂,为这一好发于老年人的慢性自身免疫性皮肤病带来突破性的创新治疗选择。
患者的维持治疗。此次获批标志着度普利尤单抗成为中国首个且目前唯一获批用于治疗大疱性类天疱疮的靶向生物制剂,为这一好发于老年人的慢性自身免疫性皮肤病带来突破性的创新治疗选择。

疾病负担沉重,老年患者亟需新方案
 和免疫抑制剂为主,但长期使用存在明显副作用。
和免疫抑制剂为主,但长期使用存在明显副作用。全球III期研究ADEPT:持续缓解率提升5倍
此次获批基于关键性II/III期临床试验ADEPT(NCT04206553)的积极结果。该研究是一项为期52周的随机、双盲、安慰剂对照临床试验,共纳入106例中重度BP成人患者,评估了度普利尤单抗(300mg,每2周1次)联合口服糖皮质激素(OCS)对比安慰剂联合OCS的疗效和安全性。

图1 LIBERTY-BP ADEPT II/III 期临床试验设计与研究终点概览
研究结果显示,治疗第36周:
持续缓解率提升5倍:度普利尤单抗组20%患者实现病情持续缓解,安慰剂组仅4%(p=0.0114) 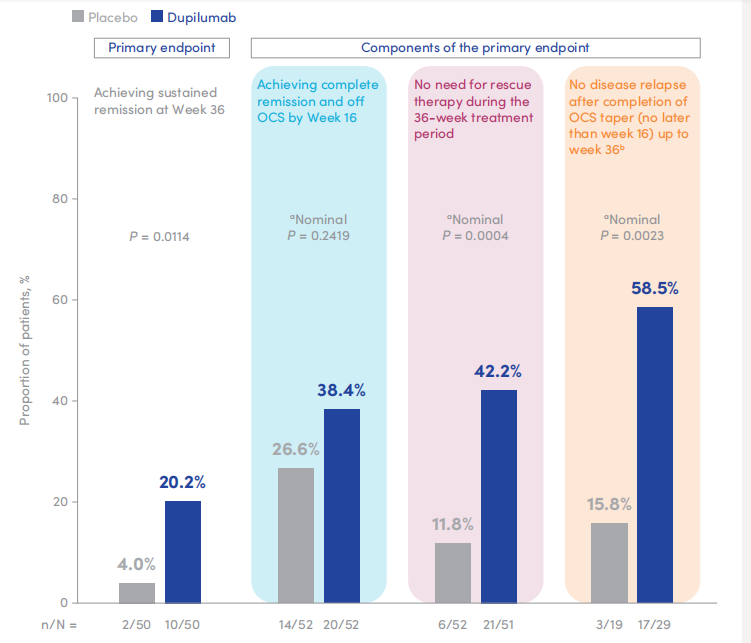
图2 度普利尤单抗组与安慰剂组36周时大疱性类天疱疮持续缓解率及主要终点各组成部分对比
疾病严重程度显著改善:40%患者疾病严重程度下降>90%,安慰剂组为10%(p=0.0003) 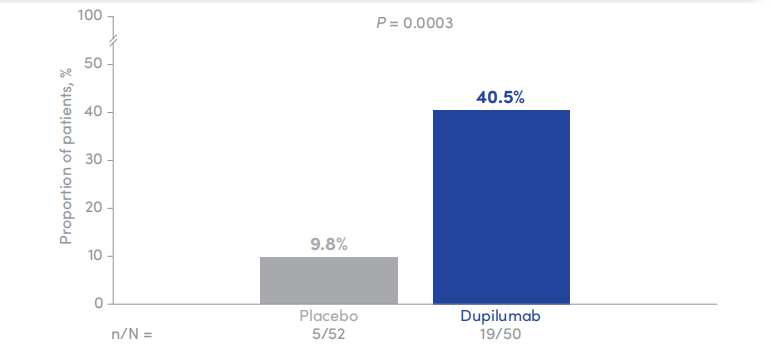
图3 度普利尤单抗组与安慰剂组36周时大疱性类天疱疮疾病面积指数(BPDAI)较基线降低≥90% 的患者比例对比
瘙痒快速缓解:40%患者实现了具有临床意义的瘙痒改善,安慰剂组为11%(p=0.0006) 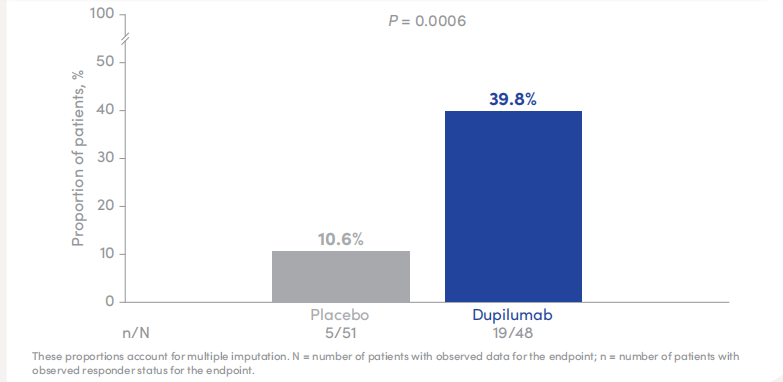
图4 度普利尤单抗组与安慰剂组36周时峰值瘙痒数字评定量表(PP-NRS)较基线降低≥4分的患者比例对比
激素减量优势
激素用量显著减少:平均累计OCS暴露量减少1678 mg(p=0.0220),抢救药物使用风险降低54%(p=0.0016) OCS停药天数增加:停用OCS的天数达40天,安慰剂组仅13天(p=0.0072) 度普利尤单抗组中位累计OCS剂量为2.8g,安慰剂组为4.1g
长期间隔给药
安全性良好

机制精准靶向,从源头阻断2型炎症
 及瘙痒的同时,减少患者对激素药物的依赖。
及瘙痒的同时,减少患者对激素药物的依赖。
未来展望:拓展2型炎症治疗版图
 、哮喘、慢性鼻窦炎
、哮喘、慢性鼻窦炎 伴鼻息肉(CRSwNP)、嗜酸性粒细胞性食管炎(EoE)、结节性痒疹、慢性自发性荨麻疹
伴鼻息肉(CRSwNP)、嗜酸性粒细胞性食管炎(EoE)、结节性痒疹、慢性自发性荨麻疹 (CSU)、慢性阻塞性肺疾病
(CSU)、慢性阻塞性肺疾病 (COPD)以及大疱性类天疱疮(BP)。
(COPD)以及大疱性类天疱疮(BP)。外用药控制不佳或不建议使用外用药的成人、青少年、儿童、6个月及以上婴幼儿全年龄段中重度特应性皮炎 适合系统治疗的中度至重度成人结节性痒疹 成人大疱性类天疱疮 6岁及以上儿童和成人哮喘患者的维持治疗 慢性阻塞性肺疾病成人患者的维持治疗
医脉通是专业的在线医生平台,“感知世界医学脉搏 ,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。

